1 . 元素周期律:元素的性质随元素原子的_______ 递增发生_______ 的规律。
您最近一年使用:0次
2 . 氧化还原离子方程式要求:原子、电子和电荷都守恒。已知:在一定条件下,RO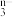 和I-发生反应的离子方程式如下:RO
和I-发生反应的离子方程式如下:RO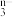 +6I-+6H+=R-+3I2+3H2O。回答下列问题:
+6I-+6H+=R-+3I2+3H2O。回答下列问题:
(1)从电荷守恒角度判断,RO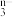 中n=
中n=____ 。
(2)RO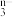 中R元素的化合价是
中R元素的化合价是____ 。
(3)生成物R-是稳定结构,R-的最外层电子数是____ 。
(4)I2使淀粉碘化钾溶液变蓝。检验RO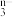 的方法是:取样,
的方法是:取样,____ 。
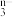 和I-发生反应的离子方程式如下:RO
和I-发生反应的离子方程式如下:RO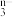 +6I-+6H+=R-+3I2+3H2O。回答下列问题:
+6I-+6H+=R-+3I2+3H2O。回答下列问题:(1)从电荷守恒角度判断,RO
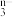 中n=
中n=(2)RO
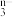 中R元素的化合价是
中R元素的化合价是(3)生成物R-是稳定结构,R-的最外层电子数是
(4)I2使淀粉碘化钾溶液变蓝。检验RO
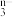 的方法是:取样,
的方法是:取样,
您最近一年使用:0次
解题方法
3 . 元素周期律
(1)元素周期律的内容:随着元素核电荷数的递增,元素的______ (除稀有气体元素外)、元素的________ 、元素的________ 和________ 都呈现周期性变化。元素周期律是指元素的性质随着核电荷数的递增_______ 的规律。
(2)元素周期律的实质:元素周期律是_______ 的必然结果。
(1)元素周期律的内容:随着元素核电荷数的递增,元素的
(2)元素周期律的实质:元素周期律是
您最近一年使用:0次
4 . 元素化合价的变化规律
(1)1~18号元素的最高正化合价的变化规律是______ ,其中_______ 元素没有最高正化合价,最低负化合价的变化规律是_______ 。
(2)元素的最高化合价与最低负化合价的数值与原子最外层电子数的关系是:最高正化合价=_______ (_______ 除外)、最低负化合价=________ 、最高正化合价+|最低负化合价|=________ 。
(3)元素主要化合价呈现周期性变化的根本原因是:随着核电荷数的递增,原子的______ 呈周期性变化。
(1)1~18号元素的最高正化合价的变化规律是
(2)元素的最高化合价与最低负化合价的数值与原子最外层电子数的关系是:最高正化合价=
(3)元素主要化合价呈现周期性变化的根本原因是:随着核电荷数的递增,原子的
您最近一年使用:0次
5 . 原子结构的变化规律
(1)原子最外层电子排布的规律性变化
除H、He外,元素随着原子序数的递增,原子最外电子层数重复出现从_______ 递增到_______ 的变化,说明元素原子的最外层电子数出现_______ 变化。
(2)元素原子半径的变化规律
随着核电荷数的递增,元素的原子半径呈现_______ 变化,原子序数为3~9号及11~17号的元素的原子半径依次________ 。
(1)原子最外层电子排布的规律性变化
除H、He外,元素随着原子序数的递增,原子最外电子层数重复出现从
(2)元素原子半径的变化规律
随着核电荷数的递增,元素的原子半径呈现
您最近一年使用:0次
2022-08-17更新
|
43次组卷
|
2卷引用:课前-5.1.1 元素周期律-苏教版2020必修第一册
6 . 预测钠、钾两种元素原子的得失电子能力强弱,并从原子结构的角度说明理由。_______
您最近一年使用:0次
7 . 含义:元素按其原子_______ 排列的序列称为元素周期系。这个序列中的元素性质随着核电荷数的递增发生_______ 的重复
您最近一年使用:0次
2022-02-16更新
|
111次组卷
|
2卷引用:课前-1.2.1 原子结构与元素周期表-人教版2019选择性必修2
20-21高一上·广东惠州·期末
8 . 如表列出了①~⑩种元素在元素周期表中的位置:
请按要求回答下列问题:
(1)画出这11种元素中,金属性最强的元素的原子结构示意图:___ 。
(2)元素④⑤⑩分别与①形成的气体化合物中,最稳定的是___ (填化合物的化学式)。
(3)元素⑨⑩⑪的最高价氧化物的水化物中,酸性最强的是___ (填化合物的化学式)。
(4)写出⑥⑧的最高价氧化物对应的水化物之间发生反应的离子方程式:___ 。
(5)请从原子结构的角度解释,解释元素⑩的非金属性比元素⑪强的原因:___ 。
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 四 | ⑪ |
(1)画出这11种元素中,金属性最强的元素的原子结构示意图:
(2)元素④⑤⑩分别与①形成的气体化合物中,最稳定的是
(3)元素⑨⑩⑪的最高价氧化物的水化物中,酸性最强的是
(4)写出⑥⑧的最高价氧化物对应的水化物之间发生反应的离子方程式:
(5)请从原子结构的角度解释,解释元素⑩的非金属性比元素⑪强的原因:
您最近一年使用:0次



