名校
1 . 下表是某些短周期元素的电负性数值(鲍林标度)。
(1)根据表中数据归纳元素的电负性的变化规律。__________
(2)试推测,前四周期元素中电负性最小的元素与电负性最大的元素分别是__________ 元素,写出这两种元素形成的化合物的电子式__________ 。
(3)预测 元素电负性的范围
元素电负性的范围__________ 。
(4)一般认为,如果两种成键元素之间的电负性差值大于1.7,它们的原子之间通常形成离子键,电负性差值小于1.7通常形成共价键。请据此预测 属于离子化合物还是共价化合物
属于离子化合物还是共价化合物__________ 。
| 元素符号 |  |  | N | O | F |  |  |  | P | S |  |
| 电负性数值 | 1.0 | 1.5 | 3.0 | 3.5 | 4.0 | 0.9 | 1.2 | 1.5 | 2.1 | 2.5 | 3.0 |
(2)试推测,前四周期元素中电负性最小的元素与电负性最大的元素分别是
(3)预测
 元素电负性的范围
元素电负性的范围(4)一般认为,如果两种成键元素之间的电负性差值大于1.7,它们的原子之间通常形成离子键,电负性差值小于1.7通常形成共价键。请据此预测
 属于离子化合物还是共价化合物
属于离子化合物还是共价化合物
您最近一年使用:0次
2022-11-27更新
|
246次组卷
|
2卷引用:广东省广州市玉岩中学2022-2023学年高二下学期期中考试化学试题
20-21高二·全国·课时练习
解题方法
2 . 下列各选项中,按元素的电负性由大到小排列,顺序正确的是
A.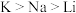 | B.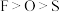 |
C.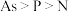 | D.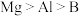 |
您最近一年使用:0次
名校
3 . 下列各组元素中,电负性依次减小的是
| A.F、N、O | B.O、 、F 、F | C. 、P、H 、P、H | D. 、S、 、S、 |
您最近一年使用:0次
2021-12-03更新
|
1023次组卷
|
3卷引用:广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题



