名校
1 . 某实验小组用工业上废渣 主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:
主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g/mL)配制500mL1.0mol/L的硫酸,需要的仪器除量筒、烧杯、玻璃棒、胶头滴管,还有_______ 。
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素。
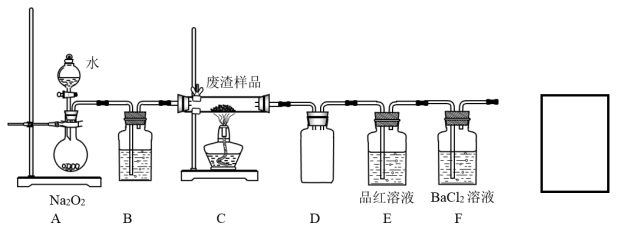
①A中盛有Na2O2的仪器名称为_______ ;装置A中反应的化学方程式为_______
②E装置中品红褪色,F装置盛放的BaCl2溶液中出现白色沉淀,写出生成白色沉淀的离子方程式为_______
③反应装置不完善,为避免空气污染,在方框中补全装置图,并注明试剂名称_______ 。
(3)从下列图中选择合适的装置,写出步骤⑤中进行的操作顺序_______ (填序号)

(4)步骤⑥中由粗铜得到纯铜的方法为_______ (填写名称)
(5)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,实验所得数据如下表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是_______ (填代号)
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为_______ (保留3位有效数字)
 主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:
主要成分Cu2S和Fe2O3制取纯铜和绿矾(FeSO4∙7H2O)产品,设计流程如下:
(1)在实验室中,欲用98%的浓硫酸(密度为1.84g/mL)配制500mL1.0mol/L的硫酸,需要的仪器除量筒、烧杯、玻璃棒、胶头滴管,还有
(2)该小组同学设计如下装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素。

①A中盛有Na2O2的仪器名称为
②E装置中品红褪色,F装置盛放的BaCl2溶液中出现白色沉淀,写出生成白色沉淀的离子方程式为
③反应装置不完善,为避免空气污染,在方框中补全装置图,并注明试剂名称
(3)从下列图中选择合适的装置,写出步骤⑤中进行的操作顺序

(4)步骤⑥中由粗铜得到纯铜的方法为
(5)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
 溶液体积 溶液体积 | 19.10 | 20.02 | 19.98 | 20.00 |
①第1组实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为
您最近一年使用:0次



