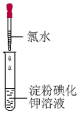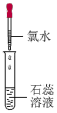名校
解题方法
1 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2、0、+4、+6四种,其不同价态的物质间可相互转化。完成下列填空:
(1)请写出硫在元素周期表的位置:___________ 。
(2)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是___________。
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径: 转化成
转化成 的化学方程式:
的化学方程式:___________ 。
你认为减少酸雨产生的无效措施是___________ (填字母序号)
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.开发新能源
某同学利用如图所示装置探究二氧化硫气体的性质,回答下列问题:___________ 。
(5)当观察到②中溶液颜色变浅时,①中的现象是___________ 。
(6)装置③的作用是___________ 。
(7)②中的现象说明二氧化硫具有的性质是___________ 。
(8)从氧化还原角度制备硫代硫酸钠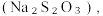 下列方案合理的是(填编号)___________。
下列方案合理的是(填编号)___________。
(9)为进一步减少 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去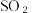 写出该反应的化学方程式:
写出该反应的化学方程式:___________ 。
(1)请写出硫在元素周期表的位置:
(2)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是___________。
A.热稳定性: | B.溶解度: 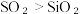 |
C.单质的熔点: | D.酸性:  |
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:

 转化成
转化成 的化学方程式:
的化学方程式:你认为减少酸雨产生的无效措施是
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.开发新能源
某同学利用如图所示装置探究二氧化硫气体的性质,回答下列问题:
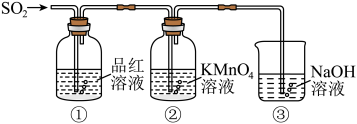
(5)当观察到②中溶液颜色变浅时,①中的现象是
(6)装置③的作用是
(7)②中的现象说明二氧化硫具有的性质是
(8)从氧化还原角度制备硫代硫酸钠
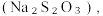 下列方案合理的是(填编号)___________。
下列方案合理的是(填编号)___________。A.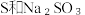 | B. 和浓 和浓 | C.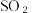 和 和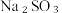 | D.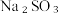 和 和 |
(9)为进一步减少
 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去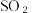 写出该反应的化学方程式:
写出该反应的化学方程式:
您最近一年使用:0次
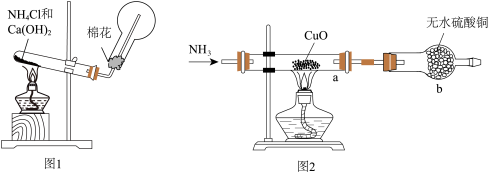
2 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为________________ ,
(2)检验圆底烧瓶中已收集满氨气的方法是________________ 。
Ⅱ、探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(3)无水硫酸铜的作用是________ ,有同学认为需要在无水硫酸铜的后面再接一个装有无水 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是________________ 。
(4)实验中观察到a中 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为________________ 。
(5)若向a中通入标准状况下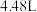 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为________ g。
(1)图1装置中生成
 的化学方程式为
的化学方程式为(2)检验圆底烧瓶中已收集满氨气的方法是
Ⅱ、探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(3)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(4)实验中观察到a中
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(5)若向a中通入标准状况下
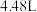 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为
您最近一年使用:0次
2024-05-04更新
|
131次组卷
|
2卷引用:天津市第二十一中学2023-2024学年高一下学期第一次月考化学试卷
解题方法
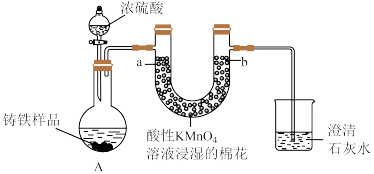
3 . Ⅰ.铸铁的主要成分为Fe和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。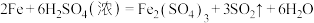 、
、________ 。
(2)实验现象:①________ ,证明确实有SO2生成。
②U型管b侧棉花的紫红色变化不明显、澄清石灰水中生成白色浑浊物。证明________ 。
(3)检测反应后A中所得溶液中含有 的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加
的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加________ ,现象为________ 证明有 。
。
(4)若取上述反应生成的0.56L(标准状况下)混合气体直接通入足量H2O2溶液中,反应完全后,向溶液中加入足量BaCl2溶液生成白色沉淀,分离、干燥后得到固体4.66g。混合气体中SO2的体积分数为________ 。
Ⅱ.纳米Fe具有很高的活性,易被氧化使其表面形成氧化层,对制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究,纳米Fe将 还原为
还原为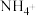 的转化关系如下:
的转化关系如下:

(5)纳米Fe制备原理: ,其中电负性H>B,反应中的氧化剂是
,其中电负性H>B,反应中的氧化剂是________ 。
(6)酸性条件下,纳米Fe和 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是________ 。
(7)检验溶液中 的操作和现象是
的操作和现象是________ 。
(8)溶液初始pH较低有利于 的去除,可能的原因是
的去除,可能的原因是________ (答1条)。
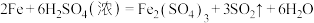 、
、(2)实验现象:①
②U型管b侧棉花的紫红色变化不明显、澄清石灰水中生成白色浑浊物。证明
(3)检测反应后A中所得溶液中含有
 的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加
的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加 。
。(4)若取上述反应生成的0.56L(标准状况下)混合气体直接通入足量H2O2溶液中,反应完全后,向溶液中加入足量BaCl2溶液生成白色沉淀,分离、干燥后得到固体4.66g。混合气体中SO2的体积分数为
Ⅱ.纳米Fe具有很高的活性,易被氧化使其表面形成氧化层,对制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究,纳米Fe将
 还原为
还原为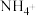 的转化关系如下:
的转化关系如下:
(5)纳米Fe制备原理:
 ,其中电负性H>B,反应中的氧化剂是
,其中电负性H>B,反应中的氧化剂是(6)酸性条件下,纳米Fe和
 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是(7)检验溶液中
 的操作和现象是
的操作和现象是(8)溶液初始pH较低有利于
 的去除,可能的原因是
的去除,可能的原因是
您最近一年使用:0次
4 . 某实验小组探究 的制取、性质及其应用。按要求回答下列问题。
的制取、性质及其应用。按要求回答下列问题。
已知:① 是难溶于水的白色固体
是难溶于水的白色固体
② (无色)
(无色)
【实验i】探究 的制取(如下图所示装置,夹持装置略)
的制取(如下图所示装置,夹持装置略) 溶液(
溶液( )中通入
)中通入 一段时间,至C中溶液的pH为7时向其中滴加一定量
一段时间,至C中溶液的pH为7时向其中滴加一定量 溶液,产生白色沉淀,过滤、洗涤、干燥,得到
溶液,产生白色沉淀,过滤、洗涤、干燥,得到 固体。
固体。
(1)试剂a是___________ 。
(2)向 溶液中通入
溶液中通入 的目的可能是
的目的可能是___________ 。
(3)pH为7时滴加一定量 溶液产生白色沉淀的离子方程式为
溶液产生白色沉淀的离子方程式为___________ 。
(4)同学甲在C中出现白色沉淀之后继续通 ,阐述你认为同学甲的操作合理与否的理由
,阐述你认为同学甲的操作合理与否的理由___________ 。
【实验ii和实验iii】探究 的性质
的性质___________ 。
(6)结合实验ii现象,写出步骤②反应的离子方程式:___________ 。
(7)对比实验ii和实验iii,得出实验结论(填2点):___________ 、___________ 。
【实验iv】探究 的应用
的应用
(8)将 溶于乳酸
溶于乳酸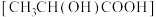 中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性 测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是
测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是___________ 。
 的制取、性质及其应用。按要求回答下列问题。
的制取、性质及其应用。按要求回答下列问题。已知:①
 是难溶于水的白色固体
是难溶于水的白色固体②
 (无色)
(无色)【实验i】探究
 的制取(如下图所示装置,夹持装置略)
的制取(如下图所示装置,夹持装置略)实验i 
 溶液(
溶液( )中通入
)中通入 一段时间,至C中溶液的pH为7时向其中滴加一定量
一段时间,至C中溶液的pH为7时向其中滴加一定量 溶液,产生白色沉淀,过滤、洗涤、干燥,得到
溶液,产生白色沉淀,过滤、洗涤、干燥,得到 固体。
固体。(1)试剂a是
(2)向
 溶液中通入
溶液中通入 的目的可能是
的目的可能是(3)pH为7时滴加一定量
 溶液产生白色沉淀的离子方程式为
溶液产生白色沉淀的离子方程式为(4)同学甲在C中出现白色沉淀之后继续通
 ,阐述你认为同学甲的操作合理与否的理由
,阐述你认为同学甲的操作合理与否的理由【实验ii和实验iii】探究
 的性质
的性质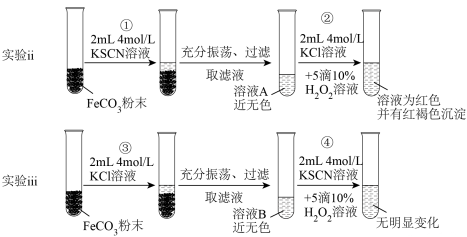
(6)结合实验ii现象,写出步骤②反应的离子方程式:
(7)对比实验ii和实验iii,得出实验结论(填2点):
【实验iv】探究
 的应用
的应用(8)将
 溶于乳酸
溶于乳酸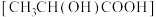 中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性 测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是
测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大于100%(操作误差略),其原因是
您最近一年使用:0次
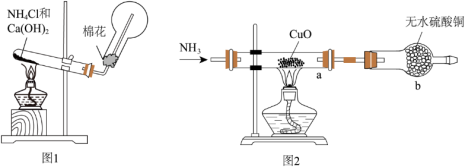
5 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成NH3的化学方程式为______ 。装置中棉花的作用_______ 。
II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是_______ 。
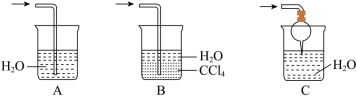
(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是____ (填字母)。________ ,证明氨气具有_____ (填“氧化”或“还原”)性。
(5)若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为_____ g。
(1)图1装置中生成NH3的化学方程式为
II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是
(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是
(5)若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为
您最近一年使用:0次
6 . A、B、C、D四物质有如下转化关系反应条件和部分产物已略去,回答下列问题:
A B
B C
C D
D
Ⅰ、若A为气态氢化物和D能通过化合反应生成一种盐,则
(1)①A的电子式为____ ,实验室制取A的方程式为___________________ ,检验气体B的方法_______ ,写出由A生成B的化学方程式________________ 。
②在标准状况下,某同学用干燥的圆底烧瓶收集瓶A气体,用滴入酚酞的水做喷泉实验,能观察到美丽的红色喷泉。用方程式解释喷泉呈红色的原因________________ 。
Ⅱ、若A与B反应能生成一种淡黄色固体单质
(2)写出该反应的化学方程式__________ ,将B通入 溶液,能观察的现象是
溶液,能观察的现象是____________ ,反应的离子方程式为_________________ 。
Ⅲ、喷泉是一种常见的现象,其产生的原理是存在压强差。试回答下列问题:_____________________________________
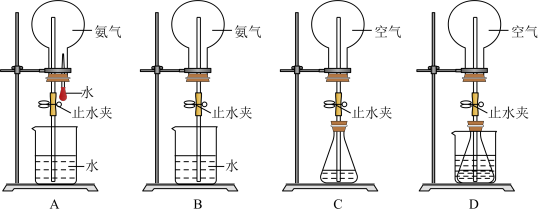
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是______________ 。
②利用图B装置引发喷泉的操作是________________________ 。
(4)利用图C装置,在锥形瓶中分别加入足量的下列物质,可能产生喷泉的有 。
(5)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是 。
(6)同温同压下,两个等体积的干燥圆底烧瓶中分别充满 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是 。
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是 。
A
 B
B C
C D
DⅠ、若A为气态氢化物和D能通过化合反应生成一种盐,则
(1)①A的电子式为
②在标准状况下,某同学用干燥的圆底烧瓶收集瓶A气体,用滴入酚酞的水做喷泉实验,能观察到美丽的红色喷泉。用方程式解释喷泉呈红色的原因
Ⅱ、若A与B反应能生成一种淡黄色固体单质
(2)写出该反应的化学方程式
 溶液,能观察的现象是
溶液,能观察的现象是Ⅲ、喷泉是一种常见的现象,其产生的原理是存在压强差。试回答下列问题:
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
②利用图B装置引发喷泉的操作是
(4)利用图C装置,在锥形瓶中分别加入足量的下列物质,可能产生喷泉的有 。
| A.Cu与稀盐酸 | B.Fe与稀硫酸 |
| C.Cu与稀硝酸 | D. 溶液与NaOH溶液 溶液与NaOH溶液 |
(5)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是 。
| A.浓硫酸 | B.食盐 | C.硝酸钾 | D.硫酸铜 |
(6)同温同压下,两个等体积的干燥圆底烧瓶中分别充满
 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是 。
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是 。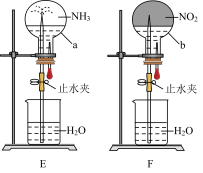
| A.a>b | B.a<b | C.a=b | D.不能确定 |
您最近一年使用:0次
2024·辽宁鞍山·二模
解题方法
7 . 某实验小组在探究 性质时,做了如下实验:
性质时,做了如下实验:
实验Ⅰ:向NaCl溶液中加入 溶液,溶液呈绿色。
溶液,溶液呈绿色。
实验Ⅱ:向 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
实验Ⅲ:向 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。
实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。
资料显示: 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。
下列说法错误的是
 性质时,做了如下实验:
性质时,做了如下实验:实验Ⅰ:向NaCl溶液中加入
 溶液,溶液呈绿色。
溶液,溶液呈绿色。实验Ⅱ:向
 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。实验Ⅲ:向
 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入
 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。资料显示:
 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。下列说法错误的是
A.实验Ⅰ: 在NaCl溶液中部分转化为 在NaCl溶液中部分转化为 |
B.实验Ⅱ:Mg消耗了溶液中的 从而产生了 从而产生了 |
C.实验Ⅲ:有 生成 生成 |
D.实验Ⅳ:获得的蓝色沉淀为 |
您最近一年使用:0次
解题方法
8 . 氯气是一种重要的化工原料,可用于制备盐酸、漂白剂和杀菌消毒剂等。
(1)1774年的舍勒用软锰矿粉末(主要成分是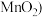 和浓盐酸混合加热制备氯气。反应的化学方程式为:
和浓盐酸混合加热制备氯气。反应的化学方程式为:_______ ;其中,_______ 是还原剂,_______ 是还原产物。
(2)某化学兴趣小组用不同的方法利用下图装置制取并探究氯气的性质。A装置中发生反应的化学方程式为:
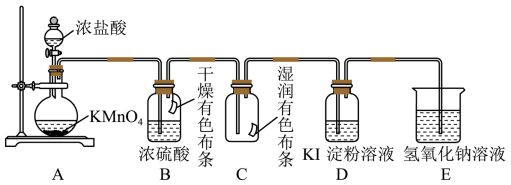
按图组装好实验装置后,首先进行的操作是_______ 。
(3)A装置中盛放浓盐酸的仪器的名称是_______ ,B装置中浓硫酸的作用_______ 。
(4)实验进行一段时间后,可观察到_______ (填“B”或“C” )装置中有色布条褪色。
(5)已知:Cl2+2KI=I2+2KCl。当氯气进入D装置后,可观察到溶液颜色变为_______ (填“红色”或“蓝色”)。
(6)E装置中NaOH溶液的作用是_______ 。
(1)1774年的舍勒用软锰矿粉末(主要成分是
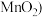 和浓盐酸混合加热制备氯气。反应的化学方程式为:
和浓盐酸混合加热制备氯气。反应的化学方程式为:(2)某化学兴趣小组用不同的方法利用下图装置制取并探究氯气的性质。A装置中发生反应的化学方程式为:


按图组装好实验装置后,首先进行的操作是
(3)A装置中盛放浓盐酸的仪器的名称是
(4)实验进行一段时间后,可观察到
(5)已知:Cl2+2KI=I2+2KCl。当氯气进入D装置后,可观察到溶液颜色变为
(6)E装置中NaOH溶液的作用是
您最近一年使用:0次
9 . 用如图所示实验装置(夹持仪器已省略)探究铜丝与过量浓硫酸的反应。下列实验不合理的是
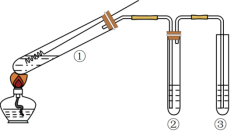
A.移动装置①中铜丝可控制 的量 的量 |
B.装置②中选用品红溶液验证 的生成 的生成 |
C.装置③中选用 溶液吸收多余的 溶液吸收多余的 |
D.向装置①反应后溶液中直接加水,确认有 生成 生成 |
您最近一年使用:0次
2024-03-20更新
|
289次组卷
|
4卷引用:天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(理科)
天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(理科)(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省眉山市仁寿第一中学校(北校区)2023-2024学年高一下学期3月月考化学试题黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷
10 . 二氧化锰与浓盐酸在加热的条件下会生成氯气,化学小组同学设计如下实验验证氯气的部分性质,并探究氯水的成分和性质。
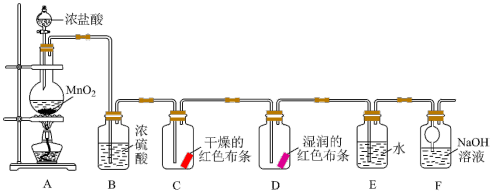
回答下列问题:
(1)验证干燥的氯气没有漂白性的现象为_________ 。
(2)装置F的作用是_________ 。
(3)研究新制氯水成分和性质。以装置E的溶液进行下列实验
资料:淀粉的特征反应——遇I2变蓝色。
①根据实验1可知氧化性:Cl2_________ I2(填“>”或“<”)。
②实验2中证明溶液中含有_________ (填微粒的化学式)。
③若用实验3证明氯水中含有氯离子,用离子方程式表示产生该实验现象的反应:_________ 。
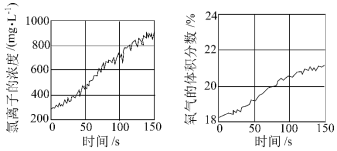
(4)同学们发现久置的氯水会失去漂白性。为探究氯水失效的原因进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定数据,得到如图曲线。两图中曲线变化的原因是_________ (用化学方程式表示)。

回答下列问题:
(1)验证干燥的氯气没有漂白性的现象为
(2)装置F的作用是
(3)研究新制氯水成分和性质。以装置E的溶液进行下列实验
实验序号 | 实验1 | 实验2 | 实验3 |
实验操作 |
|
| |
实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 有白色沉淀生成 |
①根据实验1可知氧化性:Cl2
②实验2中证明溶液中含有
③若用实验3证明氯水中含有氯离子,用离子方程式表示产生该实验现象的反应:
(4)同学们发现久置的氯水会失去漂白性。为探究氯水失效的原因进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定数据,得到如图曲线。两图中曲线变化的原因是

您最近一年使用:0次