名校
解题方法
1 . 实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。_______ 。
(2)装置E的作用是_______ 。(用离子方程式表示)
(3)装置D用于验证 的
的_______ 性,发生的化学方程式为_______ 。
(4)装置C中的现象是_______ ;若将C中的溴水改为酸性高锰酸钾溶液,现象为_______ ,发生的离子方程式为_______ 。
(5)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是_______ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。

实验中若通过空气的体积为 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是_______ 。(结果精确到0.001%)
 的性质并测定空气中
的性质并测定空气中 的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。
的体积分数。他们设计了如图所示的实验装置,请你参与探究并回答问题。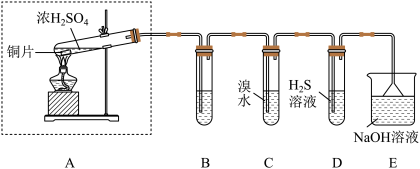
(2)装置E的作用是
(3)装置D用于验证
 的
的(4)装置C中的现象是
(5)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中a导管的作用是
装置如图所示。其中a导管的作用是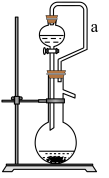
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
实验中若通过空气的体积为
 (标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
(标准状况下),最终所得固体质量为0.466g,通过计算确定该空气中二氧化硫的含量是
您最近一年使用:0次
2 . Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究 与
与 反应产生沉淀的条件。下列判断错误的是
反应产生沉淀的条件。下列判断错误的是
 与
与 反应产生沉淀的条件。下列判断错误的是
反应产生沉淀的条件。下列判断错误的是
| A.玻璃管的作用是连通大气,平衡压强 |
| B.Y形管乙中产生的可能为氧化性气体 |
| C.e、f两管中的试剂可以分别是浓氨水和NaOH固体 |
D.c、d两根导管都必须插入 溶液中,保证气体与 溶液中,保证气体与 充分接触 充分接触 |
您最近一年使用:0次
2024-03-26更新
|
238次组卷
|
2卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高一下学期4月月考化学试题
解题方法
3 . 实验室可用图中装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。___________ ,装置A中发生反应的化学方程式为___________ 。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若___________ ,则整个装置气密性良好。
(3)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择___________ (填序号)。
a.蒸馏水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液
(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案II:向第二份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案III:向第三份溶液中加入 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。
上述方案中合理的是方案___________ (填“I”“II”或“III”)。
 并验证其性质。
并验证其性质。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若
(3)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择a.蒸馏水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案II:向第二份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案III:向第三份溶液中加入
 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。上述方案中合理的是方案
您最近一年使用:0次
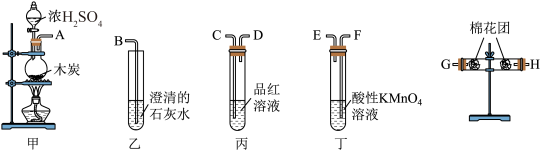
4 . 用如图所示的装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。___________ 。再此反应中硫酸显___________ 性。
如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A接G,H接C,D接F,E接C,D接B。
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中___________ ,第二次使用的丙中 ___________ ;
(3)丁中酸性KMnO4溶液的作用是___________ ;
(4)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的横线上:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
Ⅰ.在化学实验中,浓硫酸可干燥剂。___________ 。
Ⅱ.Cu与浓H2SO4反应,可生成CuSO4和SO2。___________ 。
Ⅲ.向滤纸上滴加浓H2SO4,滤纸变黑。___________ 。
Ⅳ.在冷浓H2SO4中放入铁片没明显现象。___________ 。
如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A接G,H接C,D接F,E接C,D接B。
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中
(3)丁中酸性KMnO4溶液的作用是
(4)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的横线上:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
Ⅰ.在化学实验中,浓硫酸可干燥剂。
Ⅱ.Cu与浓H2SO4反应,可生成CuSO4和SO2。
Ⅲ.向滤纸上滴加浓H2SO4,滤纸变黑。
Ⅳ.在冷浓H2SO4中放入铁片没明显现象。
您最近一年使用:0次
名校
解题方法
5 . 如图装置可用于收集气体并验证其某些化学性质能达到目的的是


选项 | 气体 | 试剂 | 现象 | 结论 |
A |
| 酚酞试液 | 溶液变红色 | 氨水显碱性 |
B |
| 紫色石蕊试液 | 溶液先变红后褪色 |  有酸性和漂白性 有酸性和漂白性 |
C |
| 溴水 | 溶液褪色 |  有氧化性 有氧化性 |
D | X | KI淀粉溶液 | 溶液变蓝 | X可能是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。
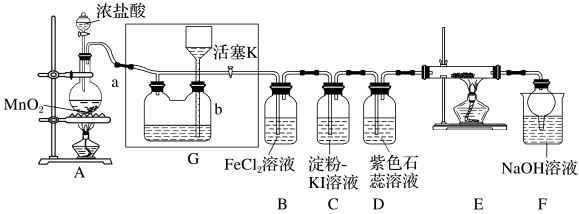
(1)A中发生反应的化学方程式为___________ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是___________ 。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为___________ 。
③装置F中球形干燥管的作用是___________ 。
(3)储气瓶b内盛放的试剂是___________ 。
(4)装置B中Fe2+被Cl2氧化为Fe3+,反应的离子方程式为___________ 。
(5)工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,该反应的化学方程式为___________ ,所得漂白粉的有效成分是___________ (填物质名称)。

(1)A中发生反应的化学方程式为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为
③装置F中球形干燥管的作用是
(3)储气瓶b内盛放的试剂是
(4)装置B中Fe2+被Cl2氧化为Fe3+,反应的离子方程式为
(5)工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 氯气常用于自来熟的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)写出该反应的离子方程式:_______ ,其中氧化剂和还原剂的物质的量之比为_______ 。
(2)若 和
和 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为_______。(不考虑盐酸的挥发)
盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为_______。(不考虑盐酸的挥发)
(3)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为 。据此回答下列问题:装置如图所示,同时验证氯气性质(其中夹持装置已省略)
。据此回答下列问题:装置如图所示,同时验证氯气性质(其中夹持装置已省略)
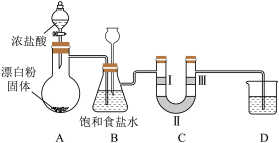
①从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是_______ 。
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:_______ 。
③装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是_______ (填序号)。
④装置D的烧杯内是NaOH溶液,其作用是_______ ,发生的反应的离子方程式:_______ 。
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效氨气的消毒剂。 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是_______(填序号)。
除去,下列试剂能实现其转化过程的是_______(填序号)。
(1)写出该反应的离子方程式:
(2)若
 和
和 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为_______。(不考虑盐酸的挥发)
盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为_______。(不考虑盐酸的挥发)| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(3)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为
 。据此回答下列问题:装置如图所示,同时验证氯气性质(其中夹持装置已省略)
。据此回答下列问题:装置如图所示,同时验证氯气性质(其中夹持装置已省略)
①从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
③装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| 序号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效氨气的消毒剂。
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是_______(填序号)。
除去,下列试剂能实现其转化过程的是_______(填序号)。A. | B. | C.KI | D. |
您最近一年使用:0次
名校
解题方法
8 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
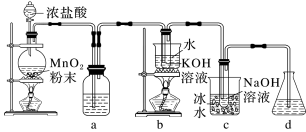
回答下列问题:
(1)浓盐酸在反应过程中表现出来的性质有:___________ (填字母)。
a.酸性 b.氧化性 c.还原性 d.碱性 e.易挥发性
(2)a中的试剂为___________ 。b中发生的化学反应的离子方程式是___________ 。
(3)d中可选用试剂___________ (填字母)。
a. 溶液 b.饱和
溶液 b.饱和 溶液 c.石灰乳 d.稀
溶液 c.石灰乳 d.稀
(4)反应结束后,取出b中试管,经冷却结晶,过滤,___________ ,干燥,得到 晶体。
晶体。
(5)取少量 和
和 溶液置于两支试管中,分别滴加一定浓度的中性淀粉
溶液置于两支试管中,分别滴加一定浓度的中性淀粉 溶液。装有
溶液。装有 的试管溶液颜色不变,装有
的试管溶液颜色不变,装有 的试管溶液变为蓝色。由此可知在该条件下,氧化能力
的试管溶液变为蓝色。由此可知在该条件下,氧化能力
___________  (填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:
(填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:___________ 。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)浓盐酸在反应过程中表现出来的性质有:
a.酸性 b.氧化性 c.还原性 d.碱性 e.易挥发性
(2)a中的试剂为
(3)d中可选用试剂
a.
 溶液 b.饱和
溶液 b.饱和 溶液 c.石灰乳 d.稀
溶液 c.石灰乳 d.稀
(4)反应结束后,取出b中试管,经冷却结晶,过滤,
 晶体。
晶体。(5)取少量
 和
和 溶液置于两支试管中,分别滴加一定浓度的中性淀粉
溶液置于两支试管中,分别滴加一定浓度的中性淀粉 溶液。装有
溶液。装有 的试管溶液颜色不变,装有
的试管溶液颜色不变,装有 的试管溶液变为蓝色。由此可知在该条件下,氧化能力
的试管溶液变为蓝色。由此可知在该条件下,氧化能力
 (填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:
(填“大于”或“小于”)。溶液变蓝的试管内发生反应的离子方程式为:
您最近一年使用:0次
2023-12-21更新
|
127次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
9 . 氯气、“84”消毒液、源白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
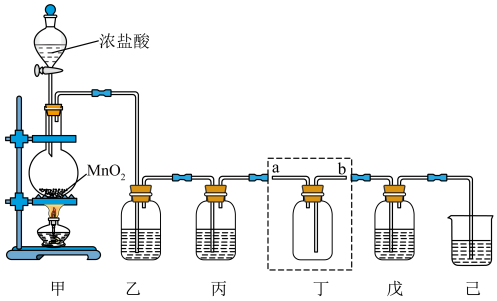
(1)装置甲中发生反应的化学方程式为_______ ,盛装浓盐酸的仪器的名称为________ 。
(2)实验开始前应进行的操作是___________ 。
(3)装置丁用来收集纯净且干燥的氯气,进气口为___________ (填a或b);装置乙盛装的试剂是___________ ,其作用是___________ ;丙盛装的试剂是___________ ,其作用是___________ 。(试剂填名称)
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为___________ ;漂白粉长时间暴露在空气中容易发生变质的原因为___________ (结合化学方程式说明)。
(5)实验室中,除上述制取氯气的方法以外,还可利用以下反应: 。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
①写出该反应的离子方程式:___________ 。
②该反应中,氧化剂是___________ ,被氧化的物质是___________ 。

(1)装置甲中发生反应的化学方程式为
(2)实验开始前应进行的操作是
(3)装置丁用来收集纯净且干燥的氯气,进气口为
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
(5)实验室中,除上述制取氯气的方法以外,还可利用以下反应:
 。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
。此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。①写出该反应的离子方程式:
②该反应中,氧化剂是
您最近一年使用:0次
名校
10 . 某小组为了探究硫酸的性质,设计如下实验:
回答下列问题:
(1)实验①没有明显现象的原因是___________ ;改变一个条件,为使实验①中的反应持续发生,改变条件是___________ 。
(2)为了引发实验②中的反应,宜采取的措施是___________ ;实验后,观察产物水溶液的颜色,其操作方法是___________ 。
(3)实验④产生的气体是___________ (填化学式),比较实验③和④可知,从氧化还原角度分析,H+的作用是___________ ;写出该反应的离子方程式:___________ 。
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为___________ ;M能与稀硫酸酸化的KI溶液反应生成白色沉淀CuI(碘化亚铜),在滤液中加入淀粉溶液,溶液变蓝色。写出M和稀硫酸酸化的KI溶液反应的离子方程式:___________ 。
| 序号 | 操作 | 现象 |
| ① | 常温下,在铁片中加入过量的浓硫酸 | 没有明显现象 |
| ② | 常温下,在铜片上加入过量的浓硫酸 | 没有明显现象 |
| ③ | 在铜和过量30%H2O2的混合溶液中加入Na2SO4溶液 | 没有明显现象 |
| ④ | 在铜和过量30%H2O2的混合溶液中加入稀硫酸 | 溶液变蓝色,并产生气泡 |
(1)实验①没有明显现象的原因是
(2)为了引发实验②中的反应,宜采取的措施是
(3)实验④产生的气体是
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为
您最近一年使用:0次
2023-10-22更新
|
73次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高三上学期11月月考化学试题




