1 . 三氯化硼是重要的化工原料。可用于制取乙硼烷( ),也可作有机合成的催化剂。
),也可作有机合成的催化剂。
【查阅资料】① 的沸点为12.5℃,熔点为-107.3℃;
的沸点为12.5℃,熔点为-107.3℃;
② ,硼也能与强碱反应。
,硼也能与强碱反应。
③ 遇潮气会剧烈水解产生白雾。
遇潮气会剧烈水解产生白雾。
某研究性学习小组用如图所示装置制备三氯化硼。回答下列问题:
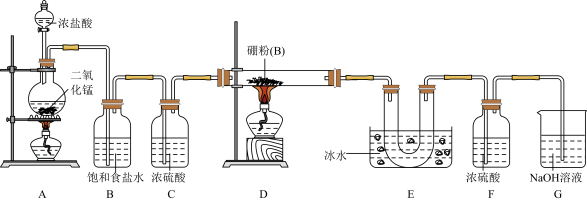
(1)A装置中反应的离子方程式______ 。
(2)B装置的作用是______ ;如果拆去B装置,可能的后果是______ 。
(3)D装置中发生反应的化学方程式______ 。
(4)G装置的作用是______ ;为使实验装置简便,可用一个装置代替F和G装置。该装置所用仪器是______ ,所装试剂是______ 。
(5)A、D两处加热的先后顺序是______ 。
 ),也可作有机合成的催化剂。
),也可作有机合成的催化剂。【查阅资料】①
 的沸点为12.5℃,熔点为-107.3℃;
的沸点为12.5℃,熔点为-107.3℃;②
 ,硼也能与强碱反应。
,硼也能与强碱反应。③
 遇潮气会剧烈水解产生白雾。
遇潮气会剧烈水解产生白雾。某研究性学习小组用如图所示装置制备三氯化硼。回答下列问题:

(1)A装置中反应的离子方程式
(2)B装置的作用是
(3)D装置中发生反应的化学方程式
(4)G装置的作用是
(5)A、D两处加热的先后顺序是
您最近一年使用:0次
2 . 如图是元素周期表的一部分,图中所列的字母分别代表某一种化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第_______ 周期第_______ 族
(2)D简单离子的结构示意图为_______
(3)D单质在空气中燃烧可生成淡黄色粉末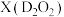 ,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和如图所示实验装置证明X有提供氧气的作用。
,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和如图所示实验装置证明X有提供氧气的作用。
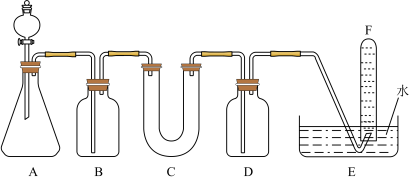
①装置A使用石灰石与稀盐酸反应制取 ,装置B中饱和
,装置B中饱和 溶液的作用是除去
溶液的作用是除去_______ 。
②装置C中X与 反应的化学方程式是
反应的化学方程式是_______ ,装置D盛放NaOH溶液的作用是除去_______ 。
③为检验试管F收集的气体,应_______ ,若出现_______ 现象,即证明X可作供氧剂。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第
(2)D简单离子的结构示意图为
(3)D单质在空气中燃烧可生成淡黄色粉末
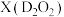 ,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和如图所示实验装置证明X有提供氧气的作用。
,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和如图所示实验装置证明X有提供氧气的作用。
①装置A使用石灰石与稀盐酸反应制取
 ,装置B中饱和
,装置B中饱和 溶液的作用是除去
溶液的作用是除去②装置C中X与
 反应的化学方程式是
反应的化学方程式是③为检验试管F收集的气体,应
您最近一年使用:0次
3 . 某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。

(1)A中发生反应的离子方程式为_______ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置C中能看到的实验现象是_______ ,发生的离子方程式为_______ 。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为_______ 。
③储气瓶b内盛放的试剂是饱和食盐水,作用是_______ 。
(3)装置B中发生的化学方程式是_______ 。

(1)A中发生反应的离子方程式为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置C中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为
③储气瓶b内盛放的试剂是饱和食盐水,作用是
(3)装置B中发生的化学方程式是
您最近一年使用:0次
名校
解题方法
4 . 金属Na、Mg、Al有广泛的应用。
(1)Al在元素周期表中的位置是______ 。
(2)金属镁可以用来生产金属铀(元素符号是U): ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是______ (填化学式,下同),被还原的物质是______ 。
(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
由实验1和实验2得出的结论是:金属性,______ >______ >______ (填元素符号),用原子结构理论解释:同周期元素从左到右,______ 。
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式______ 。
(1)Al在元素周期表中的位置是
(2)金属镁可以用来生产金属铀(元素符号是U):
 ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
| 实验1 | 实验2 |
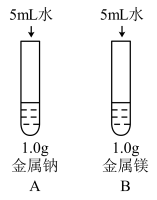 |  |
| 钠与水反应剧烈,镁与水反应缓慢 | 镁与盐酸反应剧烈,铝与盐酸反应缓慢 |
由实验1和实验2得出的结论是:金属性,
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式
您最近一年使用:0次
2022-12-14更新
|
92次组卷
|
2卷引用:新疆伊宁市第八中学2021-2022学年高一上学期期末考试化学试题
5 . 如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
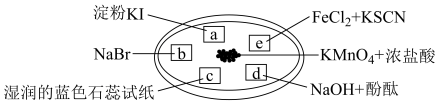
下列说法不正确 的是

下列说法
| A.产生氯气的反应为:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O |
| B.a处变蓝,b处变红棕色,说明氧化性:Cl2>Br2>I2 |
| C.c处先变红,后褪色,证明氯气与水生成酸及具有漂白性的物质 |
| D.d、e处颜色都有改变,反应中消耗等量Cl2时转移的电子数不相同 |
您最近一年使用:0次
2022-10-05更新
|
422次组卷
|
3卷引用:新疆昌吉州行知学校2022-2023学年高一上学期第一次线上月考化学试题
解题方法
6 . 如图是实验室中制备气体或验证气体性质的装置图。

(1)仪器a的名称是________ 。
(2)利用图装置证明SO2具有漂白性、还原性及生成气体中含有CO2。圆底烧瓶内加入碳,a中加入浓硫酸,B、D中均为少量品红溶液,C中为酸性高锰酸钾溶液,E中为澄清石灰水。
①证明SO2通常使用的试剂是________ 。
②证明SO2具有还原性的现象是________ 。
③证明生成气体中含有CO2的现象是________ 。
④证明SO2具有漂白性的装置是________ 。
⑤D装置的作用是________ 。
⑥如果将E中试剂换成硅酸钠溶液,看到E中浑浊,则酸性H2CO3________ H2SiO3(填“=”、“>”或“<”)。
(3)某同学拟用以下方法测定空气中SO2含量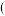 假设空气中无其它还原性气体
假设空气中无其它还原性气体 。
。
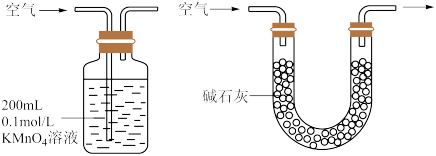
你认为不可行的装置是________  填序号“a”或“b”
填序号“a”或“b” ,理由是
,理由是________ 。

(1)仪器a的名称是
(2)利用图装置证明SO2具有漂白性、还原性及生成气体中含有CO2。圆底烧瓶内加入碳,a中加入浓硫酸,B、D中均为少量品红溶液,C中为酸性高锰酸钾溶液,E中为澄清石灰水。
①证明SO2通常使用的试剂是
②证明SO2具有还原性的现象是
③证明生成气体中含有CO2的现象是
④证明SO2具有漂白性的装置是
⑤D装置的作用是
⑥如果将E中试剂换成硅酸钠溶液,看到E中浑浊,则酸性H2CO3
(3)某同学拟用以下方法测定空气中SO2含量
 假设空气中无其它还原性气体
假设空气中无其它还原性气体 。
。
你认为不可行的装置是
 填序号“a”或“b”
填序号“a”或“b” ,理由是
,理由是
您最近一年使用:0次
7 . 硫酸制备是工业重要课题
I.历史上曾用绿矾(FeSO4·H2O)制备硫酸。高温条件下FeSO4发生如下分解反应:2FeSO4 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
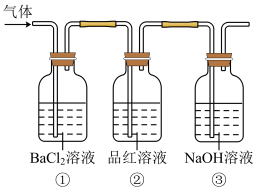
(1)装置①能检验出的气体产物是_______ ,装置②能检验出的气体产物是_______ 。
(2)如果把①和②互换位置对该实验是否有影响:_______ (填是或否)。
II.现代硫酸工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:

(3)接触室中的发生化学方程式_______ ,吸收环节中使用_______ 吸收SO3。
III.某硫酸厂周围的空气中含有较多的二氧化硫,环保部门为了测定空气中二氧化硫的体积分数,做了如下实验。取标准状况下的空气1.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。试回答:
(4)通过足量溴水的离子方程式为:_______ 。
(5)计算该空气样品中二氧化硫的体积分数是_______ 。
I.历史上曾用绿矾(FeSO4·H2O)制备硫酸。高温条件下FeSO4发生如下分解反应:2FeSO4
 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
(1)装置①能检验出的气体产物是
(2)如果把①和②互换位置对该实验是否有影响:
II.现代硫酸工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:

(3)接触室中的发生化学方程式
III.某硫酸厂周围的空气中含有较多的二氧化硫,环保部门为了测定空气中二氧化硫的体积分数,做了如下实验。取标准状况下的空气1.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。试回答:
(4)通过足量溴水的离子方程式为:
(5)计算该空气样品中二氧化硫的体积分数是
您最近一年使用:0次
2022-09-01更新
|
358次组卷
|
3卷引用:新疆石河子第一中学2021-2022学年高一下学期4月月考化学试题
8 . 下图是实验室制取SO2并验证SO2的某些性质的装置,请回答:
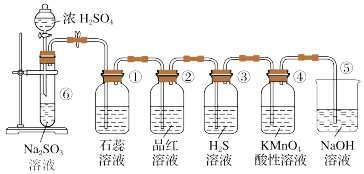
(1)①中的实验现象为石蕊试液________ 。
(2)②中的品红溶液________ ,证明SO2具有________ 性。
(3)③中的涉及的化学反应方程式________ 。
(4)④中的实验现象是________ ,证明SO2有________ 性。
(5)⑤装置的作用是________ 。

(1)①中的实验现象为石蕊试液
(2)②中的品红溶液
(3)③中的涉及的化学反应方程式
(4)④中的实验现象是
(5)⑤装置的作用是
您最近一年使用:0次
9 . 实验室研究不同价态元素的转化,对于物质的制备和应用至关重要。实验室可以用如下图所示装置研究S(+6价)→S(+4价)。
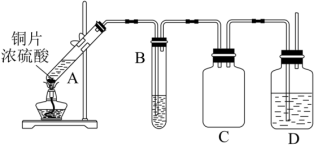
(1)装置C的作用是___________ 。
(2)装置B、D盛放的试剂应分别为___________ 、___________ (填标号)。
a.BaCl2溶液 b.KI淀粉溶液 c.FeSO4溶液 d.NaOH溶液 e.品红溶液
(3)实验结束后,发现装置A中溶液几乎为无色,且试管中有较多的白色固体。试管中溶液显无色,体现了浓硫酸的___________ 性。
(4)实验结束后,若要证明装置A中白色固体为无水CuSO4,需要采取的操作是___________ 。
(5)实验结束后把B取下,用酒精灯加热可以看到的现象是___________

(1)装置C的作用是
(2)装置B、D盛放的试剂应分别为
a.BaCl2溶液 b.KI淀粉溶液 c.FeSO4溶液 d.NaOH溶液 e.品红溶液
(3)实验结束后,发现装置A中溶液几乎为无色,且试管中有较多的白色固体。试管中溶液显无色,体现了浓硫酸的
(4)实验结束后,若要证明装置A中白色固体为无水CuSO4,需要采取的操作是
(5)实验结束后把B取下,用酒精灯加热可以看到的现象是
您最近一年使用:0次
2022-03-21更新
|
200次组卷
|
3卷引用:新疆石河子第一中学2021-2022学年高一5月月考化学试题
10 . 某实验小组同学用下图所示装置制取少量SO2并验证其漂白性,下列说法正确的是
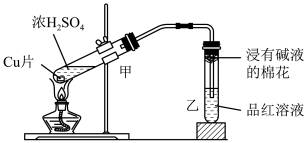

| A.试管甲中发生反应时,浓H2SO4仅显氧化性 |
| B.试管乙中反应时,SO2将品红氧化使溶液褪色 |
| C.浸有碱液的棉花的作用是吸收过量的SO2,防止污染空气 |
| D.实验结束后,取下试管乙,置于酒精灯火焰上加热,溶液无明显变化 |
您最近一年使用:0次
2022-01-22更新
|
643次组卷
|
3卷引用:新疆哈密市第十五中学2021-2022学年高一下学期3月月考试卷化学试题
新疆哈密市第十五中学2021-2022学年高一下学期3月月考试卷化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)吉林省长春市实验中学2021-2022学年高一下学期第一次阶段性考试化学试题



