真题
名校
1 . 为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
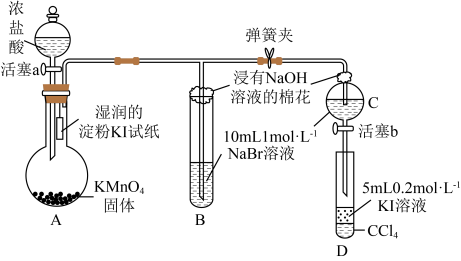
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a。
Ⅳ………
(1)A中产生黄绿色气体,其电子式是________ 。
(2)验证氯气的氧化性强于碘的实验现象是_______ 。
(3)B中溶液发生反应的离子方程式是_______ 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是___________ 。
(5)过程Ⅲ实验的目的是__________ 。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下_________ ,得电子能力逐渐减弱。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a。
Ⅳ………
(1)A中产生黄绿色气体,其电子式是
(2)验证氯气的氧化性强于碘的实验现象是
(3)B中溶液发生反应的离子方程式是
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是
(5)过程Ⅲ实验的目的是
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下
您最近一年使用:0次
2019-01-30更新
|
3098次组卷
|
36卷引用:2015-2016学年天津市静海一中高一下3月月考化学试卷
2015-2016学年天津市静海一中高一下3月月考化学试卷【全国百强校】天津市静海区第一中学2018-2019学年高一下学期3月月考化学试题22010年北京普通高等学校招生全国统一考试理科综合能力测试化学(已下线)2012年鲁科版高中化学选修6 1.2 植物中某些成分的提取练习卷(已下线)2014年高一下学期化学必修2 1-1-2 元素的性质与原子结构练习卷2014-2015学年黑龙江省龙东南四校高一下学期期末联考化学试卷2015-2016学年福建省厦门六中高一下学期期中化学试卷2015-2016学年四川省双流中学高一下期中化学试卷吉林省东北师范大学附属中学净月实验学校2016-2017学年高一下学期期中考试化学试题《课时同步君》2017-2018学年高一化学人教必修2-1.1.2 元素的性质与原子结构(已下线)精做01 元素周期表——《大题精做》2017-2018学年高一化学人教必修2(已下线)《周末培优君》2017-2018学年高一下学期化学-第04周 阶段测评(一) 物质结构 元素周期律【全国百强校】北京师范大学附属中学2017-2018学年高一下学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氯及其化合物【押题专练】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】步步为赢 高一化学暑假作业:作业一 元素周期表(已下线)2019年8月15日 《每日一题》 (一轮复习) 卤素单质性质的相似性和递变性陕西省咸阳市三原南郊中学2020届高三第四次月考化学试题2020届人教版高中化学高三专题基础复习专题2《物质及其变化》测试卷福建省福州市第一中学2020年高一在线自测自评质检化学试题(已下线)考点13 常见非金属元素单质及其重要化合物1——氯-2020年【衔接教材·暑假作业】新高三一轮复习化学人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第一节 原子结构与元素周期表 教材帮(已下线)4.1.4 原子结构与元素的性质(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.1.4 原子结构和元素的性质-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)第10讲 氯及其化合物(练) — 2022年高考化学一轮复习讲练测(新教材新高考)山西省实验中学2021-2022学年高二下学期开学分班素质测试化学试题北京市中国人民大学附属中学2021-2022学年高一下学期期中考试化学试题山东聊城第二中学2022-2023学年高三上学期期中考试化学试题山西省实验中学2021-2022学年高二上学期开学考试化学试题第四章 非金属及其化合物 第19讲 卤素的性质及提取(已下线)题型44 卤素单质及其化合物的相似性和递变性(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练(已下线)第11讲 氯气和卤族元素(已下线)第2讲 卤素及海水提溴、提碘(已下线)考点14 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题
2 . 下列气体的制备和性质实验中,由现象得出的结论错误的是
| 选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
| A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
| B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
| C | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
| D | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-01-30更新
|
2733次组卷
|
30卷引用:2016-2017学年天津市第一中学高一上期末化学卷
2016-2017学年天津市第一中学高一上期末化学卷天津市静海县第一中学2017-2018学年高一上学期期末终结性检测化学试题2016年全国普通高等学校招生统一考试化学(上海卷精编版)2015-2016学年湖南省五市十校教研教改共同体高二下期末化学试卷2017届四川省龙泉中学、温江中学等五校高三上第一次联考化学卷2017届内蒙古临河区巴彦淖尔一中高三上9月月考化学卷2017届河南省开封市高三上学期10月定位考试化学试卷2017届河南省郑州一中高三上期中化学试卷2017届辽宁省六校协作体高三上学期期中化学试卷内蒙古集宁一中(东校区)2016-2017学年高二下学期期末考试化学试题江苏省溧水高级中学2018届高三上学期期初模拟考试化学试题广东省汕头市潮南实验学校2018届高三上学期入学摸底考试化学试题湖南省长郡中学2017-2018学年高二上学期第一次模块检测化学试题1贵州省遵义航天高级中学2018届高三第二次模拟(10月)理科综合化学试题云南省腾冲市第八中学2017-2018学年高一下学期第一次月考化学试题江苏省常州市田家炳高级中学2019届高三上学期10月月考化学试题四川省成都市七中实验学校2019届高三上学期10月月考化学试题(已下线)解密17 物质的检验分离与提纯(教师版)——备战2018年高考化学之高频考点解密2016年全国普通高等学校招生统一考试化学(上海卷参考版)2019年秋高三化学复习强化练习—— 硫及其化合物人教版(2019)必修第二册第五章 模拟高考高一必修第一册(鲁科2019)考试帮 3 核心素养解读必修第二册RJ第5章挑战区 模拟高考(已下线)易错20 表格类化学实验选择题-备战2021年高考化学一轮复习易错题四川省峨眉第二中学校2021-2022学年高一下学期3月月考化学试题上海市川沙中学2021-2022学年高三下学期5月月考化学试题陕西省黄陵中学2021-2022学年高一上学期期末考试化学试题上海市嘉定区2023届高三一模化学试题北京市清华大学附属中学2023-2024学年高三上学期开学考试化学(B)试题陕西省安康中学2023-2024学年高一下学期3月月考化学试卷
3 . 某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
已知:氢氧化钠溶液不与NO反应,能与NO2反应,2NO2+2NaOH=NaNO3+NaNO2+H2O。
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是________
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后________
(3)装置①中发生反应的化学方程式是_________
(4)装置②的作用是________ ,发生反应的化学方程式是__________
(5)该小组得出的结论依据的实验现象是___________
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)( )
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化

已知:氢氧化钠溶液不与NO反应,能与NO2反应,2NO2+2NaOH=NaNO3+NaNO2+H2O。
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
(3)装置①中发生反应的化学方程式是
(4)装置②的作用是
(5)该小组得出的结论依据的实验现象是
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
您最近一年使用:0次
2019-01-30更新
|
3195次组卷
|
22卷引用:2010年天津市天津一中高三第五次月考(理综)化学部分
(已下线)2010年天津市天津一中高三第五次月考(理综)化学部分2009年普通高等学校招生统一考试理综试题化学部分(北京卷)09高考真题汇编—实验设计与评价 综合性实验2009年高考真题汇编-氮族元素(已下线)2010—2011学年浙江省杭州学军中学高一下学期期中考试化学试卷2016届贵州省务川民族中学高三上学期期中考试化学试卷2015-2016学年江苏省盐城市建湖二中高一下学期期中考试化学试卷2017届河北省邯郸市大名一中高三上学期第一次月考化学试卷宁夏青铜峡市高级中学2018届高三上学期期中考试化学试题内蒙古集宁一中2017-2018学年高一下学期第二次月考理科综合化学试题人教版化学必修一.4.4氨 硝酸 硫酸同步测试卷(已下线)【走进新高考】(人教版必修一)4.4.2氨、硝酸、硫酸——硝酸 同步练习02【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题江西省宜春市奉新县第一中学2019-2020学年高一下学期第二次月考化学试题福建省福州市2020届高三模拟考试化学试题专题7 第二单元 第2课时 硝酸-高中化学必修第二册苏教版2019人教版2019必修第二册 第五章 第二节 第3课时 硝酸 酸雨及防治第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系北京市顺义牛栏山第一中学2022-2023学年高一下学期3月月考化学试题(已下线)专题03 硫酸和硝酸专讲(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)浙江省杭州学军中学2023-2024学年高一上学期期末模拟考试化学试卷 (已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
4 . 如图所示为氢气燃烧的实验。发现烧杯中酸性KMnO4溶液褪色,若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈红色。下列说法不正确的是
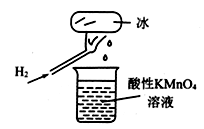

| A.将烧杯中溶液换成氢硫酸溶液,溶液无明显变化 |
| B.与酸性FeSO4溶液发生反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O |
| C.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 |
| D.该条件下H2燃烧的产物中可能含有一定量的H2O2 |
您最近一年使用:0次
2019-01-20更新
|
185次组卷
|
3卷引用:【区级联考】天津市蓟州等部分区2019届高三上学期期末联考化学试题
14-15高三上·北京海淀·期末
5 . 氨气在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式:________ ;
②NH3的稳定性比PH3________ (填“强”或“弱”)。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
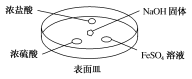
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_________ 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是________ (写化学式,一种即可)。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O===Fe(OH)2↓+2NH 和
和________ 。
(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因:____________________ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为_________________ ,若反应中有0.3 mol电子发生转移时,生成亚硝酸的质量为________ g(小数点后保留两位有效数字)。
(1)①氮气用于工业合成氨,写出氮气的电子式:
②NH3的稳定性比PH3
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O===Fe(OH)2↓+2NH
 和
和(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因:
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近一年使用:0次
6 . 某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验。
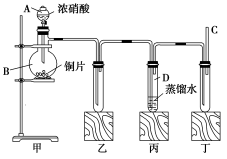
回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是_____ ,该装置中发生反应的化学方程式为___ 。
(2)实验过程中,装置乙、丙中出现的现象分别是__________ 、____________ ;装置丙中的试管内发生反应的离子方程式为________________ (不是离子反应的不写)。
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________ 色,为了证明铁元素在该反应中的产物,可以再向溶液中滴加KSCN溶液,溶液变为________ 色。

回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是
(2)实验过程中,装置乙、丙中出现的现象分别是
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为
您最近一年使用:0次
2018-09-08更新
|
326次组卷
|
2卷引用:2018-2019学年高中化学鲁科版必修1 章末综合测评3
7 . 某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
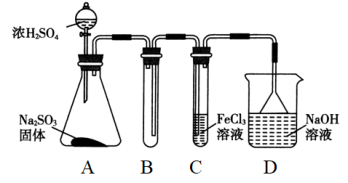
(1)通入足量SO2时C中观察到的现象是______________________ 。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:_______________________ ;
②请设计实验方案检验有Fe2+生成:_________________________ ;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法_____ (填“合理”或“不合理”),理由是______ 。
(3)D装置中倒置漏斗的作用是__________________________ 。
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________ (填字母)。
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液

(1)通入足量SO2时C中观察到的现象是
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:
②请设计实验方案检验有Fe2+生成:
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法
(3)D装置中倒置漏斗的作用是
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
您最近一年使用:0次
2018-09-08更新
|
422次组卷
|
3卷引用:2018-2019学年高中化学鲁科版必修1 模块综合测评
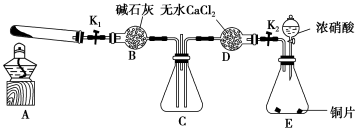
8 . 某化学课外活动小组通过实验探究NO2的性质。已知:2NO2+2NaOH===NaNO3+NaNO2+H2O。
任务1:利用如图所示装置探究NO2能否被NH3还原(夹持固定装置已略去)。
请回答下列问题:
(1)E装置中制取NO2的化学方程式是_____________________________ 。
(2)若NO2能被NH3还原,预期观察到C装置中的现象是________________ 。
(3)此实验装置存在的一个明显缺陷是_______________________________________ 。
任务2:探究NO2能否与Na2O2发生氧化还原反应。
(4)实验前,该小组同学提出三种假设。
假设1:二者不反应;
假设2:NO2能被Na2O2氧化;
假设3:________________________________________________ 。
(5)为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如图所示),重新组装,进行实验。
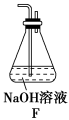
①装置的合理连接顺序是(某些装置可以重复使用)_________________ 。
②实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中发生反应的化学方程式为______________________ 。
任务1:利用如图所示装置探究NO2能否被NH3还原(夹持固定装置已略去)。

请回答下列问题:
(1)E装置中制取NO2的化学方程式是
(2)若NO2能被NH3还原,预期观察到C装置中的现象是
(3)此实验装置存在的一个明显缺陷是
任务2:探究NO2能否与Na2O2发生氧化还原反应。
(4)实验前,该小组同学提出三种假设。
假设1:二者不反应;
假设2:NO2能被Na2O2氧化;
假设3:
(5)为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如图所示),重新组装,进行实验。

①装置的合理连接顺序是(某些装置可以重复使用)
②实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中发生反应的化学方程式为
您最近一年使用:0次
2018-09-05更新
|
738次组卷
|
6卷引用:2018-2019学年高中化学鲁科版必修1 模块综合测评
2018-2019学年高中化学鲁科版必修1 模块综合测评2018-2019学年人教版高中化学必修一:非金属及其化合物章末综合测评(四)(已下线)2019年1月9日 《每日一题》人教必修1-二氧化氮和一氧化氮的性质辽宁省铁岭市调兵山市第一高级中学2019-2020学年高一下学期第一次月考化学试题甘肃省静宁县第一中学2019-2020学年高一下学期期中考试(第二次月考)化学试题(已下线)2020年1月1日《每日一题》人教版(必修1)—— 二氧化氮和一氧化氮的性质
名校
解题方法
9 . 下列有关研究物质性质的方法和程序的说法,正确的是( )
| A.探究金属钠的性质只需应用实验法即可 |
| B.研究未知物质的性质可按照观察→实验→预测→结论的顺序进行 |
| C.科学家提出的假说一定能成为科学理论 |
| D.使用模型有助于人们研究物质的性质 |
您最近一年使用:0次
2018-09-04更新
|
417次组卷
|
9卷引用:2018-2019学年高中化学鲁科版必修1章末综合测评题(一)
2018-2019学年高中化学鲁科版必修1章末综合测评题(一)【全国百强校】山东省新泰市新泰一中2018-2019学年高一上学期第一次质量检测化学试题福建省三明市尤溪第一中学2019-2020学年高一上学期第一次月考化学试题福建省厦门市双十中学2020-2021学年高一上学期第一次月考化学试题福建省厦门外国语学校2019-2020学年高一上学期第一次月考(10月)化学试题山东省济南市2020-2021学年高一上学期10月月考化学试题山东省菏泽市单县第五中学希望部2021-2022学年高一上学期第一次月考化学试题山东省菏泽市单县第五中学2021-2022学年高一上学期第一次月考化学试题福建省南平市浦城县2022-2023学年高一上学期11月期中化学试题
名校
10 . 用如下图所示的装置进行实验(夹持仪器略去,必要时可加热),其中a、b、c中分别盛有试剂1、2、3,能达到相应实验目的的是
| 选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
| A | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 除去Cl2中的HCl | 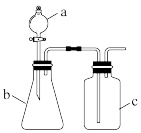 |
| B | 浓HNO3 | Cu片 | KI—淀粉溶液 | 验证NO2的氧化性 | |
| C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证X中是否有 | |
| D | 70%硫酸 | Na2SO3 | 酸性KMnO4溶液 | 验证SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-07-09更新
|
549次组卷
|
2卷引用:天津市第一中学2021届高三上学期摸底考(零月考)化学试题



