1 . 某小组探究Na2SO3溶液和KIO3溶液的反应。
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O
(1)溶液变蓝,说明Na2SO3具有_________ 性。
(2)针对t秒前溶液未变蓝,小组做出如下假设:
i.t秒前未生成I2,是由于反应的活化能______ (填“大”或“小”),反应速率慢导致的。
ii.t秒前生成了I2,但由于存在Na2SO3,_____ (用离子方程式表示),I2被消耗。
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入_______ ,蓝色迅速消失,后再次变蓝。
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:
① K闭合后,取b极区溶液加入盐酸酸化的BaCl2溶液,现象是______ 。
② 0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断IO3-在a极放电的产物是_______ 。
③ 结合反应解释t2~t3时指针回到“0”处的原因:________ 。
(5)综合实验I、II、III,下列说法正确的是_______ 。
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化
B.对比实验I、III,t秒前IO3- 未发生反应
C.实验III中指针返回X处的原因,可能是I2氧化SO32-
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O
(1)溶液变蓝,说明Na2SO3具有
(2)针对t秒前溶液未变蓝,小组做出如下假设:
i.t秒前未生成I2,是由于反应的活化能
ii.t秒前生成了I2,但由于存在Na2SO3,
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:
| 表盘 |  | 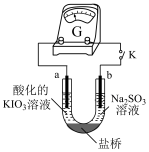 | ||
| 时间/min | 0~t1 | t2~t3 | t4 | |
| 偏转 位置 | 右偏至Y | 指针回到“0”处,又返至“X”处;如此周期性往复多次…… | 指针 归零 | |
② 0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断IO3-在a极放电的产物是
③ 结合反应解释t2~t3时指针回到“0”处的原因:
(5)综合实验I、II、III,下列说法正确的是
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化
B.对比实验I、III,t秒前IO3- 未发生反应
C.实验III中指针返回X处的原因,可能是I2氧化SO32-
您最近一年使用:0次
2019-04-04更新
|
2445次组卷
|
8卷引用:江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(A)
江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(A)北京市海淀区北京大学附中2020 届高三化学阶段性测试化学试题 北京市回民学校2023-2024学年高三上学期统练二化学试题【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题专题3.2 非金属及其化合物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)《2020年新高考政策解读与配套资源》模拟试题07-2020年北京新高考化学模拟试题(已下线)第10讲 氯及其化合物-2021年高考化学一轮复习名师精讲练2021年北京高考化学试题变式题11-19
2 . 某实验小组的同学为了探究CuSO4溶液与Na2CO3溶液的反应原理并验证产物,进行如下实验。
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
(2)为进一步确定蓝绿色固体的组成,使用如下装置再进行定量实验。

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是________________ ,装置E的作用是____________________ ,反应结束时要通入适量的空气,其作用是____________________________________ 。
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为____________ 。
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式______________ 。
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是_________________________ 。
(5)有同学为了降低实验误差,提出如下建议,其中合理的是______ (填字母序号)。
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| 实验Ⅱ | 取适量蓝绿色固体,加入足量稀硫酸 | 固体溶解,生成蓝色溶液, | 蓝绿色固体中含有CO32- |

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是
(5)有同学为了降低实验误差,提出如下建议,其中合理的是
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
您最近一年使用:0次



