1 . 两个原来处于热平衡状态的系统分开后,由于外界的影响,其中一个系统的温度升高了5K,另一个系统温度升高了5℃,则下列说法不正确的是( )
| A.两个系统不再是热平衡系统了 | B.两个系统仍处于热平衡 |
| C.两个系统的状态都发生了变化 | D.两个系统的状态没有变化 |
您最近一年使用:0次
2022-06-27更新
|
1115次组卷
|
5卷引用:2021新教材版选择性必修第三册 第二章 第1节 温度和温标 基础练习
2021新教材版选择性必修第三册 第二章 第1节 温度和温标 基础练习(已下线)2.1.温度和温标 课后练(已下线)第二章 气体、固体和液体 讲和练2.1.温度和温标-随堂练习山东省微山县第二中学2017-2018学年高二下学期第二学段考试物理试题
名校
2 . 下列说法不正确的是( )
| A.空调既能制热又能制冷,说明热传递不存在方向性 |
| B.第一类永动机不可能制成是因为它违背了能量守恒定律 |
| C.对于一定质量的理想气体,只要温度升高其内能就一定增大 |
| D.用温度计测量温度是根据热平衡的原理 |
您最近一年使用:0次
2021-11-11更新
|
292次组卷
|
4卷引用:上海市交通大学附属中学2021-2022学年高二上学期期中物理试题
3 . 下列说法正确的是( )
| A.空调既能制热又能制冷,说明热传递不存在方向性 |
| B.第一类永动机不可能制成是因为它违背了能量守恒定律 |
| C.对于一定质量的理想气体,只要温度升高其内能就一定增大 |
| D.用温度计测量温度是根据热平衡的原理 |
您最近一年使用:0次
2021-09-27更新
|
118次组卷
|
2卷引用:人教版(2019)选择性必修第三册 第三章 C 高考挑战区(8页)
4 . 下列说法正确的是( )
| A.温度计测温原理就是热平衡定律 |
| B.温度计与被测系统的温度不相同时,读不出示数 |
| C.温度计读出的示数是它自身这个系统的温度,若它与被测系统热平衡,这一示数也是被测系统的温度 |
| D.温度计读出的示数总是被测系统的温度,无论是否达到热平衡 |
您最近一年使用:0次
2021-09-26更新
|
121次组卷
|
2卷引用:人教版(2019)选择性必修第三册 第二章 课时1 温度和温标
5 . 下列关于热平衡定律的理解,说法正确的是( )
| A.两系统的温度相同时,才能达到热平衡 |
| B.A、B两系统分别与C系统达到热平衡,则A、B两系统也达到热平衡 |
| C.甲、乙、丙物体温度不相等,先把甲、乙接触,最终达到热平衡,再将丙与乙接触最终也达到热平衡,则甲、丙是处于热平衡的 |
| D.热平衡时,两系统的温度相同,压强、体积也一定相同 |
| E.温度是决定两个系统是否达到热平衡状态的唯一物理量 |
您最近一年使用:0次
6 . 下列说法正确的是( )
| A.根据热力学第二定律可知,热量不可能从低温物体传递到高温物体 |
| B.第二类永动机不可能制成,说明内能不能全部转化为机械能,又不引起其他变化 |
| C.当分子间的距离增大时,分子间的引力增大、斥力减小 |
| D.温度是描述热运动的物理量,一个系统与另一个系统达到热平衡时,两系统温度相同 |
您最近一年使用:0次
7 . 如图所示,绝热汽缸中间用固定栓将可无摩擦移动的导热隔板固定,隔板质量不计,左、右两室分别充有一定量的氢气和氧气(均视为理想气体)。初始时,两室气体的温度相等,氢气的压强大于氧气的压强,松开固定栓直至系统重新达到平衡,下列说法正确的是( )


| A.初始时氢分子的平均动能大于氧分子的平均动能 |
| B.系统重新达到平衡时,氢气的内能比初始时的小 |
| C.系统重新达到平衡时,两者温度相同,等于初始值 |
| D.松开固定栓直至系统重新达到平衡的过程中有热量从氧气传递到氢气 |
| E.松开固定栓直至系统重新达到平衡的过程中,氧气的内能先增加后减少 |
您最近一年使用:0次
2021-09-24更新
|
373次组卷
|
4卷引用:2022年新教材高考一轮创新复习 选修3-3 第3讲 热力学定律与能量守恒 课时作业
2022年新教材高考一轮创新复习 选修3-3 第3讲 热力学定律与能量守恒 课时作业2022年新教材高考一轮创新复习 第十二章第2讲 气体、固体与液体 课时作业2023红对勾 一轮复习 第十三单元 课时作业56 热力学定律与能量守恒定律(已下线)2.1温度和温标-2022-2023高二物理课后培优分级练(人教版 2019选择性必修第三册)
8 . 下列关于热力学定律的理解正确的是( )
| A.热量不可能从低温物体传到高温物体 |
| B.如果两个系统分别与状态确定的第三个系统达到热平衡,那么这两个系统彼此之间也必定处于热平衡 |
C.物体的摄氏温度变化了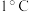 ,其热力学温度变化了1 K ,其热力学温度变化了1 K |
| D.空调机作为制冷机使用时,将热量从温度较低的室内送到温度较高的室外,所以制冷机的工作不遵守热力学第二定律 |
| E.一辆空载的卡车停于水平地面,在缓慢装沙的过程中,若车胎不漏气,胎内气体温度不变,不计分子间势能,则胎内气体向外界放热 |
您最近一年使用:0次
2021-09-22更新
|
186次组卷
|
2卷引用:2022年新教材高考一轮创新复习 选修3-3 第3讲 热力学定律与能量守恒
名校
9 . 下列说法正确的是( )
| A.如果两个系统处于热平衡状态,则它们的温度一定相同 |
| B.压缩气体时气体会表现出抗拒压缩的力是由于气体压强变大的原因 |
| C.当温度一定时,花粉颗粒越小,布朗运动进行得越激烈 |
| D.液体表面张力是由液体表面层分子间的作用力产生的,其力方向与液面垂直 |
| E.当水面上方的水蒸气达到饱和状态时,液态水分子已不再转化为气态水分子 |
您最近一年使用:0次
2021-09-05更新
|
354次组卷
|
6卷引用:2022届百师联盟高三上学期开学联考物理试题
10 . 关于平衡态和热平衡,下列说法正确的是( )
| A.热平衡就是平衡态 |
| B.只要系统的温度不变且处处相等,系统就处于平衡态 |
| C.处于热平衡的两个系统内能一定相同 |
| D.处于热平衡的两个系统温度一定相同 |
您最近一年使用:0次



