19. 《天工开物》中记载了一种“绿青”的宝石,是孔雀石的一种,其主要成分为碱式碳酸铜【Cu
2(OH)
2CO
3】。在现代生产中被用于制造油漆、颜料等。某兴趣小组欲在实验室中制备碱式碳酸铜。
活动一:探究制备碱式碳酸铜的条件。
【查阅资料】碱式碳酸铜是翠绿色、难溶于水的固体,酸性条件下不稳定。
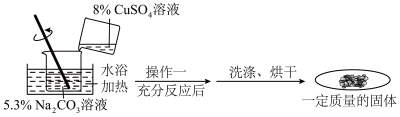
【进行实验】按下表中的数据进行图示实验,记录实验结果。
(1)操作一为:
______。
序号 | CuSO4溶液体积/mL | Na2CO3溶液体积/mL | 水浴温度/℃ | 固体颜色 |
I | 50 | 60 | 60 | 蓝绿 |
II | 50 | 60 | 70 | 翠绿 |
Ⅲ | 50 | 60 | 80 | 暗绿 |
IV | 50 | 70 | 70 | 蓝绿 |
V | 50 | 50 | x | 蓝绿 |
【解释与结论】
(2)为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH
______7;
(3)分析步骤Ⅱ、IV、V的数据可知CuSO
4溶液与Na
2CO
3溶液最佳配比,则x为
______;
(4)分析步骤I、Ⅱ、Ⅲ的数据,实验的最佳温度为
______℃;
活动二:探究步骤Ⅲ中所得固体颜色偏暗的原因。
【查阅资料】碱式碳酸铜受热分解会生成的CuO为黑色。
【猜想与假设】固体颜色偏暗是因为实验过程中生成了CuO。
【进行实验】
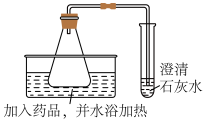
(5)如图所示,锥形瓶中加入的药品为50 mL CuSO
4溶液和Na
2CO
3溶液,水浴温度为
______,观察到固体变为暗绿色,澄清的石灰水变浑浊。
(6)【结论】碱式碳酸铜反应的方程式:
 ______
______。