19. 某化学兴趣小组用实验室的稀盐酸。稀硫酸和一些药品做如下实验。
【实验一】将氯化钠溶液加入稀硫酸中加热一段时间后,闻到制激性气味。小组同学猜想刺激性气体可能是二氧化硫、氯化氢或氨气中的一种。
(1)甲同学认为刺激性气味气体是氨气。大家讨论后认为氨气不合理,依据是
_______。
(2)SO
2和CO
2的化学性质相似,都能使澄清石灰水变浑浊。用化学方程式表示二氧化硫使澄清石灰水变浑浊的原因(一种生成物是CaSO
3)
________。
(3)乙同学将产生的气体通入紫色石蕊溶液中,观察到
_______,认为该气体是氯化氢。
(4)丙同学认为乙同学的结论不科学,他做了如图所示实验,小试管中盛放的液体是
_______,观察到
________,排除了二氧化硫的可能性,说明该气体是氯化氢。
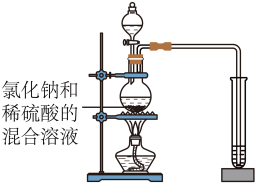
【实验二】兴趣小组同学发现向试管中(含生锈铁钉)加入过量溶质质量分数为10%稀盐酸浸泡。观察到铁锈逐渐消失,铁钉表面有气泡产生,溶液呈黄色,一段时间后黄色变为浅绿色。
(5)写出铁锈(Fe
2O
3)溶于盐酸的化学方程式:
_______。
(6)推测试管中溶液由黄色变为浅绿色,可能是因为氯化铁与某些物质发生反应所致。现进行如表3个实验(持续10小时,已知氢气不影响该反应)
| 序号 | 实验I | 实验Ⅱ | 实验Ⅲ |
| 实验内容 | 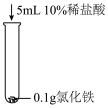 | 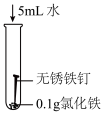 | 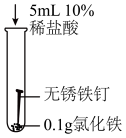 |
| 现象 | 溶液颜色始终呈黄色 | 产生红褐色沉淀 | 溶液逐渐由黄色变浅绿色 |
①设计实验I的目的是
_______。
②综合分析上述3个实验,实验Ⅲ试管中溶液由黄色变为浅绿色的原因是:在酸性条件下,
______。