安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
安徽
高一
阶段练习
2021-10-07
256次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、化学反应原理、化学与STSE
安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
安徽
高一
阶段练习
2021-10-07
256次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、化学反应原理、化学与STSE
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 下列说法正确的是
| A.有色玻璃是某些胶态金属氧化物分散于玻璃中制成的,它是一种晶体 |
| B.氯水在常温下能导电,所以氯水是一种电解质 |
| C.KH和H2O反应生成H2和KOH,反应中1mol KH失去1mol电子 |
| D.过滤时,漏斗里液体的液面要高于滤纸的边缘 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
您最近一年使用:0次
2021-08-12更新
|
334次组卷
|
4卷引用:云南省丽江市2020-2021学年高一下学期期末教学质量监测理科化学试题
单选题
|
适中(0.65)
3. 下列叙述正确的是
| A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 |
| B.Na2O2与水反应、红热的Fe与水蒸气反应均生成碱 |
| C.Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物 |
| D.CO2、HCl、NH3的水溶液都能导电,它们均属于电解质 |
您最近一年使用:0次
2016-12-09更新
|
522次组卷
|
3卷引用:2015届江苏连云港市东海县第二中学高三上第一次月考化学试卷
(已下线)2015届江苏连云港市东海县第二中学高三上第一次月考化学试卷广西钦州市钦州港经济技术开发区中学2018届高三上学期开学考试化学试题安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 铁粉与水蒸气反应的装置如图所示,下列说法错误的是
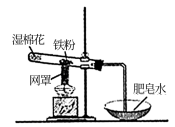

| A.铁与水蒸气的反应属于氧化还原反应 |
| B.铁与水蒸气反应能生成红色的Fe2O3 |
| C.该实验中网罩的作用是集中火焰,提高温度 |
| D.常温下,Fe能与空气中的O2和H2O发生反应 |
您最近一年使用:0次
2021-02-08更新
|
335次组卷
|
5卷引用:重庆八中2020-2021学年高一上学期期末考试化学试题
重庆八中2020-2021学年高一上学期期末考试化学试题(已下线)《新教材变化解读及考法剖析 》(人教版2019必修第一册)第三章安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题重庆市巫山县官渡中学2021-2022学年高一上学期期末考试化学试题四川省广元市宝轮中学2022-2023学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
名校
5. 下列说法错误的一组是
①不溶于水的BaSO4 是强电解质 ②可溶于水的酸都是强电解质 ③0.5mol/L的所有一元酸中氢离子浓度都是0.5mol/L ④熔融态的电解质都能导电。
①不溶于水的BaSO4 是强电解质 ②可溶于水的酸都是强电解质 ③0.5mol/L的所有一元酸中氢离子浓度都是0.5mol/L ④熔融态的电解质都能导电。
| A.①③④ | B.②③④ | C.①④ | D.①②③ |
您最近一年使用:0次
2016-12-09更新
|
914次组卷
|
7卷引用:2010年重庆市西南师大附中高一上学期期中考试化学试卷
(已下线)2010年重庆市西南师大附中高一上学期期中考试化学试卷重庆市巴蜀中学2017-2018学年高一上学期期中考试化学试题河北省巨鹿县二中2017-2018学年高二下学期期末考试化学试题(已下线)【走进新高考】(人教版必修一)高一上学期期中复习模拟(A卷)(基础篇)01河南省信阳市罗山高级中学2018-2019学年高一上期期中考试化学试题安徽省黄山市祁门县第一中学2019-2020学年高一下学期期中考试化学试题安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
单选题
|
较易(0.85)
6. 对于反应MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑,下列说法错误的是
MnCl2+2H2O+Cl2↑,下列说法错误的是
 MnCl2+2H2O+Cl2↑,下列说法错误的是
MnCl2+2H2O+Cl2↑,下列说法错误的是| A.该反应是氧化还原反应 |
| B.MnO2发生还原反应 |
| C.HCl是还原剂 |
| D.若生成7.1g Cl2,则转移0.1mol电子 |
【知识点】 氧化还原反应的几组概念解读 与氧化剂、还原剂有关的计算解读
您最近一年使用:0次
2021-10-06更新
|
100次组卷
|
2卷引用:安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 把 溶液滴入明矾溶液中,使
溶液滴入明矾溶液中,使 全部转化成
全部转化成 沉淀,此时铝元素的主要存在形式是
沉淀,此时铝元素的主要存在形式是
 溶液滴入明矾溶液中,使
溶液滴入明矾溶液中,使 全部转化成
全部转化成 沉淀,此时铝元素的主要存在形式是
沉淀,此时铝元素的主要存在形式是A. | B. | C. | D. 和 和 |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 氢氧化铝
您最近一年使用:0次
2021-11-08更新
|
783次组卷
|
57卷引用:新课标2010-2011学年度上学期高三一轮复习单元测试3(新人教)
(已下线)新课标2010-2011学年度上学期高三一轮复习单元测试3(新人教)(已下线)2011届福建省福州市八县(市)高三上学期期中联考化学卷(已下线)2011-2012年度上海市吴淞中学高二第一学期期末考试化学试卷(已下线)2012-2013学年甘肃省兰州一中高一上学期期末考试化学试卷(已下线)2012-2013学年北京市东城区(南片)高一上学期期末考试化学试卷(已下线)2013-2014学年吉林省长春外国语学校高一上学期期末理科化学试卷(已下线)2014吉林省长春外国语学校高一上学期期末化学(理)试卷 2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2014-2015陕西省西安市一中高一上学期期末化学试卷2015-2016学年河北冀州市中学高一上第四次月考化学试卷2015-2016学年甘肃省会宁一中高一上期末考试化学试卷2015-2016学年浙江省乐清一中高一上学期12月月考化学试卷2015-2016学年安徽省六安一中高一下开学考试化学试卷2015-2016学年陕西省西北农林科大附中高一上第二次月考化学试卷2015-2016学年浙江省温州市瑞安市龙翔中学高二上第三次月考化学卷2017届陕西省黄陵中学高新部高三上学期一轮复习第一次测试化学试卷2017届福建省莆田二十五中高三上第二次月考化学试卷黑龙江省哈尔滨市第六中学2016-2017学年高二6月月考化学试题山东省临沂市2016-2017学年高一下学期期末考试化学试题山西省忻州市第一中学2016-2017学年高一必修一:3.2.2几种重要的金属化合物同步练习化学试题2017-2018学年高一人教版必修一:16 铝的重要化合物课时训练化学试题黑龙江省牡丹江市第一高级中学2017-2018学年高一上学期期中考试化学试题河北省邢台市第一中学2017-2018学年高一上学期第三次月考化学试题河北省衡水市安平中学2017-2018学年高一上学期第三次月考化学试题2宁夏育才中学勤行校区2017-2018学年高一12月月考化学试题山西省太原市第五中学2017-2018学年高一12月月考化学试题高中化学人教版 必修1 第三章 金属及其化合物 2.几种重要的金属化合物 铝的重要化合物湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高一上学期第二次月考化学试题江西省南康中学2018-2019学年高一上学期第三次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期期末考试化学试题上海市复旦大学附中2015-2016学年高二(上)期末化学试题上海市向明中学2018-2019学年高二第一学期期末考试化学试题山西省应县第一中学校2019-2020学年高一上学期第四次月考化学试题四川省三台县芦溪中学2017—2018学年高一上学期第三次月考化学试题四川省绵阳市三台县芦溪中学2017-2018学年高一上学期第三次月考化学试题福建省泉州第五中学高中化学必修1【专题练习】金属单质及其化合物江西省南康中学2019-2020学年高一上学期12月月考化学试题(已下线)【新东方】2020-14陕西省咸阳市实验中学2019-2020学年高一上学期第三次月考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题宁夏石嘴山市平罗中学2020-2021学年高一上学期第三次月考化学试题上海市浦东新区2019-2020学年高二上学期期末考试化学试题江西省吉安市2020-2021学年高一上学期期末教学质量检测化学试题新疆哈密市第八中学2020-2021学年高一上学期期末考试化学试题湖南常德市第一中学2020-2021学年高一上学期期末考试化学试题湖南省娄底市第一中学2020-2021学年高一下学期期中考试化学(高考班)试题四川省成都市实验外国语学校(西区)2019-2020学年高一上学期11月月考化学试题(已下线)课时16 铝及其化合物-2022年高考化学一轮复习小题多维练(全国通用)安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题上海市向明中学2021-2022学年高二上学期期中考试化学试题上海市向明中学2021-2022学年高三上学期期中考试化学试题(已下线)专题七 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)陕西省西安市长安区第一中学2021-2022学年高一上学期第二次月考化学试题黑龙江省绥化市第一中学2020-2021学年高一上学期期末考试化学试题江苏省宿迁市沭阳县潼阳中学2022-2023学年高三上学期第一次月考化学试题江西省安福县第三中学2021届高三下学期期中考试化学试题
单选题
|
较易(0.85)
解题方法
8. 有关下列三个化学反应的叙述,氧化产物和还原产物物质的量之比为2:1的是
①2H2S+SO2=3S↓+2H2O
②S+2H2SO4(浓)=3SO2↑+2H2O
③3S+6KOH=2K2S+K2SO3+3H2O。
①2H2S+SO2=3S↓+2H2O
②S+2H2SO4(浓)=3SO2↑+2H2O
③3S+6KOH=2K2S+K2SO3+3H2O。
| A.① | B.①② | C.②③ | D.①②③ |
【知识点】 氧化还原反应的几组概念解读 与氧化剂、还原剂有关的计算解读
您最近一年使用:0次
单选题
|
适中(0.65)
9. 下列说法正确的是
| A.加入BaCl2溶液,沉淀不溶于盐酸,证明原溶液含有SO42- |
| B..Na2O、Na2O2与CO2反应产物相同 |
| C.小苏打用于治疗胃溃疡病人的胃酸过多症 |
| D.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
您最近一年使用:0次
2018-09-22更新
|
83次组卷
|
2卷引用:黑龙江省黑河市逊克县第一中学2019届高三上学期学期初考试化学试题
单选题
|
较易(0.85)
10. 2HCHO+NaOH(浓)=CH3OH+HCOONa,该反应中甲醛发生的反应类型是
| A.仅被氧化 | B.仅被还原 |
| C.既被氧化又被还原 | D.复分解反应 |
【知识点】 氧化还原反应基本概念 氧化还原反应的几组概念解读
您最近一年使用:0次
单选题
|
较易(0.85)
名校
11. 下列各组离子在溶液中能大量共存的是
A.Ca2+、Na+、CO 、NO 、NO | B.Na+、Cl-、H+、OH- |
C.Na+、Al3+、Cl-、SO | D.H+、K+、CO 、SO 、SO |
【知识点】 离子反应的发生条件解读 无附加条件的离子共存解读
您最近一年使用:0次
2021-10-06更新
|
272次组卷
|
4卷引用:安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
单选题
|
较易(0.85)
名校
解题方法
12. 下列说法合理的是
| A.碳酸钠可称为碳酸盐、钠盐或者碱式盐 |
| B.鸡蛋清、浑浊的河水不可能属于同一类别 |
C.强光通过 胶体发生了显著的化学变化 胶体发生了显著的化学变化 |
D.直径为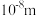 的粒子不一定是胶体 的粒子不一定是胶体 |
您最近一年使用:0次
2021-10-06更新
|
233次组卷
|
5卷引用:安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
单选题
|
较易(0.85)
名校
解题方法
13. 下列关于碘水中萃取碘的实验的说法不正确的是
| A.使用分液漏斗前,要检验它是否漏水 |
| B.振荡分液漏斗的过程中要适时打开活塞进行“放气” |
C.用 作萃取剂,萃取后液体分层且下层无色 作萃取剂,萃取后液体分层且下层无色 |
| D.分液时,旋开旋塞,使下层液体流出,上层液体从上口倒出 |
您最近一年使用:0次
2021-10-06更新
|
147次组卷
|
2卷引用:安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
单选题
|
适中(0.65)
14. 如果按照某种标准能将FeSO4、Na2SO3、NO2划归为同一类物质,则下列物质中也能划归为此类物质的是
| A.KMnO4 | B.Al2(SO4)3 | C.KClO3 | D.K2HPO4 |
您最近一年使用:0次
2019-01-30更新
|
75次组卷
|
2卷引用:2014-2015学年福建省清流一中高一上学期第二次阶段测试化学试卷
单选题
|
较难(0.4)
解题方法
15. 能正确表示下列反应的离子方程式是
A. 溶于足量稀 溶于足量稀 |
B.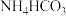 溶液与足量 溶液与足量 溶液混合: 溶液混合: |
C.向澄清石灰水中通入少量 |
D.向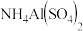 溶液中加入 溶液中加入 溶液至 溶液至 恰好完全沉淀: 恰好完全沉淀: |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
2021-10-06更新
|
767次组卷
|
3卷引用:【校级联考】江西省吉安市西路片七校2018届高三上学期第一次联考化学试题
单选题
|
适中(0.65)
名校
解题方法
16. 下列实验的现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将新制氯水滴到淀粉KI试纸上 | 试纸变蓝色 | 氧化性:I2>Cl2 |
| B | 将过量的CO2通入CaCl2溶液中 | 产生白色沉淀 | 酸性:HCl>H2CO3 |
| C | FeSO4溶液中滴入酸性高锰酸钾溶液 | 紫色褪色 | Fe2+有还原性 |
| D | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-25更新
|
256次组卷
|
4卷引用:广东省珠海市第二中学2021届高三10月月考化学试题
单选题
|
较易(0.85)
名校
17. 下列说法正确的是
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.SO2能使酸性KMnO4溶液褪色,说明SO2具有漂白性 |
| C.将分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
| D.将等物质的量的Cl2和SO2的混合气体作用于潮湿的红布条,红布条立即快速褪色 |
您最近一年使用:0次
2021-10-06更新
|
431次组卷
|
5卷引用:安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题
安徽省滁州市定远县育才学校2020-2021学年高一上学期第一次质检化学试题2021年北京高考化学试题变式题1-10上海市静安区2022届高三适应性练习(二模)化学试题上海市松江一中2021-2022学年高一下学期线上期末诊断测化学试题(已下线)3.1.1 硫和二氧化硫-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
单选题
|
适中(0.65)
解题方法
18. 向一定量的Fe、FeO和 的混合物中加入
的混合物中加入 的稀硝酸,恰好使混合物完全溶解,放出
的稀硝酸,恰好使混合物完全溶解,放出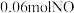 ,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为
,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为
 的混合物中加入
的混合物中加入 的稀硝酸,恰好使混合物完全溶解,放出
的稀硝酸,恰好使混合物完全溶解,放出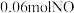 ,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为
,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为A.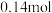 | B. | C.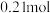 | D. |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
19. 纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图

请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+,Mg2+, 等。粗盐溶解之后,依次加入下列药品:
等。粗盐溶解之后,依次加入下列药品:
足量NaOH溶液____________________________________ 除杂,然后过滤,向滤液中加入适量盐酸得到精制食盐水。
(2)向饱和食盐水中通氨气和二氧化碳反应的方程式为:_________________________ 。
(3)可以区别A固体和Na2CO3固体的方法有________________ 。
A.利用热稳定性不同,加热固体并将生成的气体通入澄清石灰水中,观察是否有浑浊
B.将相同浓度的盐酸逐滴滴入相同浓度的上述固体的溶液中,观察气体产生的速率
C.向相同浓度的两种固体的溶液中滴入酚酞试液,观察溶液颜色的深浅
D.取两种固体配成的溶液,分别加入BaCl2溶液,观察是否有固体生成
E.取两种固体配成的溶液,分别加入Ba(OH)2溶液,观察是否有固体生成
F.取两种固体配成的溶液,分别测量溶液的pH值并比较大小
(4)检验滤液A中含有的阳离子的方法为______________________________ 。

请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+,Mg2+,
 等。粗盐溶解之后,依次加入下列药品:
等。粗盐溶解之后,依次加入下列药品:足量NaOH溶液
(2)向饱和食盐水中通氨气和二氧化碳反应的方程式为:
(3)可以区别A固体和Na2CO3固体的方法有
A.利用热稳定性不同,加热固体并将生成的气体通入澄清石灰水中,观察是否有浑浊
B.将相同浓度的盐酸逐滴滴入相同浓度的上述固体的溶液中,观察气体产生的速率
C.向相同浓度的两种固体的溶液中滴入酚酞试液,观察溶液颜色的深浅
D.取两种固体配成的溶液,分别加入BaCl2溶液,观察是否有固体生成
E.取两种固体配成的溶液,分别加入Ba(OH)2溶液,观察是否有固体生成
F.取两种固体配成的溶液,分别测量溶液的pH值并比较大小
(4)检验滤液A中含有的阳离子的方法为
您最近一年使用:0次
2016-12-09更新
|
236次组卷
|
2卷引用:2015-2016学年山东省临沂十八中高二下学期六月月考化学试卷
解答题-实验探究题
|
适中(0.65)
20. 在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:

(1)上述仪器的正确连接顺序为(填各接口处的字母):___________ 。
(2)装置中饱和食盐水的作是___________ 。
(3)NaOH溶液中发生反应的离子方程式:___________ 。
(4)常用湿润的淀粉碘化钾试纸检验是否有Cl2产生。如果有Cl2产生,可观察到___________ 。

(1)上述仪器的正确连接顺序为(填各接口处的字母):
(2)装置中饱和食盐水的作是
(3)NaOH溶液中发生反应的离子方程式:
(4)常用湿润的淀粉碘化钾试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
您最近一年使用:0次
三、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
21. (1)现有以下物质①熔融状态的NaCl ②NH3·H2O ③Na2O固体 ④铜 ⑤BaSO4固体 ⑥酒精 ⑦液态HCl ⑧KNO3溶液,其中属于电解质的是:___________ ;该状态下能导电的是_____________ ;属于非电解质的是_________________ 。(请用序号作答)
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□ MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内____ ;该反应的还原剂是_________________ ;
②H2O2既体现氧化性,又体现还原性的反应是________ ,H2O2既不作氧化剂又不作还原剂的反应是__________ 。(请用代号作答)
③请用双线桥法表示B反应中电子转移的方向和数目:___________ 。
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□ MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内
②H2O2既体现氧化性,又体现还原性的反应是
③请用双线桥法表示B反应中电子转移的方向和数目:
您最近一年使用:0次
2018-03-09更新
|
316次组卷
|
3卷引用:黑龙江省大庆实验中学2017-2018学年高一上学期期末考试化学试题
四、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
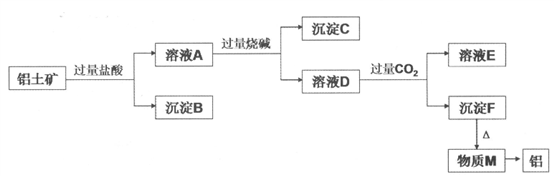
22. 铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:
请回答下列问题:
(1)沉淀B的成分是____________ (填化学式,下同);
(2)沉淀C的成分是__________ ;
(3)沉淀F转化为物质M的化学方程式为__________ ;
(4)由物质M制取铝的化学方程式为____________________ ;
(5)溶液D中通入过量CO2生成沉淀F的离子方程式为____________________ 。
请回答下列问题:
(1)沉淀B的成分是
(2)沉淀C的成分是
(3)沉淀F转化为物质M的化学方程式为
(4)由物质M制取铝的化学方程式为
(5)溶液D中通入过量CO2生成沉淀F的离子方程式为
您最近一年使用:0次
2017-05-26更新
|
385次组卷
|
4卷引用:北京市第四中学2016-2017学年高一上学期期末考试化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、化学实验基础、常见无机物及其应用、化学反应原理、化学与STSE
试卷题型(共 22题)
题型
数量
单选题
18
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 分散系有关的实例 非电解质、电解质物质类别判断 氧化还原反应的几组概念 过滤 | |
| 2 | 0.85 | 氨的碱性 浓硫酸的吸水性 | |
| 3 | 0.65 | 非电解质、电解质物质类别判断 硝酸的强氧化性 铁与水蒸气的反应 | |
| 4 | 0.65 | 铁与水蒸气的反应 | |
| 5 | 0.85 | 电解质的电离 电解质、非电解质概念 强电解质和弱电解质的判断 强电解质与弱电解质 | |
| 6 | 0.85 | 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 | |
| 7 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 氢氧化铝 | |
| 8 | 0.85 | 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 | |
| 9 | 0.65 | 硫酸根离子的检验 碳酸氢钠 铝 | |
| 10 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 | |
| 11 | 0.85 | 离子反应的发生条件 无附加条件的离子共存 | |
| 12 | 0.85 | 分散系有关的实例 胶体的性质和应用 | |
| 13 | 0.85 | 常用仪器及使用 化学实验基础操作 萃取和分液 | |
| 14 | 0.65 | 氧化还原反应的规律 | |
| 15 | 0.4 | 离子方程式的正误判断 | |
| 16 | 0.65 | 氧化性、还原性强弱的比较 氯水的性质 二氧化硫与其他强氧化剂的反应 Fe2+的还原性 | |
| 17 | 0.85 | 氯水的性质 二氧化硫的物理性质 二氧化硫的漂白性 二氧化硫与其他强氧化剂的反应 | |
| 18 | 0.65 | 硝酸的强氧化性 铁与强氧化性酸的反应 几种铁的氧化物的化学性质 铁及铁的氧化物混合物反应的相关计算 | |
| 二、解答题 | |||
| 19 | 0.4 | 碳酸氢钠的不稳定性 物质分离、提纯综合应用 纯碱的生产 | 工业流程题 |
| 20 | 0.65 | 氯气的实验室制法 化学实验探究 | 实验探究题 |
| 22 | 0.65 | 铝盐与强碱溶液反应 铝土矿提取铝的综合考查 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 三、填空题 | |||
| 21 | 0.65 | 电解质与非电解质 单线桥、双线桥分析氧化还原反应 氧化还原反应方程式的配平 | |



