2015-2016学年江苏省扬州市高一下学期期末化学试卷
江苏
高一
期末
2017-07-27
523次
整体难度:
适中
考查范围:
化学反应原理、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.将废电池深埋 |
| B.大量使用化肥 |
| C.开发太阳能、风能和氢能 |
| D.大量开发利用可燃冰 |
A.N2的电子式: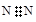 |
B.质子数为53,中子数为78的碘原子: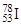 |
C.S2-的结构示意图: |
| D.乙烯的结构简式:CH2=CH2 |
【知识点】 化学用语
3. A、B、C、D 均为气体,对于A+ 3B 2C + D 的反应来说,以下化学反应速率的表示中反应速率最快的是( )
2C + D 的反应来说,以下化学反应速率的表示中反应速率最快的是( )
| A.v(A)=0.4 mol/(L•s) | B.v(B)=0.8mol/(L•s) | C.v(C)=0.6 mol/(L•s) | D.v(D)=0.1mol/(L•s) |
【知识点】 化学反应的速率
| A.HI | B.NaOH | C.Br2 | D.NaCl |
| A.水晶和干冰的熔化 | B.食盐和冰醋酸熔化 |
| C.氯化铵和水的分解 | D.纯碱和烧碱的熔化 |
【知识点】 不同晶体的结构微粒及微粒间作用的区别解读
| A.0.1 mol氮气中所含的氮原子数是0.1 NA |
| B.标准状况下,2.24 L乙醇中所含的分子数是0.1 NA |
| C.1 mol·L-1氨水溶液中含NH4+的数目是NA |
| D.24 g镁和足量的盐酸反应,电子转移的数目是2 NA |
【知识点】 化学计量
| A.碱性:NaOH>Mg(OH)2>Al(OH)3 | B.原子半径:Na<Mg<Al |
| C.金属性:Na<Mg<Al | D.单质的还原性:Al>Mg>Na |
【知识点】 元素周期表 元素周期律

应一定不能发生
| A.生成物比反应物稳定 |
| B.该反应的ΔH<0 |
| C.该图可以表示石灰石高温分解反应 |
| D.因为生成物的总能量高于反应物的总能量,所以该反 |
| A.Na+、Al3+、OH- |
| B.Ba2+、NO3-、SO42- |
| C.K+、Na+、NO3- |
| D.K+、NH4+、OH- |
【知识点】 离子共存
| A.糖类物质中含C、H、O元素,都有甜味 |
| B.油脂是高分子化合物,热值较大 |
| C.在蛋白质溶液中加入CuSO4溶液后有物质析出,加水后该物质溶解 |
| D.向淀粉溶液中加入碘水,溶液变蓝 |
【知识点】 烃的衍生物
| A.氨气极易溶于水,可用作制冷剂 |
| B.乙醇燃烧时放出热量,可用作燃料 |
| C.碳酸氢钠能与盐酸反应,用作治疗胃酸过多 |
| D.葡萄糖能与银氨溶液反应,可用作制镜 |
【知识点】 氮族元素及其化合物
| A.分子式是C6H6 |
| B.所有的原子在同一平面上 |
| C.存在碳碳单键与碳碳双键交替出现的结构 |
| D.能和浓硝酸浓硫酸的混合物在一定条件下发生取代反应 |
【知识点】 烃
 2NH3。下列说法错误的是
2NH3。下列说法错误的是| A.使用合适催化剂可以加快反应速率 |
| B.升高温度可以增大反应速率 |
| C.达到化学平衡时,N2、H2和NH3物质的量浓度一定相等 |
| D.若反应在密闭容器中进行,N2和H2不可能100%转化为NH3 |
【知识点】 催化剂对化学反应速率的影响解读 化学平衡状态的判断方法解读
A.少量碳酸氢铵溶液与足量烧碱溶液混合加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| B.铜片与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| C.氨水与稀醋酸反应:OH-+H+=H2O |
| D.铁片与稀盐酸反应:2Fe+6H+ =2Fe3++3H2↑ |
【知识点】 离子反应的发生及书写
二、多选题 添加题型下试题
| A.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量NaOH溶液,振荡后静置分液 |
| B.除去干燥CO2中混有的少量SO2:将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
| C.探究不同催化剂对H2O2分解速率的影响:在相同条件下,向两支试管均加入2 mL5%H2O2,然后同时分别加入少量MnO2固体粉末和少量FeCl3固体粉末,观察并比较实验现象 |
| D.证明铁的金属性比铜强:常温下,分别向盛有浓硝酸的两支试管中加入铁粉和铜粉,观察并比较产生气体的快慢 |
三、单选题 添加题型下试题
A.图2:收集NO2气体 |
B.图3:验证X溶液为浓硝酸 |
C.图4:验证氨气在水中的溶解性 |
D.图5:用于吸收尾气NH3 |
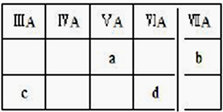
| A.a的氢化物水溶液显酸性 | B.在这4种元素中,b的氢化物热稳定性最好 |
| C.C的氧化物是碱性氧化物 | D.d的氧化物对应水化物一定是强酸 |
【知识点】 元素周期表 元素周期律
| A.凡吸热反应均需在加热条件下才能发生 |
| B.离子化合物中不可能含有共价键 |
C.液氨作为清洁能源的反应原理是4NH3+5O2 4NO+6H2O。 4NO+6H2O。 |
| D.实验收集NO和乙烯常用排水法不能用排空气法 |
【知识点】 反应热
四、多选题 添加题型下试题
 Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
Y(g) ΔH<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
| A.虚线表示使用催化剂的情形 |
| B.b、c两点表明反应在相应条件下达到了最大限度 |
| C.反应进行到a点时放出的热量大于反应进行到b点时放出的热量 |
| D.反应从开始到a点的平均反应速率可表示为v(Y)=0.01mol/(L·min) |
五、解答题 添加题型下试题
回答下列问题:
(1)B在周期表中的位置为
(2)B、C、D原子的半径从大到小的顺序是
(3)设计实验证明E的非金属性比D的非金属性强

回答下列问题:
(1)A的化学式是
(2)反应①的离子方程式是

请回答下列问题:
(1)A的结构简式为
(2)反应⑦中物质X的分子式为
(3)反应⑤的化学方程式为
(4)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为
(5)请补充完整证明反应①是否发生的实验方案:取反应①的溶液2 mL于试管中
(1)甲烷分子的空间构型为
(2)已知25 ℃、101 kPa 时,1 g甲烷完全燃烧生成液态水放出55.64 kJ热量,则该条件下反应CH4(g)+2O2(g)=CO2(g)+2H2O (l)的ΔH=
(3)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是
(4)用甲烷空气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。装置如图所示:
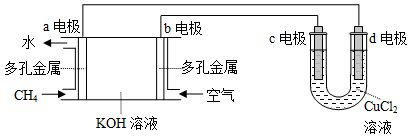
①a电极名称为
②c电极的电极反应式为
③假设CuCl2溶液足量,当某电极上析出3.2 g 金属Cu时,理论上燃料电池消耗的空气在标准状况下的体积是
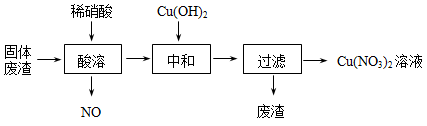
(1)Cu2O与稀硝酸反应的离子方程式为
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)过滤后所得废渣的主要成分的化学式为
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为
【知识点】 铜与强氧化性酸的反应 物质制备的探究解读
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 废弃电池的污染及回收 新能源的开发 化肥与农药的生产与合理使用 | |
| 2 | 0.64 | 化学用语 | |
| 3 | 0.85 | 化学反应的速率 | |
| 4 | 0.65 | 化学键概念理解及判断 离子键概念及判断 共价键与离子键的比较 | |
| 5 | 0.85 | “四同”的相关比较 | |
| 6 | 0.65 | 不同晶体的结构微粒及微粒间作用的区别 | |
| 7 | 0.4 | 化学计量 | |
| 8 | 0.85 | 元素周期表 元素周期律 | |
| 9 | 0.85 | 能量的相互转化 化学键与化学反应中的能量关系 吸热反应和放热反应 | |
| 10 | 0.85 | 离子共存 | |
| 11 | 0.64 | 烃的衍生物 | |
| 12 | 0.64 | 氮族元素及其化合物 | |
| 13 | 0.64 | 烃 | |
| 14 | 0.65 | 催化剂对化学反应速率的影响 化学平衡状态的判断方法 | |
| 15 | 0.64 | 离子反应的发生及书写 | |
| 17 | 0.65 | 氨与氯化氢反应的实验 氨气的实验室制法 二氧化氮与水反应 | |
| 18 | 0.4 | 元素周期表 元素周期律 | |
| 19 | 0.64 | 反应热 | |
| 二、多选题 | |||
| 16 | 0.4 | 综合实验设计与评价 | |
| 20 | 0.4 | 化学反应速率计算 | |
| 三、解答题 | |||
| 21 | 0.4 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 结合物质计算的元素周期律、元素周期表相关推断 | 无机推断题 |
| 22 | 0.4 | 无机综合推断 二氧化氮与水反应 硝酸的强氧化性 | 无机推断题 |
| 23 | 0.65 | 乙酸的酯化反应 有机物的合成 有机物的推断 | 有机推断题 |
| 24 | 0.4 | 盖斯定律与热化学方程式 原电池、电解池综合考查 晶体类型判断 | 原理综合题 |
| 25 | 0.4 | 铜与强氧化性酸的反应 物质制备的探究 | 工业流程题 |



