河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
河北
高三
期末
2024-03-05
84次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、化学实验基础、认识化学科学、物质结构与性质、化学反应原理
河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
河北
高三
期末
2024-03-05
84次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、化学实验基础、认识化学科学、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 化学与社会、生产、生活密切相关,下列说法正确的是
| A.鲜花运输途中需喷洒高锰酸钾稀溶液,主要是为鲜花补充钾肥 |
| B.生活中常利用“84”消毒液和火碱的强氧化性杀菌消毒 |
| C.华为自主研发的“麒麟”芯片与太阳能电池感光板所用主要材料均为晶体硅 |
| D.变质的植物油有难闻的特殊气味,是由于植物油发生了加成反应 |
您最近一年使用:0次
2021-12-04更新
|
221次组卷
|
3卷引用:湖南省190多所名校2021-2022学年高三上学期12月联考化学试题
单选题
|
较易(0.85)
名校
解题方法
2. 兔年春晚《满庭芳·国色》以中国传统色为切入点,使得桃红、凝脂、群青等有着优美名字的“中国色”扑而而来。其中“桃红”可从红花、铅丹、朱砂或赫石等原料中提取。下列说法错误的是
| A.提取红花中的有效成分红花素时,可使用萃取操作 |
B.铅丹 中 中 价 价 与 与 价 价 的个数比为 的个数比为 |
C.以朱砂(主要成分为 )为原料提取的“桃红”不宜用于制作化妆品 )为原料提取的“桃红”不宜用于制作化妆品 |
D.赭石(主要成分为 )可用于制作磁性物质 )可用于制作磁性物质 |
【知识点】 硫化物 几种铁的氧化物的物理性质及用途解读 萃取和分液解读
您最近一年使用:0次
2023-03-09更新
|
1084次组卷
|
8卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题1-5)(已下线)先机卷 06 -【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)专题01 化学与STSE(已下线)T7-化学与STSE江苏省南京市第二十九中学2022-2023学年高一下学期5月月考化学试题福建省福州高级中学2023-2024学年高三第二次阶段考试化学试题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
较易(0.85)
名校
3. 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.25℃时,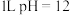 的 的 溶液中含有 溶液中含有 的数目为 的数目为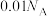 |
B. 白磷 白磷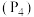 和 和 硅晶体中含有共价键的数目均为 硅晶体中含有共价键的数目均为 |
C.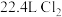 (标准状况)通入水中充分反应,转移电子的数目为 (标准状况)通入水中充分反应,转移电子的数目为 |
D.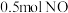 和 和 混合后的分子数目为 混合后的分子数目为 |
您最近一年使用:0次
2023-03-09更新
|
596次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题1-5)(已下线)专题03 阿伏伽德罗常数的应用河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 下列离子方程式书写正确的是
A.Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O +6H+=2S↓+3H2O +6H+=2S↓+3H2O |
B.Fe与稀硝酸反应,当n(Fe):n(HNO3)=1:2时,3Fe+2 +8H+=3Fe2++2NO↑+4H2O +8H+=3Fe2++2NO↑+4H2O |
C.向饱和Na2CO3溶液中通入过量CO2, +CO2+H2O=2 +CO2+H2O=2 |
D.AgNO3溶液与过量浓氨水反应的离子方程式:Ag++NH3•H2O=AgOH↓+ |
您最近一年使用:0次
2021-09-03更新
|
188次组卷
|
2卷引用:天津市塘沽一中2022届高三上学期毕业班开学调研考试化学试题
单选题
|
较易(0.85)
名校
解题方法
5. 下列说法错误的是
A.基态铬原子的电子排布式为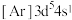 |
B. 晶体中存在配位键 晶体中存在配位键 |
| C.所有元素中,氟的第一电离能最大 |
D.光气 分子中,所有原子均满足8电子稳定结构 分子中,所有原子均满足8电子稳定结构 |
您最近一年使用:0次
2023-03-09更新
|
446次组卷
|
5卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题1-5)(已下线)专题02 化学用语新疆乌鲁木齐市第八中学2022-2023学年高二下学期期中考试化学试题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
6. 下列选项中,陈述Ⅰ、Ⅱ的化学原理相同的是
| 陈述Ⅰ | 陈述Ⅱ | |
| A | 不能用浓硫酸干燥NH3 | 不能用浓硫酸干燥H2S |
| B | 高温时用Na与TiCl4反应制Ti | 高温时用Na与KCl反应制K |
| C | 用FeS处理含Cu2+的废水 | 用含氟牙膏预防龋齿 |
| D | 向NaHCO3溶液中滴加AlCl3溶液,产生白色沉淀 | 向NaHCO3溶液中滴加CaCl2溶液,产生白色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-09更新
|
461次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)(已下线)专题13 化学实验方案的设计与评价河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 4-溴甲基肉桂酸甲酯是合成抗肿瘤药物帕比司他的重要中间体,其结构简式如下:
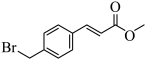
关于4-溴甲基肉桂酸甲酯的说法正确的是

关于4-溴甲基肉桂酸甲酯的说法正确的是
| A.最多有18个原子共平面 |
| B.不能发生消去反应 |
C.与 互为顺反异构体 互为顺反异构体 |
D.最多可消耗 |
您最近一年使用:0次
2023-03-09更新
|
568次组卷
|
5卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)(已下线)专题10 有机化学基础河北省石家庄市河北师范大学附属实验中学2024届高三上学期10月月考化学试题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
8. 下列装置能达到相应实验目的的是
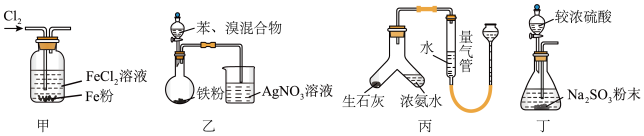

A.利用甲装置可使 粉最终消失得到澄清溶液 粉最终消失得到澄清溶液 |
B.利用乙装置可制备溴苯并验证有 生成 生成 |
C.利用丙装置可制备 并测量其体积 并测量其体积 |
D.利用丁装置可制备 |
您最近一年使用:0次
2023-03-09更新
|
635次组卷
|
5卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)(已下线)专题12 化学实验基础(已下线)第3讲 铁盐及其亚铁盐河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
9. 某碳-碳成键反应的催化剂由R3+和结构如图所示的阴离子组成,X、Y、Z、Q为原子序数依次增大的短周期主族元素,R3+与Ar具有相同的核外电子排布。下列说法正确的是


| A.R位于第四周期ⅢA族 |
| B.X、Y、Z的简单氢化物的沸点依次升高 |
| C.XQ2和QY2的空间结构相同 |
| D.基团-XZ3与碘原子形成的化合物可水解为XZ3H和HIO |
您最近一年使用:0次
2023-03-09更新
|
477次组卷
|
3卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
10. 下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向淀粉溶液中加入适量20% 溶液,加热,冷却后加 溶液,加热,冷却后加 溶液至中性,再滴加少量碘水,溶液变蓝 溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
| B | 将盐酸酸化的 溶液加水稀释,溶液的颜色由黄绿色变为绿色,最终变为蓝色 溶液加水稀释,溶液的颜色由黄绿色变为绿色,最终变为蓝色 | 溶液中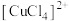 浓度减小, 浓度减小, 浓度增大 浓度增大 |
| C | 将铁锈溶于浓盐酸,滴入 溶液,紫色褪去 溶液,紫色褪去 | 铁锈中含有二价铁 |
| D | 向 溶液中滴加 溶液中滴加 溶液,变红褐色;再滴加 溶液,变红褐色;再滴加 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 |  既发生了水解反应,又发生了还原反应 既发生了水解反应,又发生了还原反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-09更新
|
425次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题11-14)河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题(已下线)选择题6-10
单选题
|
适中(0.65)
名校
解题方法
11. 利用如下流程可从废光盘的金属层中回收其中的银(金属层中其他金属含量过低,对实验影响可忽略):

已知: 溶液在加热时易分解产生
溶液在加热时易分解产生 和
和 ;“溶解”工序发生的反应为可逆反应。下列说法错误的是
;“溶解”工序发生的反应为可逆反应。下列说法错误的是

已知:
 溶液在加热时易分解产生
溶液在加热时易分解产生 和
和 ;“溶解”工序发生的反应为可逆反应。下列说法错误的是
;“溶解”工序发生的反应为可逆反应。下列说法错误的是| A.“氧化”时,适宜选择水浴加热方式 |
| B.若省略第一次过滤,会使氨水的用量增加 |
| C.滤渣Ⅱ洗涤后的滤液可送入“还原”工序利用 |
D.“还原”时,每生成 ,理论上消耗 ,理论上消耗 |
您最近一年使用:0次
2023-03-09更新
|
921次组卷
|
7卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题11-14)(已下线)专题09 物质的反应及转化山东师范大学附属中学2023届高三下学期6月模拟考试化学试题河北省部分学校2023届高三下学期二模联考化学试题重庆市第七中学校2023-2024学年高三下学期2月月考化学试题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
较难(0.4)
名校
12. 金属钯催化乙醇羰基化的反应过程如图所示。下列说法正确的是


| A.在金属钯催化下不能被羰基化的醇中,相对分子质量最小的为60 |
B.整个反应过程的化学方程式为: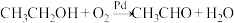 |
| C.反应过程中断裂和形成最多的键是Pd-H键 |
| D.反应过程中钯的化合价没有变化 |
您最近一年使用:0次
2023-03-11更新
|
463次组卷
|
2卷引用:河北省邢台市名校联盟2022-2023学年高三下学期3月模拟考试化学试题
单选题
|
较难(0.4)
名校
解题方法
13. 电化学合成具有反应条件温和、反应试剂纯净和生产效率高等优点,利用下图所示装置可合成己二腈 。充电时生成己二睛,放电时生成
。充电时生成己二睛,放电时生成 ,其中a、b是互为反置的双极膜,双极膜中的
,其中a、b是互为反置的双极膜,双极膜中的 会解离出
会解离出 和
和 向两极移动。下列说法正确的是
向两极移动。下列说法正确的是

 。充电时生成己二睛,放电时生成
。充电时生成己二睛,放电时生成 ,其中a、b是互为反置的双极膜,双极膜中的
,其中a、b是互为反置的双极膜,双极膜中的 会解离出
会解离出 和
和 向两极移动。下列说法正确的是
向两极移动。下列说法正确的是
| A.N极的电势高于M极的电势 |
B.放电时,双极膜中 向M极移动 向M极移动 |
C.充电时,阴极的电极反应式为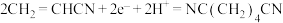 |
D.若充电时制得 ,则放电时需生成 ,则放电时需生成 ,才能使左室溶液恢复至初始状态 ,才能使左室溶液恢复至初始状态 |
【知识点】 原电池、电解池综合考查解读 电解池有关计算解读
您最近一年使用:0次
2023-03-09更新
|
797次组卷
|
6卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题1-16)(已下线)专题11 电化学的综合应用 河北正定中学等名校联盟2023-2024学年高二上学期第三次月考化学试题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
14. 一定温度下,AgCl和Ag2CrO4的沉淀溶解平衡曲线如图所示。
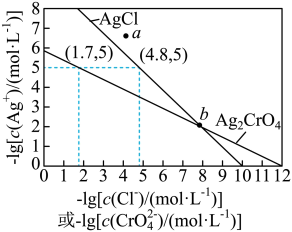
下列说法正确的是

下列说法正确的是
| A.a点条件下能生成Ag2CrO4沉淀,也能生成AgCl沉淀 |
B.b点时,c(Cl-)=c(CrO ),Ksp(AgCl)=Ksp(Ag2CrO4) ),Ksp(AgCl)=Ksp(Ag2CrO4) |
C.Ag2CrO4+2Cl- 2AgCl+CrO 2AgCl+CrO 的平衡常数K=107.9 的平衡常数K=107.9 |
| D.向NaCl、Na2CrO4均为0.1mol·L-1的混合溶液中滴加AgNO3溶液,先产生Ag2CrO4沉淀 |
您最近一年使用:0次
2023-06-12更新
|
15738次组卷
|
32卷引用:2023年高考全国乙卷化学真题
2023年高考全国乙卷化学真题(已下线)T13-溶液中的离子平衡(已下线)2023年高考化学真题完全解读(全国乙卷)(PPT+Word)(已下线)专题16 水溶液中的离子平衡(已下线)第15练 水溶液中的离子平衡图像分析 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)江西省宜丰中学2022-2023学年高二下学期7月期末考试化学试题湖南师范大学附属中学2024届高三摸底考试化学试题 (已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)河南省南阳市第一中学校2023-2024学年高三上学期第一次月考化学试题河南省南阳市南阳一中2023-2024学年高三上学期9月月考化学试题(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第6讲 沉淀溶解平衡图像分析浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷重庆市南开中学校2023-2024学年高二上学期期中考试化学试题(已下线)题型03 电解质溶液图像分析-2024年高考化学答题技巧与模板构建(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)题型14 电解质溶液-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)10-2023新东方高二上期中考化学(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省娄底市新化县2023-2024学年高二上学期期末考试化学试题北京市第一○一中学2023-2024学年高三下学期开学考试化学试题重庆市巫溪县中学校2023-2024学年高二上学期期末模拟考试化学试题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题湖南省邵阳市第二中学2023-2024学年高二下学期入学考试化学试题天津市红桥区2024届高三一模化学试题河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题云南省宣威市第九中学2023-2024学年高三下学期入学考试理综试题-高中化学广西壮族自治区河池市普通高中2024届高三毕业班下学期模拟测试(二模)化学试题福建省福州第三中学2023-2024学年高三下学期第十六次检测(三模)化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
名校
解题方法
15. 苯甲酸乙酯可用于配制香水香精和人造精油,也可用于食品中。某实验小组以苯甲酸和乙醇为原料,利用如图装置合成苯甲酸乙酯,步骤如下:

Ⅰ.反应回流:向 圆底烧瓶中加入磁搅拌子,然后依次加入
圆底烧瓶中加入磁搅拌子,然后依次加入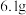 苯甲酸、
苯甲酸、 95%乙醇、
95%乙醇、 环己烷,搅拌均匀后再加入
环己烷,搅拌均匀后再加入 浓硫酸。按如图组装好仪器后,水浴加热回流1.5小时。实验过程中分水器中得到的液体会分层,需多次开启分水器活塞放出下层液体。
浓硫酸。按如图组装好仪器后,水浴加热回流1.5小时。实验过程中分水器中得到的液体会分层,需多次开启分水器活塞放出下层液体。
Ⅱ.产物蒸馏提纯:继续水浴加热,从圆底烧瓶中蒸出环己烷和剩余的乙醇,经分水器放出。将圆底烧瓶中残留物倒入盛有冷水的烧杯中,再经一系列除杂操作后,最后蒸馏收集210~213℃的馏分,得到 产品。
产品。
可能用到的数据如下:
*环己烷、乙醇和水可形成共沸物,其沸点为62.1℃。
回答下列问题:
(1)若用 标记乙醇,则所得产品苯甲酸乙酯的结构简式为
标记乙醇,则所得产品苯甲酸乙酯的结构简式为___________ 。
(2)如果步骤Ⅰ中加热一段时间后发现忘记加入磁搅拌子,应采取的正确操作为___________ 。
(3)步骤Ⅰ中“多次开启分水器活塞放出下层液体”的目的为___________ 。
(4)步骤Ⅱ中“一系列除杂操作”用到的试剂包括a.无水氯化钙b.碳酸钠c.食盐。按照操作先后顺序,应依次加入___________ (填试剂的字母编号)。操作过程中,当观察到___________ 现象时,即可停止加入碳酸钠;加入食盐的目的为___________ 。
(5)步骤Ⅱ中蒸馏收集产物时,所需用到的玻璃仪器有酒精灯、蒸馏烧瓶、尾接管、接收瓶和___________ (填仪器名称)。
(6)本实验的产率为___________ %(保留两位有效数字)。
(7)下列仪器不能为产品结构分析提供有效信息的是___________ (填选项字母)。
A元素分析仪 B.质谱仪 C.红外光谱仪 D.核磁共振仪 E.X射线衍射仪

Ⅰ.反应回流:向
 圆底烧瓶中加入磁搅拌子,然后依次加入
圆底烧瓶中加入磁搅拌子,然后依次加入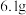 苯甲酸、
苯甲酸、 95%乙醇、
95%乙醇、 环己烷,搅拌均匀后再加入
环己烷,搅拌均匀后再加入 浓硫酸。按如图组装好仪器后,水浴加热回流1.5小时。实验过程中分水器中得到的液体会分层,需多次开启分水器活塞放出下层液体。
浓硫酸。按如图组装好仪器后,水浴加热回流1.5小时。实验过程中分水器中得到的液体会分层,需多次开启分水器活塞放出下层液体。Ⅱ.产物蒸馏提纯:继续水浴加热,从圆底烧瓶中蒸出环己烷和剩余的乙醇,经分水器放出。将圆底烧瓶中残留物倒入盛有冷水的烧杯中,再经一系列除杂操作后,最后蒸馏收集210~213℃的馏分,得到
 产品。
产品。可能用到的数据如下:
| 相对分子质量 | 密度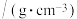 | 沸点/℃ | 水中溶解性 | |
| 苯甲酸 | 122 | 1.266 | 249 | 微溶 |
| 乙醇 | 46 | 0.789 | 78 | 溶 |
| 苯甲酸乙酯 | 150 | 1.045 | 213 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.8* | 难溶 |
回答下列问题:
(1)若用
 标记乙醇,则所得产品苯甲酸乙酯的结构简式为
标记乙醇,则所得产品苯甲酸乙酯的结构简式为(2)如果步骤Ⅰ中加热一段时间后发现忘记加入磁搅拌子,应采取的正确操作为
(3)步骤Ⅰ中“多次开启分水器活塞放出下层液体”的目的为
(4)步骤Ⅱ中“一系列除杂操作”用到的试剂包括a.无水氯化钙b.碳酸钠c.食盐。按照操作先后顺序,应依次加入
(5)步骤Ⅱ中蒸馏收集产物时,所需用到的玻璃仪器有酒精灯、蒸馏烧瓶、尾接管、接收瓶和
(6)本实验的产率为
(7)下列仪器不能为产品结构分析提供有效信息的是
A元素分析仪 B.质谱仪 C.红外光谱仪 D.核磁共振仪 E.X射线衍射仪
您最近一年使用:0次
2023-03-09更新
|
962次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(实验探究题)(已下线)专题16 实验题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
16. 湿法炼锌综合回收系统产出的萃余液中含有Na2SO4、ZnSO4、H2SO4,还含有Mn2+、Co2+、Ni2+、Cd2+、Fe2+、Al3+等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
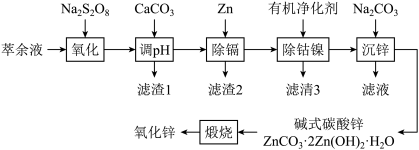
回答下列问题:
(1)“氧化”时,Mn2+、Fe2+均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为___________ 。
(2)“调pH”时,所得“滤渣1”中除含有MnO2和Fe(OH)3外,还有___________ 。
(3)“除镉”时,发生反应的类型为___________ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物。其净化原理可表示为:
反应时,接受电子对的一方是___________ ;Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为___________ 。
(5)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为___________ 。
(6)“沉锌”时,所得滤液经硫酸酸化后,用惰性电极电解可制备Na2S2O8,从而实现原料的循环利用,该电解过程中总反应的化学方程式为___________ 。
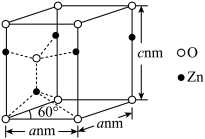
(7)氧化锌有多种晶体结构,其中一种晶胞结构及晶胞参数如图所示。已知阿伏加德罗常数的值为NA,则该氧化锌晶体的密度为___________ g∙cm-3 (列出计算式即可)。

回答下列问题:
(1)“氧化”时,Mn2+、Fe2+均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为
(2)“调pH”时,所得“滤渣1”中除含有MnO2和Fe(OH)3外,还有
(3)“除镉”时,发生反应的类型为
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物。其净化原理可表示为:

反应时,接受电子对的一方是
(5)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为
(6)“沉锌”时,所得滤液经硫酸酸化后,用惰性电极电解可制备Na2S2O8,从而实现原料的循环利用,该电解过程中总反应的化学方程式为
(7)氧化锌有多种晶体结构,其中一种晶胞结构及晶胞参数如图所示。已知阿伏加德罗常数的值为NA,则该氧化锌晶体的密度为

您最近一年使用:0次
2023-03-09更新
|
710次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(工业流程题)(已下线)专题18 工艺流程题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
解答题-原理综合题
|
困难(0.15)
名校
解题方法
17. 二甲醚是重要的有机合成原料:工业上常用合成气(主要成分为 、
、 )制备二甲醚,其主要反应如下:
)制备二甲醚,其主要反应如下:
反应ⅰ: ,
,
反应ⅱ: ,
,
反应ⅲ: ,
,
(1)已知 时,由稳定态单质生成
时,由稳定态单质生成 化合物的焓变称为该物质的标准摩尔生成焓
化合物的焓变称为该物质的标准摩尔生成焓 。几种物质的标准摩尔生成焓如下表所示,据此计算
。几种物质的标准摩尔生成焓如下表所示,据此计算
___________  。
。
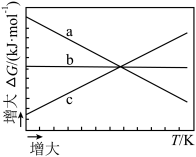
(2)已知 ,
, 随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是___________ (填线条字母)。
(3)在 催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
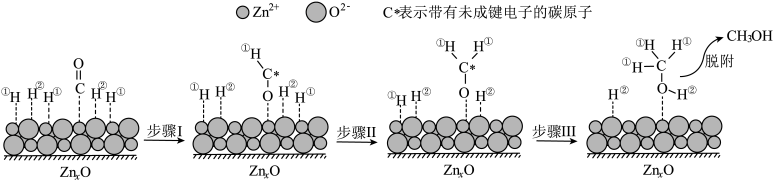
①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为___________ 。
②在合成甲醇过程中,需要不断分离出甲醇的原因为___________ (填选项字母)。
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
(4)一定温度下,在体积为 的刚性容器中充入
的刚性容器中充入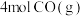 和
和 制备二甲醚,
制备二甲醚, 时达到平衡,平衡时
时达到平衡,平衡时 的转化率为80%,
的转化率为80%, ,且
,且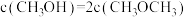 。
。
① 内,
内,
___________  。
。
②反应ⅲ的平衡常数
___________ (保留三位有效数字)。
(5)实际工业生产中,需要在260℃、压强恒为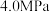 的反应釜中进行上述反应。初始时向反应釜中加入
的反应釜中进行上述反应。初始时向反应釜中加入 和
和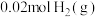 ,为确保反应的连续性,需向反应釜中以
,为确保反应的连续性,需向反应釜中以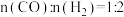 、进气流量
、进气流量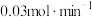 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。
①需控制出气流量小于进气流量的原因为___________ 。
②已知出气流量为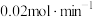 ,单位时间内
,单位时间内 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为___________ 。
 、
、 )制备二甲醚,其主要反应如下:
)制备二甲醚,其主要反应如下:反应ⅰ:
 ,
,
反应ⅱ:
 ,
,
反应ⅲ:
 ,
,
(1)已知
 时,由稳定态单质生成
时,由稳定态单质生成 化合物的焓变称为该物质的标准摩尔生成焓
化合物的焓变称为该物质的标准摩尔生成焓 。几种物质的标准摩尔生成焓如下表所示,据此计算
。几种物质的标准摩尔生成焓如下表所示,据此计算
 。
。| 物质 |  |  |  |
 | 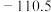 | 0.0 | 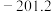 |
 ,
, 随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
(3)在
 催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为
②在合成甲醇过程中,需要不断分离出甲醇的原因为
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
(4)一定温度下,在体积为
 的刚性容器中充入
的刚性容器中充入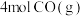 和
和 制备二甲醚,
制备二甲醚, 时达到平衡,平衡时
时达到平衡,平衡时 的转化率为80%,
的转化率为80%, ,且
,且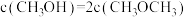 。
。①
 内,
内,
 。
。②反应ⅲ的平衡常数

(5)实际工业生产中,需要在260℃、压强恒为
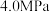 的反应釜中进行上述反应。初始时向反应釜中加入
的反应釜中进行上述反应。初始时向反应釜中加入 和
和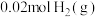 ,为确保反应的连续性,需向反应釜中以
,为确保反应的连续性,需向反应釜中以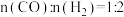 、进气流量
、进气流量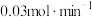 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。①需控制出气流量小于进气流量的原因为
②已知出气流量为
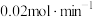 ,单位时间内
,单位时间内 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为
您最近一年使用:0次
2023-03-09更新
|
938次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(原理综合题)(已下线)专题17 原理综合题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
解答题-有机推断题
|
适中(0.65)
名校
解题方法
18. 布洛芬(N)是一种家中常备退烧药,转位重排法是合成布洛芬的主要方法,其合成路线见下图所示。

已知:①
②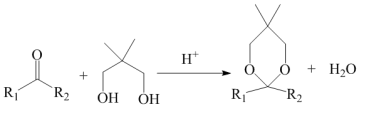
回答下列问题:
(1)F的名称为___________ ,其易溶于水的原因为___________ 。
(2)A→B的反应类型为___________ ,M中含有的官能团名称为___________ 。
(3)E+F→G的化学方程式为___________ 。
(4)手性分子在生命科学和药物生产方面有广泛应用。对于手性药物,一个异构体可能有效,另一个异构体可能无效甚至有害。布洛芬分子(N)中存在的手性碳原子个数为___________ 个。
(5)苯环上的一氯取代物有两种的D的同分异构体有___________ 种(不含立体异构),写出其中核磁共振氢谱显示四组峰,且峰面积之比为 的结构简式
的结构简式___________ 。
(6)对甲基苯丙酮( )为常用化工原料。结合上述流程,以甲苯和丙烯为原料制备对甲基苯丙酮的合成路线为(无机试剂任选)
)为常用化工原料。结合上述流程,以甲苯和丙烯为原料制备对甲基苯丙酮的合成路线为(无机试剂任选)___________ 。

已知:①

②

回答下列问题:
(1)F的名称为
(2)A→B的反应类型为
(3)E+F→G的化学方程式为
(4)手性分子在生命科学和药物生产方面有广泛应用。对于手性药物,一个异构体可能有效,另一个异构体可能无效甚至有害。布洛芬分子(N)中存在的手性碳原子个数为
(5)苯环上的一氯取代物有两种的D的同分异构体有
 的结构简式
的结构简式(6)对甲基苯丙酮(
 )为常用化工原料。结合上述流程,以甲苯和丙烯为原料制备对甲基苯丙酮的合成路线为(无机试剂任选)
)为常用化工原料。结合上述流程,以甲苯和丙烯为原料制备对甲基苯丙酮的合成路线为(无机试剂任选)【知识点】 有机物的推断 根据题给物质选择合适合成路线解读
您最近一年使用:0次
2023-03-09更新
|
487次组卷
|
4卷引用:河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题
河北省石家庄市2023届高中毕业年级教学质量检测(一)化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(有机综合题)(已下线)专题19 有机推断题河北i省石家庄市第二十四中学2023-2024学年高三上学期期末考试化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、化学实验基础、认识化学科学、物质结构与性质、化学反应原理
试卷题型(共 18题)
题型
数量
单选题
14
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 次氯酸及其性质 硅的物理性质与用途 油脂的性质 化学科学对人类文明发展的意义 | |
| 2 | 0.85 | 硫化物 几种铁的氧化物的物理性质及用途 萃取和分液 | |
| 3 | 0.85 | 阿伏加德罗常数的求算 物质结构基础与NA相关推算 常见共价晶体的结构 | |
| 4 | 0.65 | 离子方程式的正误判断 硝酸的强氧化性 碳酸钠与碳酸氢钠的相互转化 | |
| 5 | 0.85 | 电子排布式 电离能变化规律 共价键的形成及主要类型 | |
| 6 | 0.65 | 浓硫酸的强氧化性 盐类水解规律理解及应用 盐类双水解反应 沉淀转化 | |
| 7 | 0.65 | 有机分子中原子共面的判断 卤代烃的消去反应 含酯基有机物水解消耗NaOH的量的计算 多官能团有机物的结构与性质 | |
| 8 | 0.65 | 氨气的实验室制法 二氧化硫的制备 铁三角转化条件分析及判断 苯的溴代实验探究 | |
| 9 | 0.65 | 元素周期表提供的元素信息 根据原子结构进行元素种类推断 利用杂化轨道理论判断分子的空间构型 氢键对物质性质的影响 | |
| 10 | 0.65 | Fe2+的鉴别及其应用 Fe2+的还原性 化学平衡的移动及其影响因素 淀粉水解及其产物检验相关实验 | |
| 11 | 0.65 | 氧化还原反应有关计算 沉淀的溶解与生成 物质分离、提纯综合应用 常见无机物的制备 | |
| 12 | 0.4 | 醇的催化氧化 | |
| 13 | 0.4 | 原电池、电解池综合考查 电解池有关计算 | |
| 14 | 0.65 | 沉淀的溶解与生成 溶度积常数相关计算 | |
| 二、解答题 | |||
| 15 | 0.4 | 羧酸酯化反应 常见有机物的制备 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 16 | 0.65 | 氧化还原反应的规律 电解池电极反应式及化学方程式的书写与判断 晶胞的有关计算 物质制备的探究 | 工业流程题 |
| 17 | 0.15 | 盖斯定律与热化学方程式 化学反应速率计算 催化剂对化学反应速率的影响 化学平衡常数的有关计算 | 原理综合题 |
| 18 | 0.65 | 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |



