江苏省江阴市长泾高级中学2020-2021学年高一上学期四校期中联考化学试题
江苏
高一
期中
2021-02-14
238次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.荷塘上方的薄雾属于胶体 |
| B.月光通过薄雾时产生了丁达尔效应 |
| C.薄雾中的微粒直径为1~100 nm |
| D.“大漠孤烟直”中“孤烟”的组成成分和这种薄雾的组成成分相同 |
【知识点】 胶体
| A | B | C | D | |
| 电解质 | 盐酸 | 纯碱 | 小苏打 | 铜 |
| 混合物 | 漂白粉 | 液氯 | 发酵粉 | 生石灰 |
| 酸性氧化物 | 三氧化硫 | 一氧化碳 | 二氧化碳 | 二氧化硫 |
| 酸 | 次氯酸 | 醋酸 | 硫酸 | 硝酸 |
| A.A | B.B | C.C | D.D |
【知识点】 无机物质的分类 非电解质、电解质物质类别判断解读
| A.变灰暗是因为生成了过氧化钠 |
| B.出现液滴是碳酸钠吸收水蒸气形成了溶液 |
| C.液滴转化为白色晶体只发生了物理变化 |
| D.最后白色粉末是碳酸钠 |
| A.两者的阳离子与阴离子个数比均为2:1 |
| B.两者均属于碱性氧化物 |
| C.久置于空气中,最终产物不同 |
| D.均能与水发生反应,且均属于氧化还原反应 |
| A.摩尔是国际单位制中 7个基本物理量之一 |
B.1mol氧气中约含  个氧原子 个氧原子 |
| C.在一定温度和压强下,分子数相同的任何气体都具有相同的体积 |
| D.摩尔质量等于相对原子质量或相对分子质量 |
【知识点】 物质的量及单位——摩尔 阿伏加德罗常数 摩尔质量 阿伏加德罗定律的应用解读
A.Na+、K+、 、 、 | B. 、Na+、Cl-、Fe3+ 、Na+、Cl-、Fe3+ |
| C.K+、Cu2+、Cl-、OH- | D.K+、Ca2+、 、 、 |
【知识点】 限定条件下的离子共存解读
A.CaCO3溶于稀盐酸中: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.MgCl2溶液与AgNO3溶液反应:Ag++Cl-=AgCl↓ |
| C.钠与水反应:2Na+H2O=2Na++OH-+H2↑ |
D.硫酸铜溶液与氢氧化钡溶液反应:Ba2++ =BaSO4↓ =BaSO4↓ |
【知识点】 离子方程式的正误判断解读
①Cl2+2KBr=2KCl+Br2
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③2KBrO3+Cl2=Br2+2KClO3
下列说法正确的是
| A.氧化性由强到弱的顺序为:KBrO3>KClO3>Cl2>Br2 |
| B.①中Cl2是氧化剂,KBr发生还原反应 |
| C.②中12.25 g KClO3参加反应时,被氧化的HCl为21.9 g |
| D.③中产物Br2只具有还原性 |
A.0.3mol·L-1的Na2SO4溶液中含有Na+和 的总物质的量为0.9mol 的总物质的量为0.9mol |
| B.标准状况下,11.2L水中所含分子数为0.5mol |
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和 的物质的量浓度相等,则K+和Cl-的物质的量浓度一定相同 的物质的量浓度相等,则K+和Cl-的物质的量浓度一定相同 |
| D.常温常压下,3.2g氧气的物质的量为0.1mol |
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将二氧化锰加入浓盐酸中加热 | 产生黄绿色气体 | 二氧化锰表现氧化性 |
| B | 将Na投入水中 | Na浮在水面运动 | Na的熔点低 |
| C | 用pH试纸测定氯水的pH | pH试纸先变红后褪色 | 氯水只显酸性 |
| D | 向某溶液中加入硝酸银溶液 | 产生白色沉淀 | 原溶液一定有Cl- |
| A.A | B.B | C.C | D.D |
【知识点】 氯水 氯气的制法 钠与水反应原理解读 化学实验方案的设计与评价
| A.分子数:CO<CO2 | B.原子数:CO>CO2 |
| C.气体的密度:CO>CO2 | D.气体的体积:CO<CO2 |
【知识点】 摩尔质量 气体摩尔体积 阿伏加德罗定律及其推论解读
| A.等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 |
| B.放入等质量的水中溶解,溶解质量多的为小苏打 |
| C.分别加热两种样品,全部分解挥发,没有残留物的是小苏打 |
| D.先将两样品配成溶液,再分别加入氢氧化钠溶液,可以区分这两种物质 |
| A.Cl2具有漂白性,可用于漂白干燥的有色布条 |
| B.Cl2能与碱反应,工业上利用Cl2与石灰乳反应制漂白粉 |
| C.碳酸氢钠受热分解,用于治疗胃酸过多 |
| D.氢气和氯气混合光照反应,工业上用于制盐酸 |
| A.氯化钠溶液中滴入硝酸银溶液 |
| B.金属钠在氯气中燃烧 |
| C.铁片置于硫酸铜溶液中 |
| D.氢氧化钠溶液与稀硫酸反应 |
【知识点】 离子反应概念解读 氧化还原反应基本概念

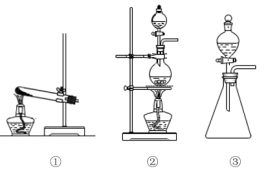
| A.用装置甲制取氯气 |
| B.用装置乙除去氯气中的少量氯化氢 |
| C.用装置丙收集氯气 |
| D.用装置丁吸收剩余的氯气 |
【知识点】 氯气的实验室制法解读 常见气体的制备与收集解读
 、
、 中的一种或几种,对其进行如下实验操作:
中的一种或几种,对其进行如下实验操作:(1)取少量溶液,滴加无色酚酞试液,酚酞变红;
(2)另取少量溶液,加入足量BaCl2溶液,产生白色沉淀;
(3)向(2)所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
(4)将(3)所得混合物过滤,向滤液中加入AgNO3溶液,有白色沉淀生成。下列对该溶液的说法正确的是
A.一定含有OH-、 、 、 、Cl- 、Cl- |
| B.一定不含有Ag+、Ba2+、Cu2+ |
| C.可能含有K+、Cl- |
| D.一定含有K+、Cl- |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 离子的检验
| A.NaCN中碳元素化合价为+2价,在反应中发生还原反应 |
| B.当有0.5 mol NaCN发生反应时生成标准状况下氨气的体积为11.2 L |
| C.NaHCO3既是氧化产物也是还原产物 |
| D.H2O2在该反应中只表现氧化性 |
【知识点】 氧化还原反应的应用 氧化还原反应有关计算 氧化还原反应的规律解读
| A.200 mL0.90 mol·L-1 KClO3溶液 | B.50 mL0.60 mol·L-1 AlCl3溶液 |
| C.200 mL0.45 mol·L-1 ZnCl2溶液 | D.100 mL0.90 mol·L-1 KCl溶液 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读

| A.所充氯气应用向上排空气法收集 |
| B.反应中,烧瓶内产生大量白色烟雾 |
| C.玻璃导管只起到定位加入钠和水的作用 |
| D.烧瓶中Cl2,可能参与四个氧化还原反应 |
二、计算题 添加题型下试题
(1)已知铁的相对原子质量是56,则1个铁原子的质量是
(2)在标准状况下,1.7g氨气所占的体积为
(3)同温同压下同体积的H2和A气体的质量分别是0.2g和l.6g,则气体A的摩尔质量为
三、填空题 添加题型下试题
(1)能导电的是
(2)写出物质⑤溶于水的电离方程式:
(3)写出物质⑤和⑥反应的离子方程式:
四、解答题 添加题型下试题
 Na2SO4+Cl2↑+H2O;为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:
Na2SO4+Cl2↑+H2O;为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置: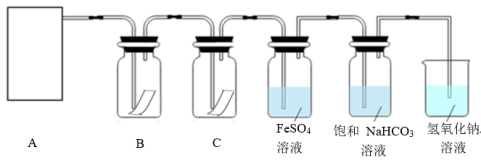
(1)从①、②、③装置中选择合适的制氯气装置(A处)
(2)装置B、C 中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
(3)反应一段时间后,该同学发现硫酸亚铁(FeSO4)溶液变黄,是氯气把亚铁离子氧化为铁离子,请试着写出该反应的离子方程式
(4)氯气通入饱和NaHCO3 溶液能产生无色气体,该实验证明氯气与水反应的生成物中含有(写化学式)

(1)B装置的作用是
(2)在双球干燥管C中发生反应的化学方程式是
(3)双球干燥管C处和D处观察到的实验现象是:C处
(4)若一开始A管内固体质量为10.0 g,充分反应后A管内固体质量减少了3.1 g,求原混合物中碳酸钠的质量分数
【知识点】 过氧化钠 碳酸氢钠 物质的分离、提纯 物质性质实验方案的设计解读
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 胶体 | |
| 2 | 0.94 | 焰色试验 | |
| 3 | 0.65 | 无机物质的分类 非电解质、电解质物质类别判断 | |
| 4 | 0.65 | 钠 钠与氧气等非金属的反应 氧化钠的化学性质 碳酸钠 | |
| 5 | 0.65 | 氧化钠 过氧化钠 | |
| 6 | 0.85 | 物质的量及单位——摩尔 阿伏加德罗常数 摩尔质量 阿伏加德罗定律的应用 | |
| 7 | 0.85 | 限定条件下的离子共存 | |
| 8 | 0.65 | 离子方程式的正误判断 | |
| 9 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应有关计算 氧化还原反应的规律 | |
| 10 | 0.65 | 22.4L/mol适用条件 根据n=m/M进行相关计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 11 | 0.65 | 氯水 氯气的制法 钠与水反应原理 化学实验方案的设计与评价 | |
| 12 | 0.65 | 摩尔质量 气体摩尔体积 阿伏加德罗定律及其推论 | |
| 13 | 0.65 | 碳酸钠与碳酸氢钠性质的比较 碳酸钠与碳酸氢钠鉴别的实验 | |
| 14 | 0.65 | 氯气 次氯酸及其性质 漂白粉和漂粉精 碳酸氢钠的俗称、物理性质及用途 | |
| 15 | 0.85 | 离子反应概念 氧化还原反应基本概念 | |
| 16 | 0.65 | 氯气的实验室制法 常见气体的制备与收集 | |
| 17 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 离子的检验 | |
| 18 | 0.65 | 氧化还原反应的应用 氧化还原反应有关计算 氧化还原反应的规律 | |
| 19 | 0.85 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 20 | 0.65 | 氯气的化学性质 钠与水反应原理 | |
| 二、计算题 | |||
| 21 | 0.65 | 气体摩尔体积 阿伏加德罗定律 物质的量有关计算 | |
| 三、填空题 | |||
| 22 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 电离方程式 | |
| 四、解答题 | |||
| 23 | 0.65 | 氯气的实验室制法 化学实验探究 | 实验探究题 |
| 24 | 0.65 | 过氧化钠 碳酸氢钠 物质的分离、提纯 物质性质实验方案的设计 | 实验探究题 |



