反应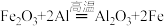 在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是
在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是_______ 。在该反应中_______ 元素的化合价升高,该元素的原子_______ 电子,被________ ;而______ 元素的化合价降低,该元素的原子______ 电子,被_______ 。该反应中, 发生了
发生了______ 反应, 发生了
发生了______ 反应,______ 是氧化剂,______ 是氧化产物,______ 是还原剂,_____ 是还原产物。
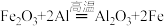 在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是
在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是 发生了
发生了 发生了
发生了
更新时间:2020-09-04 10:44:59
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓 或浓
或浓 反应生成
反应生成 以回收
以回收 。完成下列填空:
。完成下列填空:
(1) 和浓
和浓 反应的还原产物为
反应的还原产物为 和
和 ,且
,且 和
和 的物质的量之比为1:1,写出
的物质的量之比为1:1,写出 和浓
和浓 的化学反应方程式
的化学反应方程式___________
(2)已知: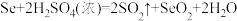
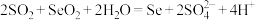
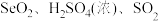 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是___________
(3)回收得到的 的含量。可以通过下面的方法测定:
的含量。可以通过下面的方法测定:
①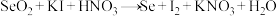
②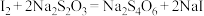
配平方程式①,并用双线桥标出电子转移的方向和数目___________
(4)上述②方程式中每生成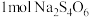 转移电子数的物质的量为:
转移电子数的物质的量为:___________
 或浓
或浓 反应生成
反应生成 以回收
以回收 。完成下列填空:
。完成下列填空:(1)
 和浓
和浓 反应的还原产物为
反应的还原产物为 和
和 ,且
,且 和
和 的物质的量之比为1:1,写出
的物质的量之比为1:1,写出 和浓
和浓 的化学反应方程式
的化学反应方程式(2)已知:
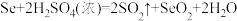
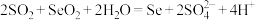
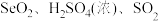 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是(3)回收得到的
 的含量。可以通过下面的方法测定:
的含量。可以通过下面的方法测定:①
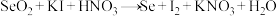
②
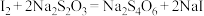
配平方程式①,并用双线桥标出电子转移的方向和数目
(4)上述②方程式中每生成
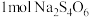 转移电子数的物质的量为:
转移电子数的物质的量为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用氯元素的价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①~⑩均含氯元素。回答下列问题:

(1)④的化学式为___________ ,⑦的电离方程式为___________ 。
(2)工业制漂白粉是将①通入___________ 中制成的,反应的离子方程式为___________ 。
(3)工业上常用 制备
制备 ,该反应的化学方程式为
,该反应的化学方程式为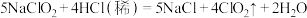 ,
,___________ (用双线桥标明电子转移方向和数目),氧化产物与还原产物物质的量之比为___________ 。
(4)比较⑥和⑦溶液的酸性强弱___________ (填可以或不可以)用pH试纸分别测定。
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的 转化为
转化为 ,整个过程对环境无污染,反应的离子方程式为
,整个过程对环境无污染,反应的离子方程式为___________ 。

(1)④的化学式为
(2)工业制漂白粉是将①通入
(3)工业上常用
 制备
制备 ,该反应的化学方程式为
,该反应的化学方程式为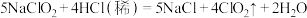 ,
,(4)比较⑥和⑦溶液的酸性强弱
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的
 转化为
转化为 ,整个过程对环境无污染,反应的离子方程式为
,整个过程对环境无污染,反应的离子方程式为
您最近一年使用:0次
【推荐3】实验室用50mL浓盐酸和足量的氯酸钾固体共热制取氯气,其中氯气中的氯元素部分来自氯酸钾,部分来自盐酸,该反应的化学方程式为: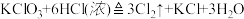
(1)用双线桥法表示电子转移的方向和数目_____________________________
(2)浓盐酸在此反应中体现的化学性质是________ (填写编号)
①挥发性 ②酸性 ③氧化性 ④还原性
(3)当反应过程转移电子数为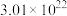 时,产生的
时,产生的 在标准状况下的体积为
在标准状况下的体积为________ mL。
(4)当反应结束时,生成氯气为0.15mol,若反应中HCl的利用率为50%,则原浓盐酸的物质的量浓度为________ 。
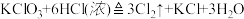
(1)用双线桥法表示电子转移的方向和数目
(2)浓盐酸在此反应中体现的化学性质是
①挥发性 ②酸性 ③氧化性 ④还原性
(3)当反应过程转移电子数为
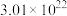 时,产生的
时,产生的 在标准状况下的体积为
在标准状况下的体积为(4)当反应结束时,生成氯气为0.15mol,若反应中HCl的利用率为50%,则原浓盐酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应是中学化学中常见的一种反应类型,请根据要求完成下列问题。
(1)在工业上次磷酸( )常用于化学镀银,发生的反应如下:
)常用于化学镀银,发生的反应如下:
 (未配平),请回答下列问题:
(未配平),请回答下列问题:
① 中,P元素的化合价为
中,P元素的化合价为___________ ;该反应中, 被
被___________ (填“氧化”或“还原”)。
②若该反应有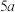 个电子转移,则镀件镀上银的质量为
个电子转移,则镀件镀上银的质量为___________ g(已知每个银原子质量为b克)。
③ 是一元弱酸,写出其与足量
是一元弱酸,写出其与足量 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(2)根据反应 ,回答下列问题。
,回答下列问题。
①氧化剂与还原剂的分子数之比为___________ 。
②若在参加反应的 中,被氧化的
中,被氧化的 比其余
比其余 少3.4g,则被氧化的
少3.4g,则被氧化的 为
为___________ g。
(3)在氯氧化法处理含 的废水过程中,液氯在碱性条件下可以将氧化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
的废水过程中,液氯在碱性条件下可以将氧化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
①某厂废水中含 ,其浓度为
,其浓度为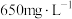 。现用氯氧化法处理,发生反应(其中N均为
。现用氯氧化法处理,发生反应(其中N均为 价、O均为
价、O均为 价)
价) 。该反应中,被氧化的元素是
。该反应中,被氧化的元素是___________ ,氧化产物是___________ 。处理上述废水20.0L,使 完全转化为
完全转化为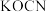 ,至少需氯气
,至少需氯气___________ g。
②投入过量液氯,可将氰酸盐进一步氧化为氮气。请用单线桥法标出电子转移方向和数目:

___________
(1)在工业上次磷酸(
 )常用于化学镀银,发生的反应如下:
)常用于化学镀银,发生的反应如下: (未配平),请回答下列问题:
(未配平),请回答下列问题:①
 中,P元素的化合价为
中,P元素的化合价为 被
被②若该反应有
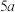 个电子转移,则镀件镀上银的质量为
个电子转移,则镀件镀上银的质量为③
 是一元弱酸,写出其与足量
是一元弱酸,写出其与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(2)根据反应
 ,回答下列问题。
,回答下列问题。①氧化剂与还原剂的分子数之比为
②若在参加反应的
 中,被氧化的
中,被氧化的 比其余
比其余 少3.4g,则被氧化的
少3.4g,则被氧化的 为
为(3)在氯氧化法处理含
 的废水过程中,液氯在碱性条件下可以将氧化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
的废水过程中,液氯在碱性条件下可以将氧化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。①某厂废水中含
 ,其浓度为
,其浓度为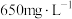 。现用氯氧化法处理,发生反应(其中N均为
。现用氯氧化法处理,发生反应(其中N均为 价、O均为
价、O均为 价)
价) 。该反应中,被氧化的元素是
。该反应中,被氧化的元素是 完全转化为
完全转化为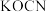 ,至少需氯气
,至少需氯气②投入过量液氯,可将氰酸盐进一步氧化为氮气。请用单线桥法标出电子转移方向和数目:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(2)工业废水中含有的重铬酸根离子(Cr2O )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是___________ (填离子符号,下同),氧化剂是___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是___________ (填化学式,下同),氧化剂是___________ 。
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:________
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是___________ (填化学式,下同),被还原的是___________ 。
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(2)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】过氧化氢(分子结构为H—O—O—H)俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.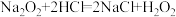
B.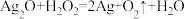
C.
D.
E.4H2O2+ +2H+=2CrO5+5H2O(CrO5分子结构为
+2H+=2CrO5+5H2O(CrO5分子结构为 )
)
(1)A反应属于四种基本反应类型中的___________ (填化学反应名称)。
(2)上述反应中,H2O2仅体现还原性的是___________ (填字母序号,下同),H2O2既体现氧化性又体现还原性的反应是___________ ;
(3)E反应___________ (填“是”、“不是”)氧化还原反应,你的判断理由是___________ 。
(4)配平下列足量的酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目:___________ 。
 +H2O2+_________—Mn2++O2↑+__________
+H2O2+_________—Mn2++O2↑+__________
(5)将黄色、微溶的NaBiO3固体加入MnSO4和H2SO4的混合溶液里并加热,最后溶液显紫色(Bi3+无色)。写出该反应的离子方程式:___________ 。
A.
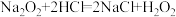
B.
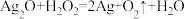
C.

D.

E.4H2O2+
 +2H+=2CrO5+5H2O(CrO5分子结构为
+2H+=2CrO5+5H2O(CrO5分子结构为 )
)(1)A反应属于四种基本反应类型中的
(2)上述反应中,H2O2仅体现还原性的是
(3)E反应
(4)配平下列足量的酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式,并用单线桥法标出反应中电子转移的方向和数目:
 +H2O2+_________—Mn2++O2↑+__________
+H2O2+_________—Mn2++O2↑+__________(5)将黄色、微溶的NaBiO3固体加入MnSO4和H2SO4的混合溶液里并加热,最后溶液显紫色(Bi3+无色)。写出该反应的离子方程式:
您最近一年使用:0次



