某化学兴趣小组在习题解析中看到:“ 通入
通入 溶液出现白色沉淀,是因为在酸性环境中,
溶液出现白色沉淀,是因为在酸性环境中, 将
将 氧化成
氧化成 而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是
而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是 氧化了
氧化了 ,与
,与 无关”,于是做了“
无关”,于是做了“ 通入
通入 溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:
溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:_______________________ 。
(2)为探究硫酸钡产生的原因,分别在装置C中进行以下探究实验,则③④号实验,应该选用的试剂为____________ 。
(3)进行①③号实验前通入氮气的目的是________________________ 。
(4)实验现象:①号依然澄清,②③④号均出现浑浊。据此请补充②号实验中装置C中反应生成沉淀的化学方程式__________________________________ 。
(5)图1~4分别为①②③④号实验所测pH随时间变化曲线。_______________________ 。
(6)计算实验②500s时产生硫酸钡的质量为__________ mg。(可忽略 溶于水产生的
溶于水产生的 )
)
 通入
通入 溶液出现白色沉淀,是因为在酸性环境中,
溶液出现白色沉淀,是因为在酸性环境中, 将
将 氧化成
氧化成 而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是
而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是 氧化了
氧化了 ,与
,与 无关”,于是做了“
无关”,于是做了“ 通入
通入 溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:
溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:
(2)为探究硫酸钡产生的原因,分别在装置C中进行以下探究实验,则③④号实验,应该选用的试剂为
编号 | ① | ② | ③ | ④ |
试剂 | 煮沸过的0.1mol/L 溶液50mL,再加入食用油25mL 溶液50mL,再加入食用油25mL | 未煮沸过的0.1mol/L 溶液50mL 溶液50mL | 煮沸过的________溶液50mL,再加入食用油25mL | 未煮沸过的__________溶液50mL |
(3)进行①③号实验前通入氮气的目的是
(4)实验现象:①号依然澄清,②③④号均出现浑浊。据此请补充②号实验中装置C中反应生成沉淀的化学方程式
(5)图1~4分别为①②③④号实验所测pH随时间变化曲线。

(6)计算实验②500s时产生硫酸钡的质量为
 溶于水产生的
溶于水产生的 )
)
更新时间:2024-05-05 22:54:12
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】某化学小组设计如下装置,探究铜和一定量的浓HNO3是否反应是否有NO生成。已知:A试管内空气体积为50mL(标准状况),B广口瓶盛80mL水,硝酸不溶于煤油。
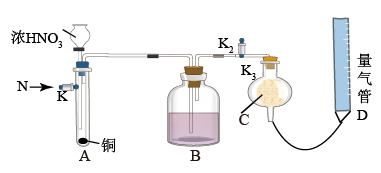
请回答下列问题:
(1)加入浓HNO3前应先通一段时间N2,具体操作为:______ ,其作用是_______ 。
(2)关闭K1、K2,打开K3,通过分液漏斗向试管中加入一定量的浓硝酸,然后在硝酸上方加一层煤油,煤油的作用是_____ ,待铜和硝酸反应完毕后,通过分液漏斗向试管中加煤油直至试管充满。
(3)读取量气管读数时,要先________ ,然后再读取读数。
(4)数据分析:
① 从B中取20mL溶液,恰好中和用去0.lmol/L的NaOH体积为16mL则B中所得硝酸的物质的量浓度为_______ 。
② 假设只生成NO2,通过计算理论上收集到的气体体积为_______ mL (标准状况下)。
③实验最终测得气体的体积为130.5mL(标准状况下),与理论值有差异,其理由可能为______ 。
A.Cu与一定物质的量浓度的HNO3反反应除了生成NO2还生成NO
B.过程中还发生了反应4NO+3O2+2H2O=4HNO3
C.过程中还发生了反应4NO2+O2+2H2O=4HNO3
D.硝酸具有挥发性,对实验有影响

请回答下列问题:
(1)加入浓HNO3前应先通一段时间N2,具体操作为:
(2)关闭K1、K2,打开K3,通过分液漏斗向试管中加入一定量的浓硝酸,然后在硝酸上方加一层煤油,煤油的作用是
(3)读取量气管读数时,要先
(4)数据分析:
① 从B中取20mL溶液,恰好中和用去0.lmol/L的NaOH体积为16mL则B中所得硝酸的物质的量浓度为
② 假设只生成NO2,通过计算理论上收集到的气体体积为
③实验最终测得气体的体积为130.5mL(标准状况下),与理论值有差异,其理由可能为
A.Cu与一定物质的量浓度的HNO3反反应除了生成NO2还生成NO
B.过程中还发生了反应4NO+3O2+2H2O=4HNO3
C.过程中还发生了反应4NO2+O2+2H2O=4HNO3
D.硝酸具有挥发性,对实验有影响
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:







(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是________ ;
②在工业生产中B转化为C的化学方程式____________________________ 。
(2)若A在常温下为无色无味的气体,C是红棕色的气体。
①A、C的化学式分别是:A________ ;C________ 。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式___________________ 。







(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是
②在工业生产中B转化为C的化学方程式
(2)若A在常温下为无色无味的气体,C是红棕色的气体。
①A、C的化学式分别是:A
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】请回答下列问题。
I.X、Y、Z、是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是(含硫)化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用:Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液能使酚酞溶液变红色。
请回答下列问题:
(1)浓硫酸与蔗糖进行“黑面包”实验时,产生大量气体中包含气体X,写出产生气体X的化学方程式:_________ 。
(2)实验室用高锰酸钾制备气体Y的离子反应方程式为:__________ 。
(3)W气体的浓溶液可以用于检验Y气体管道的泄露,写出此过程的化学方程式:______ 。
(4)Z与水的反应的化学方程式为:_____ ,此反应中氧化剂与还原剂的物质的量之比为_________ 。
(5)工业上可利用气体W制备硝酸,写出气体W发生催化氧化的化学方程式:_______ 。
II.三硅酸镁( )难溶于水,在医药上可作抗酸剂。它除了可以中和胃液中多余酸之外,生成的
)难溶于水,在医药上可作抗酸剂。它除了可以中和胃液中多余酸之外,生成的 还可覆盖在有溃疡的胃表面,保护其不再受刺激。
还可覆盖在有溃疡的胃表面,保护其不再受刺激。
(6)用氧化物形式表示三硅酸镁________ 。
I.X、Y、Z、是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是(含硫)化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用:Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液能使酚酞溶液变红色。
请回答下列问题:
(1)浓硫酸与蔗糖进行“黑面包”实验时,产生大量气体中包含气体X,写出产生气体X的化学方程式:
(2)实验室用高锰酸钾制备气体Y的离子反应方程式为:
(3)W气体的浓溶液可以用于检验Y气体管道的泄露,写出此过程的化学方程式:
(4)Z与水的反应的化学方程式为:
(5)工业上可利用气体W制备硝酸,写出气体W发生催化氧化的化学方程式:
II.三硅酸镁(
 )难溶于水,在医药上可作抗酸剂。它除了可以中和胃液中多余酸之外,生成的
)难溶于水,在医药上可作抗酸剂。它除了可以中和胃液中多余酸之外,生成的 还可覆盖在有溃疡的胃表面,保护其不再受刺激。
还可覆盖在有溃疡的胃表面,保护其不再受刺激。(6)用氧化物形式表示三硅酸镁
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】铅蓄电池的回收利用可减少其对环境的污染,具有重要的可持续发展意义。利用废铅蓄电池的铅膏(主要成分为 、
、 和少量的
和少量的 )制备
)制备 的流程如下:
的流程如下:

已知:①常温下,一些铅盐的溶解性如下表:
②常温下,一些氢氧化物沉淀时的 如下表:
如下表:
回答下列问题,
(1)步骤①的桨液通入足量 充分反应后的体系中含有的金属阳离子为
充分反应后的体系中含有的金属阳离子为_______ (填离子符号)。
(2)步骤②中加入 溶液的主要作用是
溶液的主要作用是_______ 。
(3)滤渣1的主要成份是 ,常温时,步骤③应调整溶液
,常温时,步骤③应调整溶液 的范围是
的范围是_______ 。
(4)步骤④中加氨水调 至10,发生反应的离子方程式为
至10,发生反应的离子方程式为_______ 。
(5)上述流程中,已知废铅膏中含铅 ,且灼烧过程铅的回收率为
,且灼烧过程铅的回收率为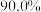 ,若对
,若对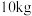 废铅膏进行处理回收得到
废铅膏进行处理回收得到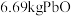 ,流程中其余步骤中铅的损失率共
,流程中其余步骤中铅的损失率共_______ (计算结果保留一位小数)。
 、
、 和少量的
和少量的 )制备
)制备 的流程如下:
的流程如下:
已知:①常温下,一些铅盐的溶解性如下表:
| 铅盐 |  |  |  |
| 溶解性 | 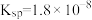 |  | 易溶于水,能部分电离 |
 如下表:
如下表:| 氢氧化物 |  |  | 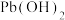 |
开始沉淀的 | 7.0 | 1.9 | 6.0 |
沉淀完全的 | 9.0 | 3.2 | 9.6 |
(1)步骤①的桨液通入足量
 充分反应后的体系中含有的金属阳离子为
充分反应后的体系中含有的金属阳离子为(2)步骤②中加入
 溶液的主要作用是
溶液的主要作用是(3)滤渣1的主要成份是
 ,常温时,步骤③应调整溶液
,常温时,步骤③应调整溶液 的范围是
的范围是(4)步骤④中加氨水调
 至10,发生反应的离子方程式为
至10,发生反应的离子方程式为(5)上述流程中,已知废铅膏中含铅
 ,且灼烧过程铅的回收率为
,且灼烧过程铅的回收率为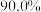 ,若对
,若对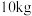 废铅膏进行处理回收得到
废铅膏进行处理回收得到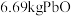 ,流程中其余步骤中铅的损失率共
,流程中其余步骤中铅的损失率共
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
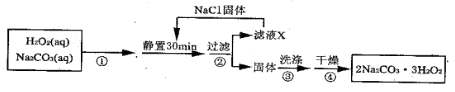
【推荐2】过碳酸钠(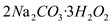 )是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
已知主反应: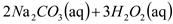

 ∆H<0
∆H<0
副反应: 50℃时
50℃时 开始分解
开始分解
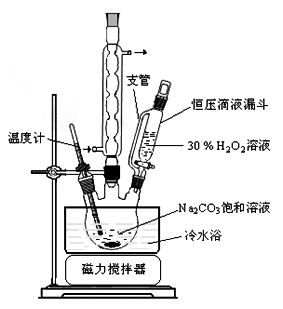
请回答下列问题:
(1)步骤①的关键是_____________ ,其原因是______________________ 。
(2)在滤液X中加入适量NaCl固体的目的是________________________ 。
(3)步骤③中选用无水乙醇洗涤产品的目的是_______________________ 。
(4)下列物质中,会引起过碳酸钠失效的有____________ 。
A.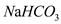 B.
B. C.
C.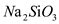 D.HCl
D.HCl
(5)过碳酸钠的产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数;其操作步骤:取样品溶液→加入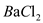 溶液→过滤→洗涤→干燥→称重。需直接测定的物理量有:样品的质量
溶液→过滤→洗涤→干燥→称重。需直接测定的物理量有:样品的质量 g,沉淀的质量
g,沉淀的质量 g,则产品中过碳酸钠质量分数的表达式为:
g,则产品中过碳酸钠质量分数的表达式为:___________ 。
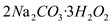 )是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
已知主反应:
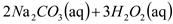

 ∆H<0
∆H<0副反应:
 50℃时
50℃时 开始分解
开始分解
请回答下列问题:
(1)步骤①的关键是
(2)在滤液X中加入适量NaCl固体的目的是
(3)步骤③中选用无水乙醇洗涤产品的目的是
(4)下列物质中,会引起过碳酸钠失效的有
A.
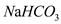 B.
B. C.
C.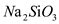 D.HCl
D.HCl(5)过碳酸钠的产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数;其操作步骤:取样品溶液→加入
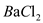 溶液→过滤→洗涤→干燥→称重。需直接测定的物理量有:样品的质量
溶液→过滤→洗涤→干燥→称重。需直接测定的物理量有:样品的质量 g,沉淀的质量
g,沉淀的质量 g,则产品中过碳酸钠质量分数的表达式为:
g,则产品中过碳酸钠质量分数的表达式为:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】磺酰氯( SO2Cl2 )可用于制造锂电池正极活性物质。实验室可利用SO2和Cl2在活性炭催化下反应制取少量SO2Cl2,装置如图(部分夹持装置已省略)。

已知:①SO2(g) +Cl2(g)=SO2Cl2(1) ΔH= -97.3 kJ/mol;
②SO2Cl2熔点为-54.1℃ ,沸点为69.1℃,常温较稳定,遇水剧烈水解,100℃以上易分解。
回答下列问题:
(1)仪器A的名称是___________ ,装置丙中橡胶管的作用是___________ 。
(2)装置丙中发生反应的离子方程式为___________ ,上述仪器的正确连接顺序是e ___________→g,h←___________←f(填仪器接口字母编号,仪器可重复使用)。________
(3)仪器F的作用是___________ 。
(4)装置丁中三颈烧瓶需置于冷水浴中,其原因是___________ 。
(5)某实验小组利用该装置消耗氯气1120 mL(标准状况下,SO2足量) ,最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为___________ ( 结果精确到0.01%)。

已知:①SO2(g) +Cl2(g)=SO2Cl2(1) ΔH= -97.3 kJ/mol;
②SO2Cl2熔点为-54.1℃ ,沸点为69.1℃,常温较稳定,遇水剧烈水解,100℃以上易分解。
回答下列问题:
(1)仪器A的名称是
(2)装置丙中发生反应的离子方程式为
(3)仪器F的作用是
(4)装置丁中三颈烧瓶需置于冷水浴中,其原因是
(5)某实验小组利用该装置消耗氯气1120 mL(标准状况下,SO2足量) ,最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某研究性学习小组得到一块软锰矿样品,其主要成分为二氧化锰( MnO2)和石英(SiO2)。为了制取Cl2和探究氯及其化合物的相关性质,进行如下实验。
【查阅资料】MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑

【制取气体】
(1)取适量矿样置于烧瓶中,加入足量浓盐酸并加热,充分反应后烧瓶中残留的固体是____ 。
(2)收集氯气应将图1导管的a接口与图2导管的_____________ 接口连接(填“b”或“c)。
(3)已知氯气中含有HCl杂质,可用______________ 除去。
【实验探究】
(4)把红热的铁丝伸入盛有氯气的集气瓶中,铁丝燃烧产生棕褐色的烟。反应的化学方程式是_______________________________________________________________________ 。
(5)按图3进行实验,观察到B中的有色布条不褪色,C中的有色布条褪色。由此得出的结论是_____________________________________________________________________ 。
(6)写出C中反应的化学方程式:_________________________________________________ 。
【联系实际】
(7)某氯碱工厂的氯气管道发生泄漏,以下采取的措施正确的是______________ (双项选择,填序号)。
A.将人群向高处疏散
B.将人群向低处疏散
C.关闭氯气管道,用碱液浸泡过的棉布覆盖泄漏部位
D.关闭氯气管道,用饱和NaCl溶液浸泡过的棉布覆盖泄漏部位
【查阅资料】MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
【制取气体】
(1)取适量矿样置于烧瓶中,加入足量浓盐酸并加热,充分反应后烧瓶中残留的固体是
(2)收集氯气应将图1导管的a接口与图2导管的
(3)已知氯气中含有HCl杂质,可用
【实验探究】
(4)把红热的铁丝伸入盛有氯气的集气瓶中,铁丝燃烧产生棕褐色的烟。反应的化学方程式是
(5)按图3进行实验,观察到B中的有色布条不褪色,C中的有色布条褪色。由此得出的结论是
(6)写出C中反应的化学方程式:
【联系实际】
(7)某氯碱工厂的氯气管道发生泄漏,以下采取的措施正确的是
A.将人群向高处疏散
B.将人群向低处疏散
C.关闭氯气管道,用碱液浸泡过的棉布覆盖泄漏部位
D.关闭氯气管道,用饱和NaCl溶液浸泡过的棉布覆盖泄漏部位
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】硫代硫酸钠(Na2S2O3)商品名“海波”,俗名“大苏打”,分析化学上常用于 滴定实验。某化学兴趣小组在实验室制备硫代硫酸钠晶体并探究其化学性质。

I.制备 Na2S2O3
(1)如图,关闭K1打开K2, 反应开始后,装置c中的产物除 了 Na2S2O3外还有一种无色无味 的气体,这种气体是______ 。
(2)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1 ,其目的是_______________ 。待c中溶液冷却后,倒入蒸发皿,通过加热蒸发、冷却结晶和干燥等操作获得Na2S2O3 CH2O晶体。
(3)实验结束后,装置d中的溶质可能有__________________ 。
探究Na2S2O3的部分化学性质
【分析推理】Na2S2O3可以看成是一个S原子取代了 Na2SO4中一个O原子形成的。据此 推测,下列说法正确的是____________ 。
A. S2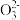 和S
和S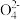 都是正四面体结构 B. S2
都是正四面体结构 B. S2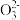 中硫硫键的键长大于硫氧键
中硫硫键的键长大于硫氧键
C. S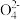 中的键角均为109º28´ D.Na2S2O3中所有原子都满足8电子结构
中的键角均为109º28´ D.Na2S2O3中所有原子都满足8电子结构
【提出假设】①Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3 溶液pH=7。②从S元素的化合价推测Na2S2O3具有较强的还原性。
【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空):
【实验结论】__________________

I.制备 Na2S2O3
(1)如图,关闭K1打开K2, 反应开始后,装置c中的产物除 了 Na2S2O3外还有一种无色无味 的气体,这种气体是
(2)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1 ,其目的是
(3)实验结束后,装置d中的溶质可能有
探究Na2S2O3的部分化学性质
【分析推理】Na2S2O3可以看成是一个S原子取代了 Na2SO4中一个O原子形成的。据此 推测,下列说法正确的是
A. S2
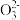 和S
和S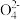 都是正四面体结构 B. S2
都是正四面体结构 B. S2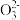 中硫硫键的键长大于硫氧键
中硫硫键的键长大于硫氧键C. S
 中的键角均为109º28´ D.Na2S2O3中所有原子都满足8电子结构
中的键角均为109º28´ D.Na2S2O3中所有原子都满足8电子结构【提出假设】①Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3 溶液pH=7。②从S元素的化合价推测Na2S2O3具有较强的还原性。
【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空):
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| ① | 溶液pH=8 | ||
| ② | 向新制氯水中滴入适量Na2S2O3溶液 | 氯水褪色 |
【实验结论】
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
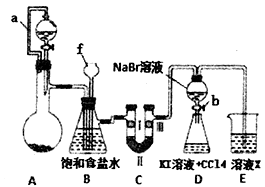
【推荐3】实验是化学研究的重要方法之一,某同学为了制备氯气并探究氯气等物质的相关性质,设计如图所示的实验方案:
(1)仪器f的名称___________ 。
(2)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr207),还原产物是CrCl3,写出A中离子方程式:________________________________ 。
(3)B装置的作用除了用来除去氯气中的氯化氢外还有____________ 。
(4)装置C的作用是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是______________
(填序号)
(5)利用D装置证明溴的非金属性比碘强的实验操作是:实验完毕,_______ ,振荡锥形瓶,现象是_____________________________________________ 。(补充完整上述实验操作和现象)
(6)D装置进行实验时存在的明显不足是________________________________ 。
(1)仪器f的名称
(2)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr207),还原产物是CrCl3,写出A中离子方程式:
(3)B装置的作用除了用来除去氯气中的氯化氢外还有
(4)装置C的作用是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是
(填序号)
① | ② | ③ | ④ | |
I | 湿润的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 湿润的红纸条 |
II | 碱石灰 | 浓硫酸 | 硅胶 | 氯化钠 |
II! | 干燥的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 干燥的红纸条 |
(6)D装置进行实验时存在的明显不足是
您最近一年使用:0次



