H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
(1)定性分析:图甲可通过观察_______________________________________ 定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_____________________________ 。

(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看__________________________ ,实验中需要测量的数据是____________________________________________________ 。
(3)课本在研究浓度对反应速率影响的实验中,酸性高锰酸钾和弱酸草酸反应的离子方程式为____________________________________________________ ,反应开始一段时间后反应速率明显提升的原因是_________________________________________________________________ 。
(1)定性分析:图甲可通过观察

(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看
(3)课本在研究浓度对反应速率影响的实验中,酸性高锰酸钾和弱酸草酸反应的离子方程式为
更新时间:2017-10-21 14:55:46
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】氯、氮、硫等及其化合物性质研究。如图是氮、硫元素的各种价态与物质类别的对应关系:

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为____ 。
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式____ 。
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl b.NO+NO2+H2O 2HNO2 c.HClO+HNO2=HNO3+HCl
2HNO2 c.HClO+HNO2=HNO3+HCl
下列分析正确的是___ 。
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:
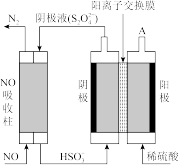
从A口中出来的物质的是____ 。写出电解池阴极的电极反应式____ 。
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=____ ,b=____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是____ (填实验编号)。

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl b.NO+NO2+H2O
 2HNO2 c.HClO+HNO2=HNO3+HCl
2HNO2 c.HClO+HNO2=HNO3+HCl下列分析正确的是
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:

从A口中出来的物质的是
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】硫酸盐(含 )气溶胶是雾霾的主要成分,主要通过
)气溶胶是雾霾的主要成分,主要通过 转化产生。不同
转化产生。不同 条件下
条件下 在水溶液中的主要存在形态及其对应的物质的量分数如图所示:
在水溶液中的主要存在形态及其对应的物质的量分数如图所示: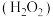 是大气中重要的氧化剂,其有多种途径将
是大气中重要的氧化剂,其有多种途径将 氧化成硫酸盐。
氧化成硫酸盐。
① 可在催化剂
可在催化剂 或
或 的作用下产生
的作用下产生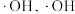 能将
能将 氧化。
氧化。 产生的机理如下:
产生的机理如下:
反应Ⅰ: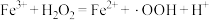 (慢反应);
(慢反应);
反应Ⅱ: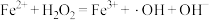 (快反应).
(快反应).
下列说法正确的是________ (填选项字母)。
A.反应涉及非极性键的断裂与形成
B.反应Ⅰ的活化能大于反应Ⅱ
C.向固定容积的反应体系中充入氦气, 氧化
氧化 的反应速率加快
的反应速率加快
D.与 作催化剂相比,相同条件下
作催化剂相比,相同条件下 作催化剂时
作催化剂时 氧化效率可能更高
氧化效率可能更高
②研究表明 与
与 水溶液的反应机理如下:
水溶液的反应机理如下:
Ⅰ.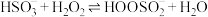 ;
;
Ⅱ.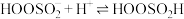 ;
;
Ⅲ.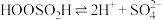 。
。
由此可判断,该条件下的 值为
值为__________ (填“ ”“
”“ ”或“
”或“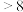 ”);请写出该过程中
”);请写出该过程中 与
与 总反应的离子方程式:
总反应的离子方程式:____________ 。
(2) 与
与 水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:
水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:
Ⅰ.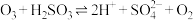 ;
;
Ⅱ. ;
;
Ⅲ.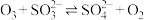 。
。
在含硫微粒总的物质的量为 的
的 水溶液中加入适量
水溶液中加入适量 固体,再通入
固体,再通入 ,反应一段时间后,测得
,反应一段时间后,测得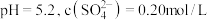 ,则
,则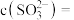
____________ (保留两位有效数字,请写出计算过程)。
(3)科学家最近发现了一种利用水催化促进硫酸盐形成的化学新机制,如图所示: 或
或 可以将电子快速转移到周围的气相
可以将电子快速转移到周围的气相 分子。观察图示可知“水分子桥”主要靠
分子。观察图示可知“水分子桥”主要靠________________ 形成;写出 与
与 间发生的总反应的离子方程式:
间发生的总反应的离子方程式:____________________ 。
②事实上,上述机理只能解释酸雨等现象的形成,却不能解释雾霾中固体硫酸盐小颗粒的存在。进一步研究发现,氨气在雾霾的形成过程中也起到了重要作用,其作用可能是________________ 。
 )气溶胶是雾霾的主要成分,主要通过
)气溶胶是雾霾的主要成分,主要通过 转化产生。不同
转化产生。不同 条件下
条件下 在水溶液中的主要存在形态及其对应的物质的量分数如图所示:
在水溶液中的主要存在形态及其对应的物质的量分数如图所示: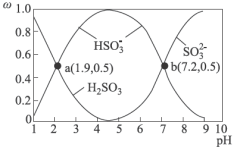
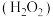 是大气中重要的氧化剂,其有多种途径将
是大气中重要的氧化剂,其有多种途径将 氧化成硫酸盐。
氧化成硫酸盐。①
 可在催化剂
可在催化剂 或
或 的作用下产生
的作用下产生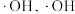 能将
能将 氧化。
氧化。 产生的机理如下:
产生的机理如下:反应Ⅰ:
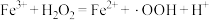 (慢反应);
(慢反应);反应Ⅱ:
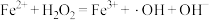 (快反应).
(快反应).下列说法正确的是
A.反应涉及非极性键的断裂与形成
B.反应Ⅰ的活化能大于反应Ⅱ
C.向固定容积的反应体系中充入氦气,
 氧化
氧化 的反应速率加快
的反应速率加快D.与
 作催化剂相比,相同条件下
作催化剂相比,相同条件下 作催化剂时
作催化剂时 氧化效率可能更高
氧化效率可能更高②研究表明
 与
与 水溶液的反应机理如下:
水溶液的反应机理如下:Ⅰ.
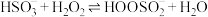 ;
;Ⅱ.
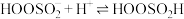 ;
;Ⅲ.
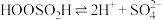 。
。由此可判断,该条件下的
 值为
值为 ”“
”“ ”或“
”或“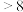 ”);请写出该过程中
”);请写出该过程中 与
与 总反应的离子方程式:
总反应的离子方程式:(2)
 与
与 水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:
水溶液的反应是硫酸盐产生的另一个重要途径.主要反应如下:Ⅰ.
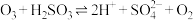 ;
;Ⅱ.
 ;
;Ⅲ.
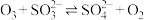 。
。在含硫微粒总的物质的量为
 的
的 水溶液中加入适量
水溶液中加入适量 固体,再通入
固体,再通入 ,反应一段时间后,测得
,反应一段时间后,测得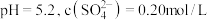 ,则
,则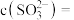
(3)科学家最近发现了一种利用水催化促进硫酸盐形成的化学新机制,如图所示:
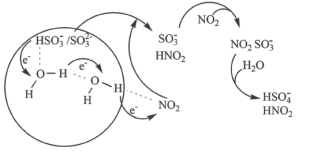
 或
或 可以将电子快速转移到周围的气相
可以将电子快速转移到周围的气相 分子。观察图示可知“水分子桥”主要靠
分子。观察图示可知“水分子桥”主要靠 与
与 间发生的总反应的离子方程式:
间发生的总反应的离子方程式:②事实上,上述机理只能解释酸雨等现象的形成,却不能解释雾霾中固体硫酸盐小颗粒的存在。进一步研究发现,氨气在雾霾的形成过程中也起到了重要作用,其作用可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】本次亚运会火炬燃料甲醇是利用焦炉气中的氢气(H2)与从工业尾气中捕集的二氧化碳(CO2)合成,并由远程甲醇动力重卡提供运输保障。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
Ⅰ.
Ⅱ.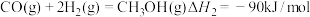
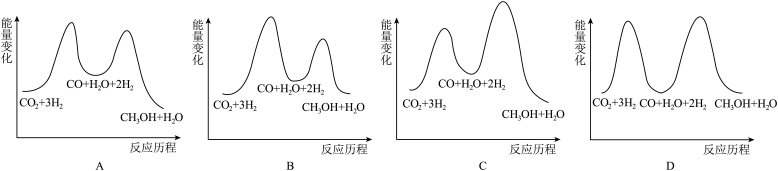
若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
(2)甲醇可作为燃料使用,下图是一个电化学过程的装置示意图。
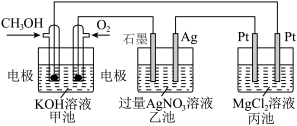
①甲池中通入 的电极电极反应方程式为
的电极电极反应方程式为___________ 。
②丙池中总反应的离子方程式为___________ 。
③当乙池中Ag极的质量增加1.08g时,甲池中理论上消耗
___________  (标准状况)。
(标准状况)。
(3)回收并利用 一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化
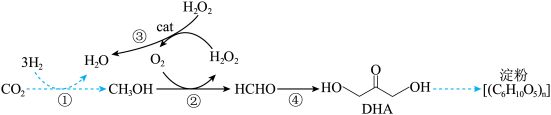
一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设
合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设 为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
(4)利用两种金属催化剂,在水溶液体系中将 分别转化为
分别转化为 和
和 的反应过程示意图如图所示。
的反应过程示意图如图所示。
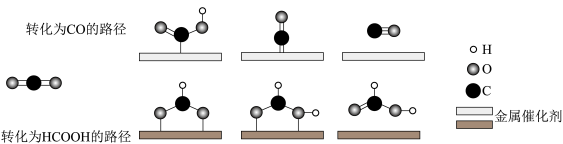
下列说法错误的是___________(填标号)。
(1)二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:Ⅰ.

Ⅱ.
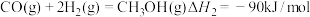
若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是

(2)甲醇可作为燃料使用,下图是一个电化学过程的装置示意图。

①甲池中通入
 的电极电极反应方程式为
的电极电极反应方程式为②丙池中总反应的离子方程式为
③当乙池中Ag极的质量增加1.08g时,甲池中理论上消耗

 (标准状况)。
(标准状况)。(3)回收并利用
 一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化
一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设
合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设 为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
A.反应①中消耗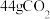 ,转移电子数为 ,转移电子数为 |
| B.淀粉与纤维素的分子式相同,互为同分异构体 |
C. 与 与 的混合物中所含氧原子数为 的混合物中所含氧原子数为 |
D.反应③中cat为催化剂,实验室常用 催化该反应 催化该反应 |
(4)利用两种金属催化剂,在水溶液体系中将
 分别转化为
分别转化为 和
和 的反应过程示意图如图所示。
的反应过程示意图如图所示。
下列说法错误的是___________(填标号)。
A.在转化为 的路径中,只涉及碳氧键的断裂和氧氢键的形成 的路径中,只涉及碳氧键的断裂和氧氢键的形成 |
B.在转化为 的路径中, 的路径中, 被氧化为 被氧化为 |
| C.两个转化路径均无非极性键的形成 |
| D.上述反应过程说明催化剂具有选择性 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,一实验小组欲通过图1装置探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

(1)该反应中MnO4-被还原为Mn2+,写出相应反应的离子方程式:___ 。
(2)该实验探究的是___ 因素对化学反应速率的影响。针筒内收集相同体积的CO2,所用时间是①__ ②(填“>”、“<”或“=”)。
(3)本实验还可通过测定___ 来比较化学反应速率。
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变化的主要原因可能是___ 。
(5)图3中阴影部分“面积”还可以表示t1~t3时间内___ 。(填字母)
A.c(Mn2+)的增加量 B.n(Mn2+)的增加量
C.c(SO42-)的增加量 D.c(MnO4-)的增加量
| 实验序号 | A溶液 | B溶液 |
① | 20mL 0.1mol/L H2C2O4溶液 | 30mL 0.1mol/L KMnO4溶液 |
② | 20mL 0.2mol/L H2C2O4溶液 | 30mL 0.1mol/L KMnO4溶液 |

(1)该反应中MnO4-被还原为Mn2+,写出相应反应的离子方程式:
(2)该实验探究的是
(3)本实验还可通过测定
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变化的主要原因可能是
(5)图3中阴影部分“面积”还可以表示t1~t3时间内
A.c(Mn2+)的增加量 B.n(Mn2+)的增加量
C.c(SO42-)的增加量 D.c(MnO4-)的增加量
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段(指①0~1、②1~2、③2~3、④3~4、⑤4~5min,下同)反应速率最大 ______ (填序号,下同),原因是 ____________________________________________ .
(2)哪一段时段的反应速率最小______ ,原因是 _____________________________________ .
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,不要求写出计算过程)______________________________________________________________________ .
(4).如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列试剂: A..蒸馏水 B.KNO3溶液 C.NaCl溶液 D.CuSO4溶液
你认为可行的是(填编号)________________________________________ .
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
(2)哪一段时段的反应速率最小
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,不要求写出计算过程)
(4).如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列试剂: A..蒸馏水 B.KNO3溶液 C.NaCl溶液 D.CuSO4溶液
你认为可行的是(填编号)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】I.某实验小组利用压强传感器,数据采集器和计算机等数字化实验设备组成数据采集系统,探究外界条件对双氧水分解速率的影响。实验装置(下图)和所完成实验编号如下。请回答下列问题。
资料显示:通常情况下, 较稳定,不易分解。
较稳定,不易分解。
实验药品: 、
、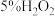 、
、 、
、

(1)用化学方程式表示实验原理_______ 。
(2)编号①和②的实验目的是_______ 。
(3)编号③④⑤探究的是不同催化剂条件下双氧水的分解速率,实验结果如图所示。说明图中曲线的含义_______ 。结合实验条件,分析三条曲线的区别_______ 。

Ⅱ.近期,我国科学家在实验室中成功用二氧化碳合成了淀粉,反应速率大小是评价该研究成果的重要依据。为探究影响反应速率的因素,某同学在实验室中寻找合适试剂进行实验。

(4)为比较 和
和 对
对 分解的催化效果,设计了以下实验:
分解的催化效果,设计了以下实验:
若该实验中反应速率①>②,能否说明 对
对 分解的催化效果一定比
分解的催化效果一定比 好,给出你的判断并简要说明理由
好,给出你的判断并简要说明理由_______ 。
(5)丙酮的碘代反应 的速率方程为
的速率方程为 (其中v为反应速率,k为速率常数,
(其中v为反应速率,k为速率常数,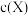 为反应物X的浓度),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为
为反应物X的浓度),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为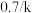 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示:
①该反应的速率常数k的数值为_______ 。
②在过量的 存在时,反应掉
存在时,反应掉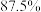 的
的 所需的时间是
所需的时间是_______  。
。
资料显示:通常情况下,
 较稳定,不易分解。
较稳定,不易分解。实验药品:
 、
、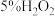 、
、 、
、

| 实验编号 | 实验药品 | 催化剂 |
| ① |  溶液 溶液 |  |
| ② |  溶液 溶液 |  |
| ③ |  溶液 溶液 | 无催化剂 |
| ④ |  溶液 溶液 |  |
| ⑤ |  溶液 溶液 |  |
(2)编号①和②的实验目的是
(3)编号③④⑤探究的是不同催化剂条件下双氧水的分解速率,实验结果如图所示。说明图中曲线的含义

Ⅱ.近期,我国科学家在实验室中成功用二氧化碳合成了淀粉,反应速率大小是评价该研究成果的重要依据。为探究影响反应速率的因素,某同学在实验室中寻找合适试剂进行实验。

(4)为比较
 和
和 对
对 分解的催化效果,设计了以下实验:
分解的催化效果,设计了以下实验:若该实验中反应速率①>②,能否说明
 对
对 分解的催化效果一定比
分解的催化效果一定比 好,给出你的判断并简要说明理由
好,给出你的判断并简要说明理由(5)丙酮的碘代反应
 的速率方程为
的速率方程为 (其中v为反应速率,k为速率常数,
(其中v为反应速率,k为速率常数,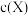 为反应物X的浓度),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为
为反应物X的浓度),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为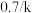 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示: |  |  |
| 0.25 | 0.050 | 1.4 |
| 0.50 | 0.050 | 2.8 |
| 1.00 | 0.050 | 5.6 |
| 0.50 | 0.10 | 2.8 |
②在过量的
 存在时,反应掉
存在时,反应掉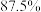 的
的 所需的时间是
所需的时间是 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】铋及其化合物在工业生产中用途广泛,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3、SiO2等杂质)制备铋酸钠,其流程如下:

已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
回答下列问题:(1)“浸取”时,为了提高浸取速率,可采取的措施有______ (任写一条);过滤1的滤渣中的某种主要成分可溶于一种弱酸,写出该反应的化学方程式______ 。
(2)浸取时加入过量浓盐酸的目的是______ ;“母液”中通入气体X后可循环利用,气体X为______ (填名称)。
(3)写出焙烧时生成铋酸钠的化学方程式______ 。
(4)用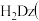 双硫腙,二元弱酸
双硫腙,二元弱酸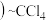 络合萃取法可从工业废水中提取金属离子:
络合萃取法可从工业废水中提取金属离子: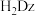 先将金属离子络合成电中性的物质
先将金属离子络合成电中性的物质 如
如 等
等 ,再用
,再用 萃取此络合物。图2是用上述方法处理含有
萃取此络合物。图2是用上述方法处理含有 、
、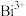 、
、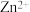 的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
①当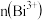 :
: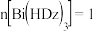 :4时,废水的
:4时,废水的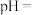
______ 。
②向萃取后的 中加入足量的NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为
中加入足量的NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为___ 。
(5)取焙烧得到的 样品
样品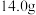 ,加入稀硫酸和
,加入稀硫酸和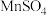 溶液使其完全溶解。已知
溶液使其完全溶解。已知 被还原为
被还原为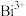 ,
,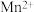 被氧化成成
被氧化成成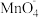 ,试写出该反应的离子方程式:
,试写出该反应的离子方程式:____ 。然后用新配制的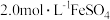 溶液对生成的
溶液对生成的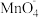 进行滴定,滴定完成后稍耗
进行滴定,滴定完成后稍耗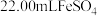 溶液。则该样品中
溶液。则该样品中 纯度为
纯度为____ 。

已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
回答下列问题:(1)“浸取”时,为了提高浸取速率,可采取的措施有
(2)浸取时加入过量浓盐酸的目的是
(3)写出焙烧时生成铋酸钠的化学方程式
(4)用
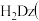 双硫腙,二元弱酸
双硫腙,二元弱酸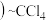 络合萃取法可从工业废水中提取金属离子:
络合萃取法可从工业废水中提取金属离子: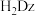 先将金属离子络合成电中性的物质
先将金属离子络合成电中性的物质 如
如 等
等 ,再用
,再用 萃取此络合物。图2是用上述方法处理含有
萃取此络合物。图2是用上述方法处理含有 、
、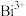 、
、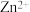 的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率)。
①当
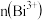 :
: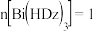 :4时,废水的
:4时,废水的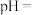
②向萃取后的
 中加入足量的NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为
中加入足量的NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为(5)取焙烧得到的
 样品
样品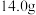 ,加入稀硫酸和
,加入稀硫酸和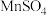 溶液使其完全溶解。已知
溶液使其完全溶解。已知 被还原为
被还原为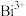 ,
,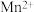 被氧化成成
被氧化成成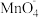 ,试写出该反应的离子方程式:
,试写出该反应的离子方程式: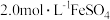 溶液对生成的
溶液对生成的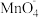 进行滴定,滴定完成后稍耗
进行滴定,滴定完成后稍耗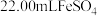 溶液。则该样品中
溶液。则该样品中 纯度为
纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】硫代硫酸钠俗称大苏打、海波,主要用作照相业定影剂,还广泛应用于鞣革、媒染、化工、医药等行业。常温下,溶液中析出晶体为Na2S2O3•5H2O.Na2S2O3•5H2O于40-45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如图甲所示。

Ⅰ.制备Na2S2O3•5H2O
将硫化钠和碳酸钠按反应要求比例放入图乙装置D中,然后注入150mL蒸馏水使其溶解,再在分液漏斗A中注入一定浓度的H2SO4,在蒸馏烧瓶B中加入亚硫酸钠固体,并按图乙安装好装置。
(1)仪器D的名称为______
(2)打开分液漏斗活塞,注入H2SO4,使反应产生的气体较缓慢均匀地通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,总反应方程式为2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2。
3Na2S2O3+CO2。
①烧瓶B中发生反应的化学方程式为______ 。
②将B中产生的气体缓慢均匀地通入D中的正确操作是______ 。
③制备过程中仪器D中的溶液要控制在弱碱性条件下,其理由是______ (用离子方程式表示)。
Ⅱ.分离Na2S2O3•5H2O并测定含量

(3)操作I为趁热过滤,其目的是______ ;操作Ⅱ是过滤、洗涤、干燥,其中洗涤操作时用______ (填试剂)作洗涤剂。
(4)蒸发浓缩滤液直至溶液中有少量晶体析出为止,蒸发时控制温度不宜过高的原因是______ 。
(5)制得的粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3•5H2O的含量,称取1.25g的粗样品溶于水,配成250mL溶液,取25.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.0100mol/L标准I2溶液滴定,当溶液中S2O32-全部被氧化时,消耗碘溶液的体积为25.00mL.试回答:(提示:I2+2S2O32-═2I-+S4O62-)
①达到滴定终点时的现象:______
②产品中Na2S2O3•5H2O的质量分数为______ 。

Ⅰ.制备Na2S2O3•5H2O
将硫化钠和碳酸钠按反应要求比例放入图乙装置D中,然后注入150mL蒸馏水使其溶解,再在分液漏斗A中注入一定浓度的H2SO4,在蒸馏烧瓶B中加入亚硫酸钠固体,并按图乙安装好装置。
(1)仪器D的名称为
(2)打开分液漏斗活塞,注入H2SO4,使反应产生的气体较缓慢均匀地通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,总反应方程式为2Na2S+Na2CO3+4SO2
 3Na2S2O3+CO2。
3Na2S2O3+CO2。①烧瓶B中发生反应的化学方程式为
②将B中产生的气体缓慢均匀地通入D中的正确操作是
③制备过程中仪器D中的溶液要控制在弱碱性条件下,其理由是
Ⅱ.分离Na2S2O3•5H2O并测定含量

(3)操作I为趁热过滤,其目的是
(4)蒸发浓缩滤液直至溶液中有少量晶体析出为止,蒸发时控制温度不宜过高的原因是
(5)制得的粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3•5H2O的含量,称取1.25g的粗样品溶于水,配成250mL溶液,取25.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.0100mol/L标准I2溶液滴定,当溶液中S2O32-全部被氧化时,消耗碘溶液的体积为25.00mL.试回答:(提示:I2+2S2O32-═2I-+S4O62-)
①达到滴定终点时的现象:
②产品中Na2S2O3•5H2O的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】Ƴ-Fe2O3是一种具有磁性、催化等作用的纳米材料,以硫铁矿烧渣等为原料生产制备Ƴ-Fe2O3的流程如下:

已知:“还原焙烧”的主要反应为:3C+2O2 3CO↑+CO2↑,Fe2O3+CO
3CO↑+CO2↑,Fe2O3+CO 2FeO + CO2
2FeO + CO2
回答下列问题:
(1)“浸取”前需将焙烧生成的混合物粉碎,其目的是_____________________ 。
(2)“滤渣1”除了CaSO4外还有_______________ 。
(3)常温下Ksp[Al(OH)3]=1.3×10-33。当常温下溶液pH=6时,c(Al3+)=____________ 。
(4)“过滤2”时需用蒸馏水洗涤,能证明已洗涤干净的方法是______________ ;
(5)沉淀缓慢氧化为铁黄的化学方程式为_____________________ 。

已知:“还原焙烧”的主要反应为:3C+2O2
 3CO↑+CO2↑,Fe2O3+CO
3CO↑+CO2↑,Fe2O3+CO 2FeO + CO2
2FeO + CO2回答下列问题:
(1)“浸取”前需将焙烧生成的混合物粉碎,其目的是
(2)“滤渣1”除了CaSO4外还有
(3)常温下Ksp[Al(OH)3]=1.3×10-33。当常温下溶液pH=6时,c(Al3+)=
(4)“过滤2”时需用蒸馏水洗涤,能证明已洗涤干净的方法是
(5)沉淀缓慢氧化为铁黄的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】已知硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)可溶于水,在100℃~110℃时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
I.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是_________ ,由此可知分解产物中有________ (填化学式)。
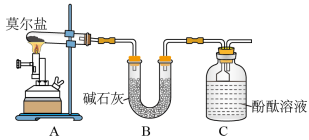
(2)乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
D. 品红溶液 E.NaOH溶液
E.NaOH溶液 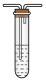 F.BaCl2溶液和足量盐酸
F.BaCl2溶液和足量盐酸 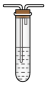 G.排水集气法
G.排水集气法 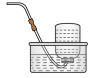 H. 安全瓶
H. 安全瓶
①乙同学的实验中,装置依次连按的合理顺序为:A→H→( ) →( ) →( ) →G。
②证明含有SO3的实验现象是__________ ;安全瓶H的作用是___________ 。
II.为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成500mL溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取25.00mL样品溶液用0.1000mol/L的酸性K2Cr2O7溶液分三次进行滴定。
乙方案(通过NH4+测定):实验设计装置如图所示。取25.00mL样品溶液进行该实验。
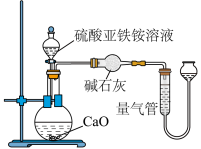
请回答:
(1)甲方案中的离子方程式为___________ 。
(2)乙方案中量气管中最佳试剂是__________ 。
a.水 b.饱和NaHCO3溶液 c.CCl4 d.饱和NaCl溶液
(3)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是_________ 。
(4)若测得NH3为VL(已折算为标准状况下),则硫酸亚铁铵纯度为____ (列出计算式)
I.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是

(2)乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
D. 品红溶液
 E.NaOH溶液
E.NaOH溶液  F.BaCl2溶液和足量盐酸
F.BaCl2溶液和足量盐酸  G.排水集气法
G.排水集气法  H. 安全瓶
H. 安全瓶
①乙同学的实验中,装置依次连按的合理顺序为:A→H→
②证明含有SO3的实验现象是
II.为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成500mL溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取25.00mL样品溶液用0.1000mol/L的酸性K2Cr2O7溶液分三次进行滴定。
乙方案(通过NH4+测定):实验设计装置如图所示。取25.00mL样品溶液进行该实验。

请回答:
(1)甲方案中的离子方程式为
(2)乙方案中量气管中最佳试剂是
a.水 b.饱和NaHCO3溶液 c.CCl4 d.饱和NaCl溶液
(3)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是
(4)若测得NH3为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】KMnO4是一种常用的氧化剂。某实验小组利用氯气氧化K2MnO4制备KMnO4并对其性质进行探究。
【KMnO4的制备】
(1)用下图装置制备KMnO4(加热和夹持装置已略去)_______ (填序号)。
A.NaOH溶液 B.饱和食盐水 C.饱和NaHCO3溶液
②C中发生反应的离子反应方程式有: ;还发生了
;还发生了_______ 。
【KMnO4的性质探究】
资料:
ⅰ. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成MnO2。
,在近中性条件下被还原成MnO2。
ⅱ.单质硫可溶于Na2S溶液,溶液呈淡黄色。
某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。
(2)①甲同学取实验I中少量溶液进行实验,检测有 ,得出S2-被氧化成
,得出S2-被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是_______ 。
②同学讨论后,设计了如下实验,证实该条件下 的确可以将S2-氧化成
的确可以将S2-氧化成 。
。_______ 。
b.连通后电流计指针偏转,一段时间后,取左侧烧杯中溶液,_______ ,(填操作、试剂和现象),证明:S2-被氧化成了 。
。
(3)实验I的现象生成棕褐色沉淀(MnO2)与资料ⅰ不相符,MnO2产生的原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是_______ 。
(4)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与_______ 等因素有关。
【KMnO4的制备】
(1)用下图装置制备KMnO4(加热和夹持装置已略去)

A.NaOH溶液 B.饱和食盐水 C.饱和NaHCO3溶液
②C中发生反应的离子反应方程式有:
 ;还发生了
;还发生了【KMnO4的性质探究】
资料:
ⅰ.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成MnO2。
,在近中性条件下被还原成MnO2。ⅱ.单质硫可溶于Na2S溶液,溶液呈淡黄色。
某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。
| 实验序号 | 实验过程 | 实验现象 |
| I |
| 紫色变浅( ),生成棕褐色沉淀(MnO2) ),生成棕褐色沉淀(MnO2) |
| II |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(2)①甲同学取实验I中少量溶液进行实验,检测有
 ,得出S2-被氧化成
,得出S2-被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将S2-氧化成
的确可以将S2-氧化成 。
。
b.连通后电流计指针偏转,一段时间后,取左侧烧杯中溶液,
 。
。(3)实验I的现象生成棕褐色沉淀(MnO2)与资料ⅰ不相符,MnO2产生的原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(4)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。

试根据题目要求,回答下列问题:
(1)若用铁粉和稀盐酸(盐酸具有挥发性)反应制取并收集干燥的氢气。
①制取并收集干燥的氢气所选仪器的连接顺序为 (填写仪器序号字母)。
②进行实验前,首先要做的一步工作是 。
(2)小明同学欲用一氧化碳气体(含少量二氧化碳和水蒸气)测定10克不纯氧化铜样品的纯度(杂质不参与反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:B1→C→D→B2。
①写出装置B1中发生反应的化学方程式 。
②装置D中观察到的实验现象是 。
③假设实验结束后,测得B2装置的质量比反应前增加了4.4克,由此推算出装置D中固体的质量减少了 克。
④小明同学的设计方案有一明显的不足,这样操作可能造成的后果是 。

试根据题目要求,回答下列问题:
(1)若用铁粉和稀盐酸(盐酸具有挥发性)反应制取并收集干燥的氢气。
①制取并收集干燥的氢气所选仪器的连接顺序为 (填写仪器序号字母)。
②进行实验前,首先要做的一步工作是 。
(2)小明同学欲用一氧化碳气体(含少量二氧化碳和水蒸气)测定10克不纯氧化铜样品的纯度(杂质不参与反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:B1→C→D→B2。
①写出装置B1中发生反应的化学方程式 。
②装置D中观察到的实验现象是 。
③假设实验结束后,测得B2装置的质量比反应前增加了4.4克,由此推算出装置D中固体的质量减少了 克。
④小明同学的设计方案有一明显的不足,这样操作可能造成的后果是 。
您最近一年使用:0次





