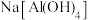名校
1 . 一定条件下,下列各组物质的转化关系能通过一步化学反应实现的是

选项 | X | Y | Z | W |
A |
|
|
|
|
B |
|
|
|
|
C |
|
|
|
|
D |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
101次组卷
|
2卷引用:河南省信阳高级中学2023-2024学年高一下学期期中教学质量检测化学试题
名校
解题方法
2 . 将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol/L的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示,下列说法错误的是

| A.根据关系图,硝酸被还原成铵盐 | B.样品中铝粉和铁粉的物质的量之比为l∶1 |
| C.a点对应NaOH溶液的体积为20mL | D.原溶液中硝酸的物质的量为0.37mol |
您最近一年使用:0次
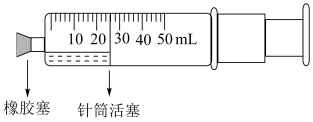
3 . 某化学社团利用注射器设计了NO与NO2相互转化的趣味实验,实验操作与现象记录如表:
(1)N在元素周期表中的位置为________________ 。
(2)在装入铜片与浓硝酸之前,对注射器需进行的操作是________________ 。
(3)步骤一中溶液呈绿色而非蓝色。甲同学认为是硝酸铜的质量分数较高所致,乙同学认为是溶解了NO2所致。同学们分别设计了以下4个实验来验证。这些方案中可行的是________。
(4)请分步写出步骤三涉及反应的化学方程式:________________ 。
(5)实验结束后吸入足量空气,充分反应,将废气、废液注入废液缸,废液缸内的试剂最好选用________。
(6)实验过程中,同学们注意到铜与浓硝酸反应的速率先慢后快;且实验前4min注射器内温度没有明显变化。同学们对此现象产生的原因做出如下假设:
①假设一:________________ (填化学式)对该反应有催化作用。
实验验证:向12 mol/L浓硝酸中加入少量 固体,重复步骤一的操作,活塞后移速度无明显变化。
固体,重复步骤一的操作,活塞后移速度无明显变化。
②假设二:NO2对该反应有催化作用。
实验验证:步骤一加入浓硝酸后,立即吸入少量NO2,继续步骤一的操作,活塞后移速度明显加快。
有同学还补充了对比实验:增大步骤一操作中硝酸的浓度,活塞后移速度无明显变化。补充对比实验的目的是________________________________________________ 。
③假设三:HNO2对该反应有催化作用。
某同学查阅资料,发现铜和浓硝酸反应会产生少量亚硝酸(HNO2)。
设计实验证明HNO2对铜和浓硝酸的反应有催化作用。操作和预期现象是________________ 。
实验结论:假设一不成立,假设二、三成立,NO2和HNO2都对铜和浓硝酸的反应有催化作用。
步骤 | 实验操作 | 实验现象 |
一 | 向注射器中加入两块铜片,吸取10mL 12mol/L的浓硝酸,塞紧橡胶塞。当针筒活塞后移至40mL刻度时,将注射器内所有液体排入废液缸 | 针筒活塞先缓慢后移,4min后迅速后移至40mL处。溶液变为绿色,产生红棕色气体 |
二 | 取下橡胶塞,缓慢吸取8mL蒸馏水,塞紧橡胶塞,轻摇注射器,观察现象 | 注射器内气体颜色由红棕色变为无色,活塞前移 |
三 | 取下橡胶塞,吸取少量空气,轻摇注射器,重复操作2~3次 | 吸取空气后,气体变为红棕色,晃动注射器,红棕色褪去 |
(1)N在元素周期表中的位置为
(2)在装入铜片与浓硝酸之前,对注射器需进行的操作是
(3)步骤一中溶液呈绿色而非蓝色。甲同学认为是硝酸铜的质量分数较高所致,乙同学认为是溶解了NO2所致。同学们分别设计了以下4个实验来验证。这些方案中可行的是________。
| A.加热绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
(4)请分步写出步骤三涉及反应的化学方程式:
(5)实验结束后吸入足量空气,充分反应,将废气、废液注入废液缸,废液缸内的试剂最好选用________。
| A.浓氨水 | B.NaOH溶液 | C.澄清石灰水 | D.稀硫酸 |
(6)实验过程中,同学们注意到铜与浓硝酸反应的速率先慢后快;且实验前4min注射器内温度没有明显变化。同学们对此现象产生的原因做出如下假设:
①假设一:
实验验证:向12 mol/L浓硝酸中加入少量
 固体,重复步骤一的操作,活塞后移速度无明显变化。
固体,重复步骤一的操作,活塞后移速度无明显变化。②假设二:NO2对该反应有催化作用。
实验验证:步骤一加入浓硝酸后,立即吸入少量NO2,继续步骤一的操作,活塞后移速度明显加快。
有同学还补充了对比实验:增大步骤一操作中硝酸的浓度,活塞后移速度无明显变化。补充对比实验的目的是
③假设三:HNO2对该反应有催化作用。
某同学查阅资料,发现铜和浓硝酸反应会产生少量亚硝酸(HNO2)。
设计实验证明HNO2对铜和浓硝酸的反应有催化作用。操作和预期现象是
实验结论:假设一不成立,假设二、三成立,NO2和HNO2都对铜和浓硝酸的反应有催化作用。
您最近一年使用:0次
4 . “价—类”二维图是将元素化合物的知识网络化的捷径,氮元素的“价—类”二维图如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是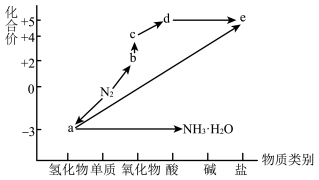
A.实验室制取气体 时可以用向上排空气法收集 时可以用向上排空气法收集 |
B.一定条件下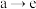 的反应能一步完成,且属于固氮反应 的反应能一步完成,且属于固氮反应 |
C.足量的铜和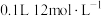 d的浓溶液反应,转移的电子数大于 d的浓溶液反应,转移的电子数大于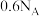 |
| D.气体a能使干燥的红色石蕊试纸变蓝 |
您最近一年使用:0次
5 . 在一定量的稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有 ),向反应后溶液中加入
),向反应后溶液中加入 溶液至沉淀完全,测得生成沉淀质量比原金属质量增加
溶液至沉淀完全,测得生成沉淀质量比原金属质量增加 ,则下列叙述正确的是
,则下列叙述正确的是
 ),向反应后溶液中加入
),向反应后溶液中加入 溶液至沉淀完全,测得生成沉淀质量比原金属质量增加
溶液至沉淀完全,测得生成沉淀质量比原金属质量增加 ,则下列叙述正确的是
,则下列叙述正确的是A.当金属全部溶解时,收集到标准状况下 |
B.当生成沉淀的量最多时,消耗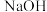 溶液体积一定为 溶液体积一定为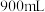 |
C.反应过程中消耗硝酸的物质的量为 |
D.参加反应的金属总质量可能为 |
您最近一年使用:0次
名校
6 . 将 9.2g 铜和铁的混合物放入一定体积的稀硝酸溶液中,充分反应后得到标准状况下1.12LNO ,有金属剩余;向所得溶液中继续加入足量的稀硫酸,金属完全溶解且又得到标准状况下1.12LNO 。若向反应后的溶液中加入 KSCN 溶液,溶液不变红,则下列说法中正确的是
| A.原混合物中铜和铁各 0.1mol |
| B.第一次剩余金属全部为铜 |
| C.反应后的溶液中溶质为硝酸亚铁和硝酸铜 |
| D.若向反应后的溶液中再加入足量稀硝酸,又可得到约标准状况下 0.37LNO |
您最近一年使用:0次
7 . 向100mL由稀 与稀
与稀 组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
 与稀
与稀 组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
组成的混合溶液中逐渐加入铁粉,加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示。下列说法错误的是
A.0A段的离子反应为 |
B.AB段的离子反应为 |
C.反应开始前溶液中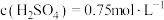 |
D.BC段的离子反应为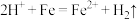 |
您最近一年使用:0次
名校
8 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.1mol 含有电子数为 含有电子数为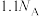 |
B.6.4gCu与0.1molS充分反应,转移电子数为 |
C.常温下,2.7g铝粉与足量浓硝酸反应,转移电子数为 |
D.1L 氨水中含有 氨水中含有 和 和 的数目之和为 的数目之和为 |
您最近一年使用:0次
名校
9 . 下列指定反应的离子方程式书写正确的是
A.NO2与水反应: |
B.氨水吸收足量SO2的反应: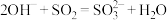 |
C.过量Fe和稀HNO3的反应: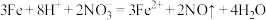 |
D.向 溶液中通入少量SO2: 溶液中通入少量SO2: |
您最近一年使用:0次
10 . 亚硝酸钠( )常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。
)常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。 是白色粉末,易溶于水。
是白色粉末,易溶于水。
(1)滴入浓硝酸前先通入一段时间的 ,目的是
,目的是___________ 。
(2)B中发生反应的化学方程式为___________ 、___________ 。
(3)C中试剂是___________ (填名称)。
(4)装置E的作用是___________ 。
(5)观察到F中溶液由紫红色变为无色,经检验氧化产物是 ,还原产物是
,还原产物是 。写出F中发生反应的离子方程式:
。写出F中发生反应的离子方程式:___________ 。
(6)实验结束后小组同学发现装置A中浓硝酸有剩余,溶液呈绿色,针对这一现象提出猜想。
查阅资料:
ⅰ. 溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
ⅱ. 与水反应时会有部分发生反应:
与水反应时会有部分发生反应: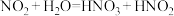 ,
, 是弱酸,无色,不稳定。
是弱酸,无色,不稳定。
ⅲ. 离子颜色为绿色。
离子颜色为绿色。
猜想1: 溶于浓硝酸,与蓝色
溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。
猜想2: 电离出的
电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。
①向浓硝酸中通入 ,溶液呈黄色,加入
,溶液呈黄色,加入___________ (填化学式)后呈绿色,证实猜想1合理。
②研究猜想2是否为所得溶液呈绿色的主要原因,实验如下。 的证据是
的证据是___________ 。
b.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想2不是实验Ⅰ所得溶液呈绿色的主要原因,说明理由:___________ 。
 )常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。
)常用作食品防腐剂,实验室常用NO和过氧化钠反应制得。 是白色粉末,易溶于水。
是白色粉末,易溶于水。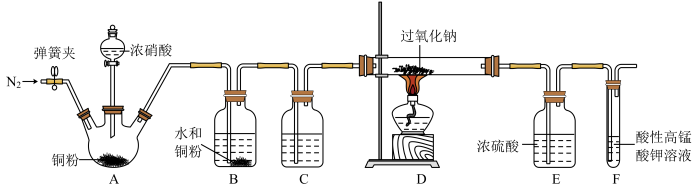
(1)滴入浓硝酸前先通入一段时间的
 ,目的是
,目的是(2)B中发生反应的化学方程式为
(3)C中试剂是
(4)装置E的作用是
(5)观察到F中溶液由紫红色变为无色,经检验氧化产物是
 ,还原产物是
,还原产物是 。写出F中发生反应的离子方程式:
。写出F中发生反应的离子方程式:(6)实验结束后小组同学发现装置A中浓硝酸有剩余,溶液呈绿色,针对这一现象提出猜想。
查阅资料:
ⅰ.
 溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;ⅱ.
 与水反应时会有部分发生反应:
与水反应时会有部分发生反应: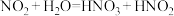 ,
, 是弱酸,无色,不稳定。
是弱酸,无色,不稳定。ⅲ.
 离子颜色为绿色。
离子颜色为绿色。猜想1:
 溶于浓硝酸,与蓝色
溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。猜想2:
 电离出的
电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。①向浓硝酸中通入
 ,溶液呈黄色,加入
,溶液呈黄色,加入②研究猜想2是否为所得溶液呈绿色的主要原因,实验如下。
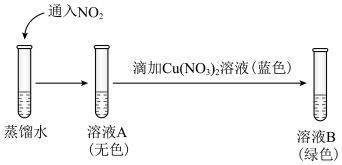
 的证据是
的证据是b.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想2不是实验Ⅰ所得溶液呈绿色的主要原因,说明理由:
您最近一年使用:0次