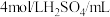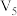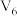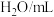名校
解题方法
1 . 在稀硫酸与锌制氢气实验中,为研究硫酸铜用量对氢气生成速率的影响,某同学设计了如下一系列实验。将表中6组溶液混合,分别加入到6个盛有过量的 粒(锌粒表面积均相同)的反应瓶中,记录相同时间产生的氢气的体积(见下图)。
粒(锌粒表面积均相同)的反应瓶中,记录相同时间产生的氢气的体积(见下图)。
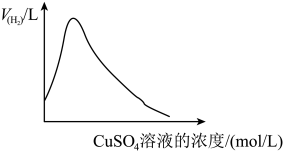
关于实验的说法中不正确的是
 粒(锌粒表面积均相同)的反应瓶中,记录相同时间产生的氢气的体积(见下图)。
粒(锌粒表面积均相同)的反应瓶中,记录相同时间产生的氢气的体积(见下图)。
实验组别 溶液 | A | B | C | D | E | F |
| 30 |
|
|
|
|
|
饱和 | 0 | 0.5 | 2.5 | 5 |
| 20 |
|
|
|
|
| 10 | 0 |
A.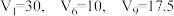 |
| B.实验中溶液蓝色逐渐变浅,可推测硫酸铜是该反应的催化剂 |
C.水的作用是控制溶液总体积,保证各组实验 的浓度相同 的浓度相同 |
D.当加入 溶液超过一定量时,生成氢气的速率反而会下降 溶液超过一定量时,生成氢气的速率反而会下降 |
您最近一年使用:0次
名校
2 . 某反应的反应机理可以分成如下两步,下列说法错误的是
| 反应机理 | 第一步反应 | 第二步反应 |
 (慢反应) (慢反应) | 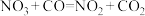 (快反应) (快反应) |
| A.在条件相同时,该反应的速率由第一步反应速率决定 |
| B.该反应的总反应方程式为NO2+CO=NO+CO2 |
| C.升高温度只会影响第一步反应速率,对第二步反应速率无影响 |
| D.加入合适的催化剂可降低反应的活化能,加快反应速率 |
您最近一年使用:0次
2024-01-01更新
|
144次组卷
|
12卷引用:安徽省A10联盟2022届高三上学期摸底考试化学试题
安徽省A10联盟2022届高三上学期摸底考试化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题陕西省宝鸡市金台区2021-2022学年高二上学期期中考试化学(理)试题(已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)2021年广东省高考化学试卷变式题11-21吉林省长春市第二十中学2021-2022学年高二上学期第一次质量检测化学试题湖北省武汉市部分学校2021-2022学年高二上学期12月联考化学试题四川省兴文第二中学校2023-2024学年高二上学期11月期中考试化学试题陕西省渭南市杜桥中学2023-2024学年高二上学期期中考试化学试卷 (已下线)专题02 化学反应速率-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
3 . 在下列四支试管中发生反应:2H2O2=2H2O+O2↑,产生O2速率最大是
| 试管 | 温度 | 过氧化氢的质量分数 | 催化剂 |
| A | 25℃ | 3% | 无 |
| B | 50℃ | 3% | 无 |
| C | 25℃ | 6% | 无 |
| D | 50℃ | 6% | 有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)硫代硫酸钠与稀硫酸反应的化学方程式为___________ 。
(2)该实验①、②可探究温度对反应速率的影响,因此V1=V2=___________ ,V3=___________ 。
(3)若V4=10.0,V5=6.0,则实验①、③可探究___________ 对反应速率的影响。
(4)可用热的NaOH浓溶液洗掉反应后试管中残余的固体。固体溶解时的离子方程式为___________ 。
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c (mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(2)该实验①、②可探究温度对反应速率的影响,因此V1=V2=
(3)若V4=10.0,V5=6.0,则实验①、③可探究
(4)可用热的NaOH浓溶液洗掉反应后试管中残余的固体。固体溶解时的离子方程式为
您最近一年使用:0次
13-14高一下·山东济宁·阶段练习
名校
解题方法
5 . 在C(s)+CO2(g)=2CO(g)的反应中,其他条件不变的情况下,现采取下列措施:①缩小体积,增大压强 ②增加碳的量 ③恒容下通入CO2 ④恒容下充入N2 ⑤恒压下充入N2,上述能够使反应速率增大的措施是
| A.①④ | B.②③⑤ | C.①③ | D.①②④ |
您最近一年使用:0次
2023-06-27更新
|
457次组卷
|
67卷引用:黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题
黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题河北省张家口市宣化一中2020-2021学年高一下学期期初考试化学试题江苏省沭阳县修远中学2020-2021学年高一下学期第一次月考化学试题(已下线)第2章 化学反应与能量(培优提升卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)广西钦州市浦北县浦北中学2020-2021学年高二3月月考化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 易错疑难集训(一)甘肃省永昌县第一高级中学2020-2021学年高一下学期期末考试化学试题江苏省连云港市赣榆智贤中学2021-2022学年高二上学期第一次月考化学试题吉林省长春北师大附属学校2021-2022学年高二上学期第一次月考化学试题山西省大同市平城中学校2021-2022学年高二上学期10月月考化学试卷天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题(已下线)2013-2014山东省济宁市汶上一中高一5月质量检测化学试卷2015-2016学年山西省怀仁一中高一下第三次月考化学试卷2015-2016学年内蒙古包头九中高一6月月考化学试卷(已下线)同步君 人教版 选修4 第2章 第2节 影响化学反应速率的因素2016-2017学年天津市静海一中高二上9月调研化学试卷(已下线)同步君 必修2 第2章 第3节 化学反应速率内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题湖北省宜昌市七校教学协作体2016-2017学年高二下学期期末考试化学试题黑龙江省大庆中学2016-2017学年高一下学期期末考试化学试题山西省怀仁县第一中学(两校区)2016-2017学年高一下学期期末考试化学试题(已下线)2.2 影响化学反应速率的因素山西省忻州市第一中学2016-2017学年高一下学期期末补考化学试题黑龙江省饶河县高级中学2017-2018学年高二上学期第一次月考化学试题高中化学人教版 必修2 第二章 化学反应与能量 第三节 化学反应的速率和限度 化学反应速率高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第二节 影响化学反应速率的因素 影响化学反应速率的因素河南省三门峡市2017-2018学年高二上学期期末考试化学试题广东省揭西县河婆中学2018-2019学年高二上学期期中考试化学试题湖北省黄州中学2018-2019学年高二下学期5月月考化学试题山西省运城市永济中学2019-2020学年高二上学期开学考试化学试题黑龙江省大庆市铁人中学2019-2020学年高二上学期9月月考化学试题广东省蕉岭县蕉岭中学2019-2020学年高二上学期第一次段考化学试题江西省上饶市“山江湖”协作体2019-2020学年高二上学期期中化学(统招班)试题江西省上饶中学2019-2020学年高二上学期期中考试(实验、重点班)化学试题第二节 化学反应的速率与限度 易错疑难集训(二)——A学习区 夯实基础(人教版(2019)第二册)第二章 化学反应与能量 易错疑难集训(二)——A学习区 夯实基础(人教版必修2)专题2 化学反应与能量转化 易错疑难集训(一)——A学习区 夯实基础(苏教版必修2)吉林省辽源市田家炳高级中学2019-2020学年高一下学期期中考试化学试题必修第二册RJ第6章易错疑难集训(二)福建省福州市罗源第一中学2020-2021学年高二上学期10月月考化学试题福建省长泰县第一中学2020-2021学年高二上学期期中考试化学试题安徽省桐城中学2020-2021学年高一上学期12月月考化学试题辽宁省大连市普兰店第二中学2020-2021学年高二上学期期中考试化学试题天津市新华中学2020-2021学年高二上学期第一次月考化学试题甘肃省天水市秦安县第一中学2021-2022学年高一下学期期中考试化学试题 (已下线)6.2.1 化学反应的速率-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)【期末复习】必刷题(2)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)吉林省长春市第二实验中学 2021-2022 学年高一下学期期中考试化学试题湖北省武汉市华中师范大学第一附属中学2021-2022学年高一下学期期中考试化学试题安徽省亳州市第二中学2021-2022学年高一下学期期末考试化学试题(已下线)2.1.2 影响化学反应速率的因素 活化能 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)云南省砚山县第二高级中学2021-2022学年高二下学期期中(4月)考试化学试题广东省珠海市第二中学2022-2023学年高二上学期10月月考化学试题湖南省衡阳市田家炳实验中学2022-2023学年高二上学期9月月考化学试题广东省深圳实验学校高中部2022-2023学年高二上学期第一阶段考试化学试题黑龙江省哈尔滨市第一二二中学2021-2022学年高一下学期期末考试化学试题北京市第一六一中学2022-2023学年高一下学期期中考试化学试题甘肃省天水市秦安县第一中学2022-2023学年高一下学期4月期中化学试题山东菏泽市曹县一中2022-2023学年高一下学期5月月考化学试题江西省景德镇市2022-2023学年高一下学期6月期末考试化学试题吉林省“BEST合作体”2022-2023学年高一下学期期末联考化学试题陕西省延安中学新2022-2023学年高一下学期6月月考化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高一下学期期末考试化学试题(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题河北省石家庄市辛集市2023-2024学年高二上学期2月期末考试化学试题江苏省扬州市广陵区红桥高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
6 . 某含硫酸的酸性工业废水中含有 。光照下,草酸(化学式为
。光照下,草酸(化学式为 ,是二元弱酸)能将其中的
,是二元弱酸)能将其中的 转化为
转化为 。某课题组研究发现,少量铁明矾
。某课题组研究发现,少量铁明矾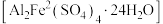 即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在
即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在 下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始
下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始 和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。
和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。
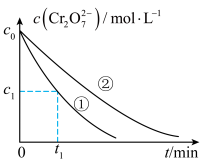
测得实验①和②溶液中的 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
(1)写出草酸与重铬酸钾反应的离子方程式:_______ 。
(2)
_______ ,
_______ ,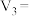
_______ 。
(3)实验①和②的结果表明_______ 。
(4)实验①中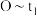 时段反应速率
时段反应速率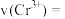
_______  (用代数式表示)。
(用代数式表示)。
 。光照下,草酸(化学式为
。光照下,草酸(化学式为 ,是二元弱酸)能将其中的
,是二元弱酸)能将其中的 转化为
转化为 。某课题组研究发现,少量铁明矾
。某课题组研究发现,少量铁明矾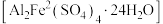 即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在
即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在 下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始
下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始 和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。
和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 |  | 30 |
| ③ | 5 |  | 20 |  |
 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
(1)写出草酸与重铬酸钾反应的离子方程式:
(2)


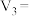
(3)实验①和②的结果表明
(4)实验①中
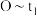 时段反应速率
时段反应速率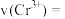
 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次
名校
7 .  是一种绿色试剂,在化学工业中用作生产过氧乙酸、亚氯酸钠等的原料,医药工业用作杀菌剂、消毒剂。某化学小组就探究双氧水的性质做了如下实验:
是一种绿色试剂,在化学工业中用作生产过氧乙酸、亚氯酸钠等的原料,医药工业用作杀菌剂、消毒剂。某化学小组就探究双氧水的性质做了如下实验:
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的数据。
研究小组在设计方案时,考虑了浓度、___________ 等因素对过氧化氢分解速率的影响。
(2)另一研究小组拟在同浓度 的催化下,探究双氧水浓度对
的催化下,探究双氧水浓度对 分解速率的影响,限选试剂与仪器:30%双氧水、
分解速率的影响,限选试剂与仪器:30%双氧水、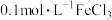 溶液、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
溶液、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
①设计实验方案:在不同 浓度下,测定
浓度下,测定___________ (要求所测得的数据能直体现反应速率大小)
②设计实验装置,完成图甲方框内的装置示意图________
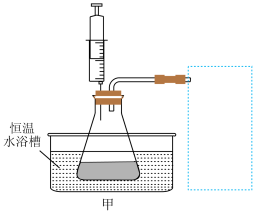
③参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据:数据用字母表示)。_______
(3)对于 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,研究小组的同学设计了如图乙所示的实验。请回答相关问题:
分解的催化效果,研究小组的同学设计了如图乙所示的实验。请回答相关问题:
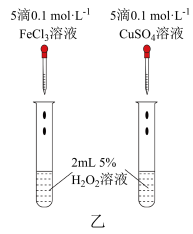
①可通过观察___________ ,比较得出结论。
②有同学提出将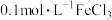 溶液改为
溶液改为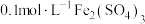 溶液更为合理,其理由是
溶液更为合理,其理由是___________ 。
 是一种绿色试剂,在化学工业中用作生产过氧乙酸、亚氯酸钠等的原料,医药工业用作杀菌剂、消毒剂。某化学小组就探究双氧水的性质做了如下实验:
是一种绿色试剂,在化学工业中用作生产过氧乙酸、亚氯酸钠等的原料,医药工业用作杀菌剂、消毒剂。某化学小组就探究双氧水的性质做了如下实验:(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的数据。
| 浓度 时间/s 反应条件 | 30%双氧水 | 15%双氧水 | 10%双氧水 | 5%双氧水 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几首不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
 、加热 、加热 | 10 | 25 | 60 | 120 |
(2)另一研究小组拟在同浓度
 的催化下,探究双氧水浓度对
的催化下,探究双氧水浓度对 分解速率的影响,限选试剂与仪器:30%双氧水、
分解速率的影响,限选试剂与仪器:30%双氧水、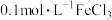 溶液、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
溶液、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器①设计实验方案:在不同
 浓度下,测定
浓度下,测定②设计实验装置,完成图甲方框内的装置示意图

③参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据:数据用字母表示)。
| 实验序号 | 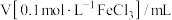 | … | |
| 1 | a | … | |
| 2 | a | … |
 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,研究小组的同学设计了如图乙所示的实验。请回答相关问题:
分解的催化效果,研究小组的同学设计了如图乙所示的实验。请回答相关问题:
①可通过观察
②有同学提出将
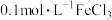 溶液改为
溶液改为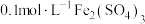 溶液更为合理,其理由是
溶液更为合理,其理由是
您最近一年使用:0次
名校
8 . 某学习小组测定锌粒与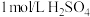 的反应速率,下列说法不正确的是
的反应速率,下列说法不正确的是
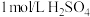 的反应速率,下列说法不正确的是
的反应速率,下列说法不正确的是A.增加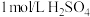 的用量,无法改变反应速率 的用量,无法改变反应速率 |
| B.改用浓硫酸,可以说明增大反应物浓度加快反应速率 |
C.可记录溶液中 随时间的变化(用pH计测定溶液的pH)来测量反应速率 随时间的变化(用pH计测定溶液的pH)来测量反应速率 |
| D.可选用等质量的锌片和锌粒与相同硫酸溶液反应,记录锌完全消失的时间,从而计算反应速率并说明固体表面积对反应速率的影响 |
您最近一年使用:0次
名校
解题方法
9 . 下列说法中正确的是
| A.0.1mol•L-1盐酸和0.1mol•L-1硫酸分别与2mol•L-1NaOH溶液反应,其反应速率相同 |
| B.相同质量的大理石块与大理石粉分别与0.1mol•L-1盐酸反应,反应速率相同 |
| C.Mg、Al在相同条件下分别与0.1mol•L-1盐酸反应,反应速率相同 |
| D.0.1mol•L-1HCl和0.1mol•L-1HNO3分别与相同形状和大小的大理石块反应,反应速率相同 |
您最近一年使用:0次
2023-01-31更新
|
982次组卷
|
11卷引用:(人教版2019)必修第二册 第六章 化学反应与能量 章末综合检测
(人教版2019)必修第二册 第六章 化学反应与能量 章末综合检测江苏省盐城市新洋高级中学2020-2021学年高一下学期第一次阶段测试化学试题河北省任丘一中2020-2021学年高一下学期第一次阶段考试化学试题云南省景谷一中2020-2021学年高一下学期6月月考化学试题山西省天镇县实验中学2021-2022学年高二上学期期中考试化学试题广西壮族自治区贺州市平桂高级中学(贺州市第五高级中学)2020-2021学年高二上学期第一次月考化学试题黑龙江省齐齐哈尔市第十六中学校2021-2022学年高一下学期期中考试化学试题 (已下线)6.2.1 化学反应速率及影响因素——同步学习必备知识第1课时 化学反应的速率1(已下线)热点06化学反应的速率和限度(已下线)专题06 化学反应的速率与限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
解题方法
10 . 近年来。研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。已知:SO2歧化反应的离子方程式:3SO2+2H2O=4H++2 +S↓
+S↓
(1)①I-可以作为水溶液中SO2歧化反应的催化剂,可能的歧化过程如下,将ii补充完整_______ 。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+______=_______+_______+2I-
②请用碰操理论解释:作为该反应的催化剂加快反应速率的原因_______ 。加入催化剂该反应的反应热_______ (填变大、变小、不变)
(2)探究i,ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和液加入到2mL下列试剂中,密闭放置观察现象(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=_______ 。
②比较A、B、C,可得出的结论是_______ 。
③实验表明,SO2的歧化反应速率:D>A。结合i,ii反应速率解释原因:_______ 。
 +S↓
+S↓(1)①I-可以作为水溶液中SO2歧化反应的催化剂,可能的歧化过程如下,将ii补充完整
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+______=_______+_______+2I-
②请用碰操理论解释:作为该反应的催化剂加快反应速率的原因
(2)探究i,ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和液加入到2mL下列试剂中,密闭放置观察现象(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.4mol•L-1KI | amol•L-1KI 0.2mol•L-1H2SO4 | 0.2mol•L-1H2SO4 | 0.2mol•L-1KI 0.0002mol•L-1I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,出现浑浊较A快 |
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率:D>A。结合i,ii反应速率解释原因:
您最近一年使用:0次