名校
解题方法
1 . 下列实验基本操作或实验应该注意的事项中,主要是从实验安全角度考虑的是
| A.实验剩余的药品不能放回原瓶 | B.在实验前进行实验装置气密性检查 |
| C.可燃性气体的验纯 | D.胶头滴管不能交叉使用 |
您最近一年使用:0次
2022-01-10更新
|
116次组卷
|
2卷引用:辽宁省辽河油田第一高级中学2021-2022学年高一(甲部)上学期11月考化学试题
名校
解题方法
2 . 下列有关实验操作的叙述合理的是
| A.用pH试纸测定溶液的pH时,不需要提前润湿 |
| B.中和反应反应热测定实验中,为防止溅出应将50mL 0.55mol/LNaOH分次缓慢倒入盛有50mL0.50mol/LHCl小烧杯中 |
C.可用如图装置测定过氧化氢分解反应的化学反应速率 |
| D.用pH试纸测定新配制氯水的pH值 |
您最近一年使用:0次
名校
3 . 自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。
I.下列A、B、C、D是中学常见的混合物分离或提纯的装置。
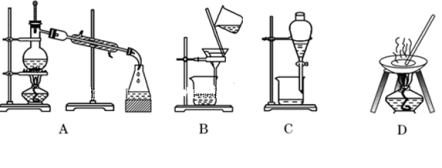
(1)请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
①碳酸钙悬浊液中分离出碳酸钙___________ ;
②氯化钠溶液中分离出氯化钠___________ ;
③分离植物油和水___________ ;
④分离酒精和水___________
Ⅱ.碘水中提取碘单质的方法如下:
(2)萃取分液
①下列可作为碘水中提取碘单质萃取剂的有___________ 。
A.酒精 B.苯
②分液漏斗在使用前必须先___________ 。
③已知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的___________ 端口放出,有机层应由分液漏斗的___________ 端口放出(此两问填“上”或者“下”)。
(3)蒸馏
①冷凝装置中冷凝水应该___________ 口进(填“上”或“下”)。
②已知碘和四氯化碳的熔沸点数据如表
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是___________ 。
I.下列A、B、C、D是中学常见的混合物分离或提纯的装置。

(1)请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
①碳酸钙悬浊液中分离出碳酸钙
②氯化钠溶液中分离出氯化钠
③分离植物油和水
④分离酒精和水
Ⅱ.碘水中提取碘单质的方法如下:
(2)萃取分液
①下列可作为碘水中提取碘单质萃取剂的有
A.酒精 B.苯
②分液漏斗在使用前必须先
③已知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的
(3)蒸馏
①冷凝装置中冷凝水应该
②已知碘和四氯化碳的熔沸点数据如表
| 物质 | 熔点 | 沸点 |
| 碘 | 113.7℃ | 184.3℃ |
| 四氯化碳 | −22.6℃ | 76.8℃ |
您最近一年使用:0次
2021-10-08更新
|
175次组卷
|
2卷引用:辽宁省辽河油田第一高级中学2021-2022学年高一(甲部)上学期11月考化学试题
4 . 下列图标表示实验中会产生有害气体,或产生烟、雾。应( )
A. | B. | C. | D. |
您最近一年使用:0次
5 . 50mL 0.50mol·L-1盐酸与50mL 0.55mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_______________ ,烧杯间填满碎泡沫塑料的作用是_________________ 。
(2)向盐酸中倒入NaOH溶液的正确操作是:________ 。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)大烧杯上如果不盖硬纸板,则求得的中和热________ (填“偏大”、“偏小”或“无影响”)。
(4)两次实验记录的数据如下表:
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18kJ/(℃·kg),各溶液的密度均为1g/cm3。则中和热ΔH=_________ kJ·mol-1。
(5)若改用60mL 0.50mol·L-1盐酸和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量_______ (填“相等”“不相等”),若实验操作均正确,则所求中和热__________ (填“相等”“不相等”)。

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)向盐酸中倒入NaOH溶液的正确操作是:
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)大烧杯上如果不盖硬纸板,则求得的中和热
(4)两次实验记录的数据如下表:
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | ΔH | |||
| ① | 50mL 0.55mol/L NaOH溶液 | 50mL 0.5mol/L HCl溶液 | 20℃ | 23.3℃ | |
| ② | 50mL 0.55mol/L NaOH溶液 | 50mL 0.5mol/L HCl溶液 | 20℃ | 23.4℃ | |
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18kJ/(℃·kg),各溶液的密度均为1g/cm3。则中和热ΔH=
(5)若改用60mL 0.50mol·L-1盐酸和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量
您最近一年使用:0次



