名校
解题方法
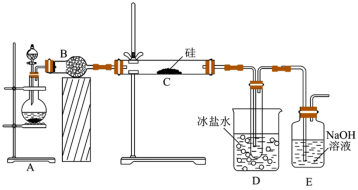
1 . 三氯硅烷(SiHCl3)可用于生产有机硅化合物、多晶硅。实验室先用NaCl固体与浓硫酸混合加热制取HCl,再利用HCl和硅粉制备三氯硅烷,实验装置如下图(加热仪器已略去)。回答下列问题: SiHCl3+H2
SiHCl3+H2
②三氯硅烷的熔点 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。
(1)装置B的名称_______ ,装置B中所装药品是_______ (填“碱石灰”或“无水氯化钙”)。
(2)加热前要先通一段时间HCl气体,原因是_______ 。
(3)装置D中冰盐水的作用是_______ 。
(4)该实验装置存在明显不足,请指出:_______ 。
(5)已知 在高温条件下易分解生成
在高温条件下易分解生成 和HCl。利用
和HCl。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图所示,写出该反应的化学方程式:
)的装置如图所示,写出该反应的化学方程式:_______ 。_______ (填序号)。
 SiHCl3+H2
SiHCl3+H2 ②三氯硅烷的熔点
 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。(1)装置B的名称
(2)加热前要先通一段时间HCl气体,原因是
(3)装置D中冰盐水的作用是
(4)该实验装置存在明显不足,请指出:
(5)已知
 在高温条件下易分解生成
在高温条件下易分解生成 和HCl。利用
和HCl。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图所示,写出该反应的化学方程式:
)的装置如图所示,写出该反应的化学方程式: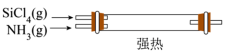
您最近半年使用:0次
2 . 过氧化钠常作漂白剂、杀菌剂、消毒剂,保存不当容易吸收空气中 而变质。
而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入___________ 溶液,若充分振荡后有白色沉淀,则证明 已经变质。
已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取 样品,并设计用如图装置来测定过氧化钠的质量分数。
样品,并设计用如图装置来测定过氧化钠的质量分数。___________ (填“是”或“否”);请写出 中发生的化学反应方程式
中发生的化学反应方程式___________ 。
②实验结束时,读取实验中生成气体的体积时,不合理的是___________ (填字母)。
A.直接读取气体体积,不需冷却到室温
B.上下移动量筒,使得 中液面高度相同
中液面高度相同
C.视线与凹液面的最低点相平读取量筒中水的体积
③读出量筒内水的体积后,折算成氧气的质量为 ,则样品中过氧化钠的质量分数为
,则样品中过氧化钠的质量分数为___________ (用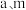 表示)。
表示)。
④实验完成后,E到F之间导管内残留水会使测量结果___________ (填“偏大”“偏小”或“不影响”)。
 而变质。
而变质。(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
 已经变质。
已经变质。(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取
 样品,并设计用如图装置来测定过氧化钠的质量分数。
样品,并设计用如图装置来测定过氧化钠的质量分数。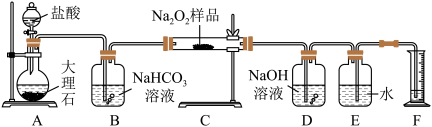
 中发生的化学反应方程式
中发生的化学反应方程式②实验结束时,读取实验中生成气体的体积时,不合理的是
A.直接读取气体体积,不需冷却到室温
B.上下移动量筒,使得
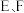 中液面高度相同
中液面高度相同C.视线与凹液面的最低点相平读取量筒中水的体积
③读出量筒内水的体积后,折算成氧气的质量为
 ,则样品中过氧化钠的质量分数为
,则样品中过氧化钠的质量分数为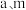 表示)。
表示)。④实验完成后,E到F之间导管内残留水会使测量结果
您最近半年使用:0次
3 . 磺化聚苯乙烯可用于制作高性能离子交换膜。某研究小组探究乙酰基磺酸 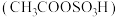 制备磺化聚苯乙烯的过程与效果。
制备磺化聚苯乙烯的过程与效果。
 .乙酰基磺酸的制备
.乙酰基磺酸的制备
向装有一定量二氯乙烷溶剂的烧杯中,加入 7.6 mL 乙酸酐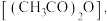 ,控制溶液温度在10℃以下,边搅拌边分批加入2.7 mL浓硫酸,得到乙酰基磺酸溶液。
,控制溶液温度在10℃以下,边搅拌边分批加入2.7 mL浓硫酸,得到乙酰基磺酸溶液。
(1)制备过程中需使用的玻璃仪器有烧杯、温度计、___________ 。
(2)控制溶液温度在10℃以下的目的是___________ 。
(3)乙酸酐与浓硫酸按物质的量之比1:1反应的化学方程式为___________ 。
 .聚苯乙烯的磺化
.聚苯乙烯的磺化
按如图装置(夹持设备略去),控制反应温度为65 ℃,缓慢滴加乙酰基磺酸溶液,得到浅棕色液体。将所得浅棕色液体慢慢滴入装有沸水的烧杯中,得到淡黄色的磺化聚苯乙烯颗粒,过滤、洗涤、干燥。___________ 进行加热。冷却水应从___________ (填“a” 或“b” ) 口通入。
(5)产品是否洗涤干净,可通过检测洗涤液中是否存在 来判断,检测的方法是
来判断,检测的方法是___________ 。
 .磺化度的测定
.磺化度的测定
称取0.500g干燥的磺化聚苯乙烯样品于锥形瓶,用苯-甲醇混合液溶解,以酚酞为指示剂,用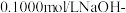 甲醇标准溶液滴定至终点,消耗标准液体积为10.00 mL, 计算磺化度。
甲醇标准溶液滴定至终点,消耗标准液体积为10.00 mL, 计算磺化度。
已知:i.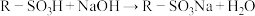 。
。
ii.聚苯乙烯链节的式量为104,磺化聚苯乙烯中含磺酸基链节的式量为184。
(6)该样品的磺化度=___________ (磺化度=含磺酸基链节数×100%)。
(7)若样品未充分干燥,将导致测得的磺化度___________ (填“偏高”“偏低”或“无影响”)。
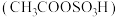 制备磺化聚苯乙烯的过程与效果。
制备磺化聚苯乙烯的过程与效果。 .乙酰基磺酸的制备
.乙酰基磺酸的制备向装有一定量二氯乙烷溶剂的烧杯中,加入 7.6 mL 乙酸酐
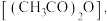 ,控制溶液温度在10℃以下,边搅拌边分批加入2.7 mL浓硫酸,得到乙酰基磺酸溶液。
,控制溶液温度在10℃以下,边搅拌边分批加入2.7 mL浓硫酸,得到乙酰基磺酸溶液。(1)制备过程中需使用的玻璃仪器有烧杯、温度计、
(2)控制溶液温度在10℃以下的目的是
(3)乙酸酐与浓硫酸按物质的量之比1:1反应的化学方程式为
 .聚苯乙烯的磺化
.聚苯乙烯的磺化按如图装置(夹持设备略去),控制反应温度为65 ℃,缓慢滴加乙酰基磺酸溶液,得到浅棕色液体。将所得浅棕色液体慢慢滴入装有沸水的烧杯中,得到淡黄色的磺化聚苯乙烯颗粒,过滤、洗涤、干燥。
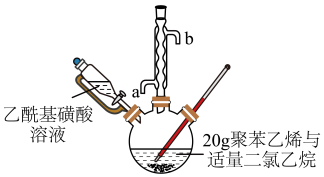
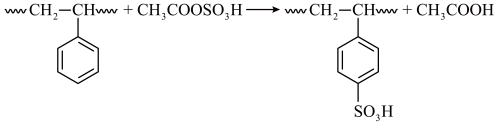
(5)产品是否洗涤干净,可通过检测洗涤液中是否存在
 来判断,检测的方法是
来判断,检测的方法是 .磺化度的测定
.磺化度的测定称取0.500g干燥的磺化聚苯乙烯样品于锥形瓶,用苯-甲醇混合液溶解,以酚酞为指示剂,用
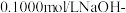 甲醇标准溶液滴定至终点,消耗标准液体积为10.00 mL, 计算磺化度。
甲醇标准溶液滴定至终点,消耗标准液体积为10.00 mL, 计算磺化度。已知:i.
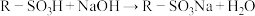 。
。ii.聚苯乙烯链节的式量为104,磺化聚苯乙烯中含磺酸基链节的式量为184。
(6)该样品的磺化度=
(7)若样品未充分干燥,将导致测得的磺化度
您最近半年使用:0次
2024·福建·模拟预测
解题方法
4 . 双氰胺( )为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮
)为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮 为原料制备双氰胺的流程如下:
为原料制备双氰胺的流程如下:


(1)已知:氰基是吸电子基团。氰氨
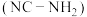 的碱性
的碱性(2)写出步骤Ⅰ的化学反应方程式:
(3)步骤Ⅱ中调节溶液pH为9.1,pH不能过低的原因:
(4)步骤Ⅲ中蒸发浓缩时,常采用真空蒸发浓缩,目的是
(5)凯氏定氮法是测定有机物中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐。
已知:
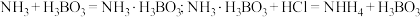

②仪器清洗后,g中加入硼酸
 和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭
和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭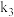 ,d中保留少量水。打开
,d中保留少量水。打开 ,加热b,使水蒸气进入e。d中保留少量水的目的是
,加热b,使水蒸气进入e。d中保留少量水的目的是③取双氰胺样品m克进行测定,滴定g中吸收液时消耗浓度为
 的盐酸VmL,则样品中氮的质量分数为
的盐酸VmL,则样品中氮的质量分数为
您最近半年使用:0次
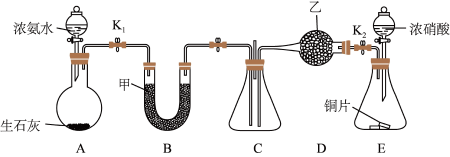
5 . 化学自主实验小组通过实验探究NH3、NO2的性质。
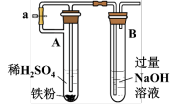
I.利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。___________ 。
(2)甲、乙分别是___________ (填字母)。
a.浓硫酸、碱石灰 b.五氧化二磷、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,预期C装置中能观察到的现象是___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
II.探究NO2、O2混合气体的喷泉实验。___________ (填字母)。
a.进气管短,出气管长 b.进气管长,出气管短 c.进气管、出气管等长
(6)G装置有多种作用,请任写出其中两种___________ 。
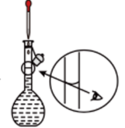
(7)常温常压下,G装置上的圆底烧瓶集满气体进行喷泉实验,若最终液体充满整个烧瓶,则所得溶液物质的量浓度为___________ mol·L-1(已知常温常压下气体摩尔体积为VL/mol)。
I.利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
(2)甲、乙分别是
a.浓硫酸、碱石灰 b.五氧化二磷、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,预期C装置中能观察到的现象是
(4)此实验装置存在一个明显的缺陷是
II.探究NO2、O2混合气体的喷泉实验。
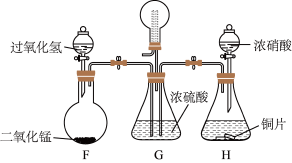
a.进气管短,出气管长 b.进气管长,出气管短 c.进气管、出气管等长
(6)G装置有多种作用,请任写出其中两种
(7)常温常压下,G装置上的圆底烧瓶集满气体进行喷泉实验,若最终液体充满整个烧瓶,则所得溶液物质的量浓度为
您最近半年使用:0次
2024-04-29更新
|
132次组卷
|
2卷引用:福建省福州九县(区、市)一中(高中)2023-2024学年高一下学期4月期中联考化学试题
名校
解题方法
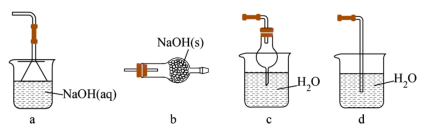
6 . 下列所选仪器和操作符合实验要求的是
| A | B | C | D |
|
|
|
|
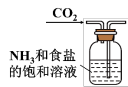
| 配制一定物质的量浓度的NaCl溶液 | 关闭止水夹a后能较长时间观察到白色Fe(OH)2沉淀 | 干燥氯气 | 制取NaHCO3 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-03更新
|
141次组卷
|
2卷引用:福建省泉州市泉港区第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . 菠菜中富含铁元素,用下列步骤完成铁元素的检验,各步选用的实验仪器不需要的是
| |
|
|
| A.将菠菜剪碎后研磨 | B.用蒸馏水溶解 | C.过滤得到滤液 | D.检验滤液中的Fe3+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-03更新
|
44次组卷
|
2卷引用:福建省泉州市泉港区第一中学2023-2024学年高一下学期3月月考化学试题
8 . 根据所学化学知识判断,下列做法错误的是
A.用 萃取溴水中的溴单质 萃取溴水中的溴单质 |
| B.温度计不慎打破,用硫粉处理散落的水银 |
| C.稀释浓硫酸时,需将水缓缓的倒入盛浓硫酸的烧杯中 |
D.用 溶液和红色石蕊试纸检验溶液中是否存在 溶液和红色石蕊试纸检验溶液中是否存在 |
您最近半年使用:0次
2024-04-01更新
|
44次组卷
|
2卷引用:福建省漳州市东山第二中学等校2023-2024学年高一上学期期中联考化学试题
9 . 下列实验方案设计正确的是
| A.用乙醇萃取碘水中的碘单质 |
B.用焰色反应鉴别NaCl和 |
C.用NaOH溶液、红色石蕊试纸可检验未知液中是否存在 |
| D.用过滤的方法分离植物油和水的混合物 |
您最近半年使用:0次
名校
解题方法
10 . 金属钒(V)广泛应用于化工生产领域,其化合物 是一种重要的工业催化剂。
是一种重要的工业催化剂。
(1)基态V原子核外电子的运动状态有________ 种,价电子排布图为________ 。
(2)钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为apm。

①该氧化物的化学式为________ 。
②该晶胞的密度为________  (写计算式即可,设
(写计算式即可,设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
(3) 催化剂参与
催化剂参与 催化氧化反应的机理如图。
催化氧化反应的机理如图。

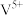 催化过程可以表示为:
催化过程可以表示为:
①……
②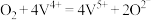
请写出①的离子方程式________ 。
(4)某 失活催化剂(主要含
失活催化剂(主要含 、
、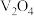 、
、 、
、 以及少量的Fe等)是重要的含钒二次资源。从失活催化剂提取钒的一种工艺流程如下。
以及少量的Fe等)是重要的含钒二次资源。从失活催化剂提取钒的一种工艺流程如下。
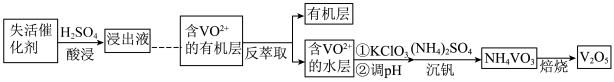
资料:i.HA(有机酸性萃取剂)对金属阳离子萃取能力由强到弱的顺序为: ;
;
ii.溶液pH<4.0时,+5价钒的存在形式为 ,6.0≤pH≤8.0时,正五价钒元素的存在形式为
,6.0≤pH≤8.0时,正五价钒元素的存在形式为 ,且二者可相互转化:
,且二者可相互转化: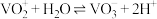 。
。
①浸出液中含有 、
、 、
、 、
、 等阳离子,浸出
等阳离子,浸出 的离子方程式是
的离子方程式是________ 。
②流程中“……”包含的操作顺序为________ 。(选填部分序号)(a.加还原剂 b.加氧化剂 c.萃取分液)
③“萃取”、“反萃取”过程机理为:
 (水层)+2HA(有机层)
(水层)+2HA(有机层)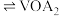 (有机层)
(有机层) (水层)。
(水层)。
反萃取剂选择 ,原因是
,原因是________ 。
④“沉钒”过程中需先加入 ,然后再通入氨气调节pH为6~8,最后加
,然后再通入氨气调节pH为6~8,最后加 。
。
a.加入 ,反应的离子方程式是
,反应的离子方程式是________ 。
b.结合平衡移动原理解释再通入氨气的作用________ 。
⑤产品中 纯度的测定方法如下。
纯度的测定方法如下。
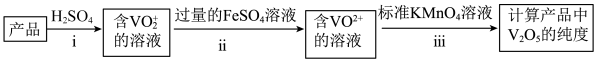
已知:此过程中, 可氧化
可氧化 ,且不与
,且不与 反应。产品中的杂质不参与反应。
反应。产品中的杂质不参与反应。
步骤iii中标准 溶液的浓度和消耗的体积分别为c和V,计算产品中
溶液的浓度和消耗的体积分别为c和V,计算产品中 的纯度还需要的实验数据有
的纯度还需要的实验数据有________ 。
 是一种重要的工业催化剂。
是一种重要的工业催化剂。(1)基态V原子核外电子的运动状态有
(2)钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为apm。

①该氧化物的化学式为
②该晶胞的密度为
 (写计算式即可,设
(写计算式即可,设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)(3)
 催化剂参与
催化剂参与 催化氧化反应的机理如图。
催化氧化反应的机理如图。
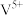 催化过程可以表示为:
催化过程可以表示为:①……
②
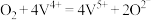
请写出①的离子方程式
(4)某
 失活催化剂(主要含
失活催化剂(主要含 、
、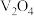 、
、 、
、 以及少量的Fe等)是重要的含钒二次资源。从失活催化剂提取钒的一种工艺流程如下。
以及少量的Fe等)是重要的含钒二次资源。从失活催化剂提取钒的一种工艺流程如下。
资料:i.HA(有机酸性萃取剂)对金属阳离子萃取能力由强到弱的顺序为:
 ;
;ii.溶液pH<4.0时,+5价钒的存在形式为
 ,6.0≤pH≤8.0时,正五价钒元素的存在形式为
,6.0≤pH≤8.0时,正五价钒元素的存在形式为 ,且二者可相互转化:
,且二者可相互转化: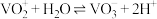 。
。①浸出液中含有
 、
、 、
、 、
、 等阳离子,浸出
等阳离子,浸出 的离子方程式是
的离子方程式是②流程中“……”包含的操作顺序为
③“萃取”、“反萃取”过程机理为:
 (水层)+2HA(有机层)
(水层)+2HA(有机层) (有机层)
(有机层) (水层)。
(水层)。反萃取剂选择
 ,原因是
,原因是④“沉钒”过程中需先加入
 ,然后再通入氨气调节pH为6~8,最后加
,然后再通入氨气调节pH为6~8,最后加 。
。a.加入
 ,反应的离子方程式是
,反应的离子方程式是b.结合平衡移动原理解释再通入氨气的作用
⑤产品中
 纯度的测定方法如下。
纯度的测定方法如下。
已知:此过程中,
 可氧化
可氧化 ,且不与
,且不与 反应。产品中的杂质不参与反应。
反应。产品中的杂质不参与反应。步骤iii中标准
 溶液的浓度和消耗的体积分别为c和V,计算产品中
溶液的浓度和消耗的体积分别为c和V,计算产品中 的纯度还需要的实验数据有
的纯度还需要的实验数据有
您最近半年使用:0次