课前-5.1.2 硫酸和硫酸根离子的检验-人教2019必修第二册
全国
高一
课前预习
2022-03-02
151次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
课前-5.1.2 硫酸和硫酸根离子的检验-人教2019必修第二册
全国
高一
课前预习
2022-03-02
151次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
一、填空题 添加题型下试题
填空题
|
较易(0.85)
解题方法
1. 硫酸的工业制法
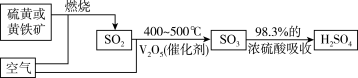
(1)三种原料:硫黄或____ 、____ ,98.3%的浓硫酸(代替水)。
(2)三个阶段
①二氧化硫的制取和净化。(造气阶段)
②SO2氧化成SO3。(接触氧化阶段)
③三氧化硫的吸收和硫酸的生成。(生成阶段)
(3)三个反应
①____ 。
②____ 。
③____ 。

(1)三种原料:硫黄或
(2)三个阶段
①二氧化硫的制取和净化。(造气阶段)
②SO2氧化成SO3。(接触氧化阶段)
③三氧化硫的吸收和硫酸的生成。(生成阶段)
(3)三个反应
①
②
③
您最近一年使用:0次
填空题
|
容易(0.94)
2. 硫酸的物理性质及酸的通性
(1)物理性质
纯净的硫酸是____ 黏稠状液体,密度比水____ ,能与水以任意比混合,沸点____ ,难挥发。
(2)酸的通性
H2SO4在水里很容易电离出____ ,具有____ ,能使紫色石蕊试液显____ ,请写出下列反应的离子方程式。
①和活泼金属(如Fe):____ 。
②和金属氧化物(如MgO):____ 。
③和碱[如Mg(OH)2]:____ 。
④和盐(如Na2CO3):____ 。
(1)物理性质
纯净的硫酸是
(2)酸的通性
H2SO4在水里很容易电离出
①和活泼金属(如Fe):
②和金属氧化物(如MgO):
③和碱[如Mg(OH)2]:
④和盐(如Na2CO3):
您最近一年使用:0次
填空题
|
容易(0.94)
3. 浓硫酸的特性
(1)浓硫酸有三大特性:_____ 、____ 和____ 。
(2)吸水性与脱水性
①吸水性
浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作____ 。
②脱水性

浓硫酸能把有机物中的氢元素和氧元素按____ 脱去。如向蔗糖中加入浓硫酸时,蔗糖逐渐变黑,体积膨胀,形成____ 固体,并放出有____ 气味的气体。
(3)强氧化性
强氧化性表现
①与金属反应
与大多数金属:如Cu:____ ;与Fe、Al:常温下____ (金属表面形成一层___ 的____ )。
②与非金属反应:如C:____ 。
③与还原性化合物反应:如:____ 。
(1)浓硫酸有三大特性:
(2)吸水性与脱水性
①吸水性
浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作
②脱水性

浓硫酸能把有机物中的氢元素和氧元素按
(3)强氧化性
| 实验操作 |  |
| 实验现象 | a试管中铜丝表面 b试管中的溶液 c试管中的 |
| 实验结论 | 在反应中,浓硫酸是 |
①与金属反应
与大多数金属:如Cu:
②与非金属反应:如C:
③与还原性化合物反应:如:
您最近一年使用:0次
二、判断题 添加题型下试题
判断题
|
较易(0.85)
解题方法
您最近一年使用:0次
判断题
|
容易(0.94)
解题方法
您最近一年使用:0次
判断题
|
容易(0.94)
7. 金属铜在常温下放入浓硫酸无现象,是浓硫酸把铜钝化了。(__)
【知识点】 浓硫酸的强氧化性解读 铜与强氧化性酸的反应
您最近一年使用:0次
2022-03-02更新
|
284次组卷
|
2卷引用:课前-5.1.2 硫酸和硫酸根离子的检验-人教2019必修第二册
判断题
|
较易(0.85)
解题方法
8. 100mL18.0mol·L-1的浓硫酸和足量铜反应生成SO2分子数目为0.9NA。(__)
您最近一年使用:0次
判断题
|
适中(0.65)
9. 浓硫酸有强烈的吸水性,因此可以干燥SO2、H2S、HI、NH3等气体。(__)
【知识点】 硫酸
您最近一年使用:0次
2022-03-02更新
|
321次组卷
|
2卷引用:课前-5.1.2 硫酸和硫酸根离子的检验-人教2019必修第二册
判断题
|
容易(0.94)
解题方法
您最近一年使用:0次
三、填空题 添加题型下试题
填空题
|
较易(0.85)
解题方法
11. 下列各过程主要表现了浓硫酸的哪些性质?请将答案的序号分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体____ 。
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸____ 。
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体____ 。
(4)常温下可以用铁或铝的容器贮存浓硫酸____ 。
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末____ 。
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体____ 。
(7)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑____ 。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体
(4)常温下可以用铁或铝的容器贮存浓硫酸
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体
(7)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑
您最近一年使用:0次
填空题
|
较易(0.85)
解题方法
12. 回答下列问题:
(1)50mL物质的量浓度为18mol·L-1的硫酸中加入足量铜片并加热,充分反应,被还原的硫酸____ 0.9mol(填“大于”“等于”或“小于”,下同),消耗铜的物质的量___ 0.45mol。原因是____ 。
(2)将一定量的锌与100mL18.5mol·L-1浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1,则下列叙述中正确的是___ (填字母)。
(1)50mL物质的量浓度为18mol·L-1的硫酸中加入足量铜片并加热,充分反应,被还原的硫酸
(2)将一定量的锌与100mL18.5mol·L-1浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1,则下列叙述中正确的是
| A.气体A为SO2和H2的混合物 |
| B.气体A中SO2和H2的体积比为4∶1 |
| C.反应中共消耗Zn97.5g |
| D.反应中共转移3mol电子 |
【知识点】 酸的通性解读 浓硫酸的强氧化性解读 铜与强氧化性酸的反应
您最近一年使用:0次
填空题
|
容易(0.94)
13. 硫酸根离子检验的实验探究
| 实验操作 |  |  |  |
| 实验现象 | 先 | 先 | 先 |
| 实验结论 | SO 与Ba2+反应生成不溶于盐酸的 与Ba2+反应生成不溶于盐酸的 | CO 与Ba2+反应生成的白色沉淀BaCO3,可溶于盐酸 与Ba2+反应生成的白色沉淀BaCO3,可溶于盐酸 | |
您最近一年使用:0次
填空题
|
较易(0.85)
解题方法
14. 检验SO 的正确操作及解释
的正确操作及解释
(1)待测液 取清液
取清液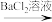 出现
出现____ 沉淀,即可确定存在SO 。
。
(2)理论解释
①先加稀盐酸的目的是排除____ 、____ 、____ 等离子干扰。
②再加入BaCl2溶液,若存在SO ,发生反应的离子方程式为
,发生反应的离子方程式为____ 。
 的正确操作及解释
的正确操作及解释(1)待测液
 取清液
取清液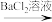 出现
出现 。
。(2)理论解释
①先加稀盐酸的目的是排除
②再加入BaCl2溶液,若存在SO
 ,发生反应的离子方程式为
,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
容易(0.94)
15. SO 检验应用——粗盐除杂
检验应用——粗盐除杂
(1)若除去粗盐中杂质(硫酸盐、CaCl2、MgCl2),将选用的试剂及反应的离子方程式填入表中:
(2)试剂加入的顺序
为使杂质离子完全除去,通常加入试剂及顺序有如下三种:
①BaCl2溶液→NaOH溶液→____ →盐酸;
②NaOH溶液→BaCl2溶液→____ →盐酸;
③____ →____ →____ →盐酸。
总结:为保障杂质离子完全除去,只要____ 在____ 之后加入即可。
 检验应用——粗盐除杂
检验应用——粗盐除杂(1)若除去粗盐中杂质(硫酸盐、CaCl2、MgCl2),将选用的试剂及反应的离子方程式填入表中:
| 杂质 | 加入的试剂 | 离子方程式 |
| 硫酸盐 | ||
| CaCl2 | ||
| MgCl2 |
为使杂质离子完全除去,通常加入试剂及顺序有如下三种:
①BaCl2溶液→NaOH溶液→
②NaOH溶液→BaCl2溶液→
③
总结:为保障杂质离子完全除去,只要
您最近一年使用:0次
2022-03-02更新
|
702次组卷
|
2卷引用:课前-5.1.2 硫酸和硫酸根离子的检验-人教2019必修第二册
四、判断题 添加题型下试题
判断题
|
容易(0.94)
您最近一年使用:0次
判断题
|
容易(0.94)
解题方法
19. 为除去粗盐水中少量的CO ,可向溶液中加入过量的K2CO3溶液,然后过滤。(__)
,可向溶液中加入过量的K2CO3溶液,然后过滤。(__)
 ,可向溶液中加入过量的K2CO3溶液,然后过滤。(__)
,可向溶液中加入过量的K2CO3溶液,然后过滤。(__)
您最近一年使用:0次
判断题
|
容易(0.94)
20. 为除去粗盐中的Mg2+、Ca2+、SO ,可依次加入稍过量的NaOH、BaCl2、Na2CO3溶液,过滤后加入稀盐酸调节溶液为中性。(__)
,可依次加入稍过量的NaOH、BaCl2、Na2CO3溶液,过滤后加入稀盐酸调节溶液为中性。(__)
 ,可依次加入稍过量的NaOH、BaCl2、Na2CO3溶液,过滤后加入稀盐酸调节溶液为中性。(__)
,可依次加入稍过量的NaOH、BaCl2、Na2CO3溶液,过滤后加入稀盐酸调节溶液为中性。(__)
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
较易(0.85)
21. 为检验某种阳离子为Na+的溶液中含有的阴离子是SO 、CO
、CO 还是OH-、Cl-,下列设计的方案中合理的是
还是OH-、Cl-,下列设计的方案中合理的是____ 。
方案一:检验CO :向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
:向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
方案二:检验SO :先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
:先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
方案三:检验OH-:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验Cl-:向待测溶液中依次加入稀盐酸和AgNO3溶液,有白色沉淀生成
 、CO
、CO 还是OH-、Cl-,下列设计的方案中合理的是
还是OH-、Cl-,下列设计的方案中合理的是方案一:检验CO
 :向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
:向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成方案二:检验SO
 :先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
:先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀方案三:检验OH-:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验Cl-:向待测溶液中依次加入稀盐酸和AgNO3溶液,有白色沉淀生成
您最近一年使用:0次
填空题
|
较易(0.85)
22. 依据粗盐提纯的原理,除去氯化钾溶液中少量的氯化镁、硫酸镁等杂质,可选用氢氧化钡溶液、稀盐酸和碳酸钾溶液三种试剂,按如图步骤操作:
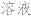


 纯净氯化钾溶液
纯净氯化钾溶液
(1)B的化学式是____ ,C的化学式是____ 。
(2)加入过量A的目的是___ 。
(3)加入过量B的目的是____ 。
(4)加热煮沸的目的是____ 。
(5)操作Ⅰ的名称是____ 。
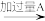
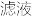

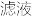

 纯净氯化钾溶液
纯净氯化钾溶液(1)B的化学式是
(2)加入过量A的目的是
(3)加入过量B的目的是
(4)加热煮沸的目的是
(5)操作Ⅰ的名称是
您最近一年使用:0次
2022-03-02更新
|
489次组卷
|
2卷引用:课前-5.1.2 硫酸和硫酸根离子的检验-人教2019必修第二册
试卷分析
整体难度:较易
考查范围:认识化学科学、常见无机物及其应用、化学实验基础
试卷题型(共 22题)
题型
数量
填空题
10
判断题
12
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、填空题 | |||
| 1 | 0.85 | 氧化还原反应方程式的配平 二氧化硫与氧气的反应 酸性氧化物通性 | |
| 2 | 0.94 | 硫酸物理性质 酸的通性 | |
| 3 | 0.94 | 浓硫酸的吸水性 浓硫酸的脱水性 浓硫酸的强氧化性 | |
| 11 | 0.85 | 硫酸物理性质 浓硫酸的吸水性 浓硫酸的脱水性 浓硫酸的强氧化性 | |
| 12 | 0.85 | 酸的通性 浓硫酸的强氧化性 铜与强氧化性酸的反应 | |
| 13 | 0.94 | 硫酸根离子的检验 | |
| 14 | 0.85 | 硫酸根离子的检验 | |
| 15 | 0.94 | 离子反应在混合物分离、除杂中的应用 硫酸根离子的检验 | |
| 21 | 0.85 | 硫酸根离子的检验 常见阳离子的检验 常见阴离子的检验 | |
| 22 | 0.85 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯综合应用 | |
| 二、判断题 | |||
| 4 | 0.85 | 酸的通性 | |
| 5 | 0.94 | 浓硫酸的吸水性 浓硫酸的脱水性 | |
| 6 | 0.94 | 浓硫酸的吸水性 浓硫酸的脱水性 | |
| 7 | 0.94 | 浓硫酸的强氧化性 铜与强氧化性酸的反应 | |
| 8 | 0.85 | 化学方程式计算中物质的量的运用 浓硫酸的强氧化性 铜与强氧化性酸的反应 | |
| 9 | 0.65 | 硫酸 | |
| 10 | 0.94 | 浓硫酸的脱水性 浓硫酸的强氧化性 | |
| 16 | 0.85 | 硫酸根离子的检验 | |
| 17 | 0.94 | 硫酸根离子的检验 | |
| 18 | 0.94 | 硫酸根离子的检验 | |
| 19 | 0.94 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯的常见化学方法 | |
| 20 | 0.94 | 离子反应在混合物分离、除杂中的应用 硫酸根离子的检验 物质分离、提纯的常见化学方法 | |



