2019年10月15日 《每日一题》2020年高考化学一轮复习——沉淀溶解平衡
全国
高三
专题练习
2019-10-17
245次
整体难度:
适中
考查范围:
化学反应原理
2019年10月15日 《每日一题》2020年高考化学一轮复习——沉淀溶解平衡
全国
高三
专题练习
2019-10-17
245次
整体难度:
适中
考查范围:
化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. ①已知t ℃时AgCl的Ksp=2.0×10-10;②在t ℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
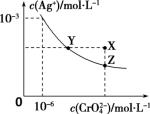

| A.在t ℃时,Ag2CrO4的Ksp为1.0×10-12 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| C.在t ℃时,以0.01 mol·L-1AgNO3溶液滴定20.00 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液,CrO42-后沉淀 |
D.在t ℃时,反应Ag2CrO4(s)+2Cl-(aq) 2AgCl(s)+CrO 2AgCl(s)+CrO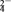 (aq)的平衡常数K=2.5×107 (aq)的平衡常数K=2.5×107 |
您最近一年使用:0次
2019-01-20更新
|
470次组卷
|
5卷引用:2015届河南省中原名校高三上学期第一次摸底考试化学试卷
单选题
|
适中(0.65)
名校
2. 已知溶液中存在平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入Na2CO3溶液,其中固体质量增加
⑦向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
 Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入Na2CO3溶液,其中固体质量增加
⑦向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
| A.①⑥ | B.①⑥⑦ | C.②③④⑥ | D.①②⑥⑦ |
您最近一年使用:0次
2019-10-17更新
|
892次组卷
|
11卷引用:2019年10月15日 《每日一题》2020年高考化学一轮复习——沉淀溶解平衡
2019年10月15日 《每日一题》2020年高考化学一轮复习——沉淀溶解平衡(已下线)专题8.4 难溶电解质的溶解平衡(讲)-《2020年高考一轮复习讲练测》云南省元阳县一中2020-2021学年高二下学期6月份考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(精讲)-2022年一轮复习讲练测(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)云南省开远市第一中学校2021-2022学年高二下学期开学考试化学试题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)3.4 沉淀溶解平衡-同步学习必备知识第1课时 沉淀溶解平衡与溶度积(已下线)第32讲难溶电解质的溶解平衡(已下线)第5讲 难溶电解质的溶解平衡
单选题
|
适中(0.65)
解题方法
3. 某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
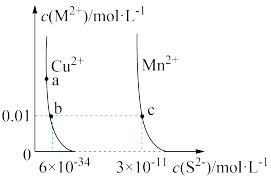
| A.该温度下,Ksp(CuS)小于Ksp(MnS) |
| B.向CuSO4溶液中加入MnS发生如下反应:Cu2+(aq)+MnS(s)=CuS(s)+Mn2+(aq) |
| C.在含有CuS和MnS固体的溶液中c(Cu2+):c(Mn2+)为2×10-23:1 |
| D.a点对应的Ksp大于b点对应的Ksp |
您最近一年使用:0次
单选题
|
较难(0.4)
4. 25 ℃时,向0.10 mol·L-1 H2S溶液中通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)的关系如图(忽略溶液体积的变化、H2S的挥发)。已知H2S的Ka1=1.3×10-7,Ka2=7.1×10-15,CdS的Ksp=3.6×10-29,一般认为溶液中离子浓度不大于1.0×10-5 mol·L-1时即沉淀完全。下列说法正确的是
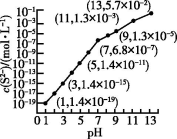

| A.pH=13时,溶液中的溶质为Na2S |
| B.pH=5时,向H2S溶液中通入了少量的HCl |
| C.pH=7时,溶液中c(H2S)≈0.043 mol·L-1 |
| D.pH=1时,c(S2-)太小,故不能处理含Cd2+的污水 |
【知识点】 弱电解质的电离平衡 难溶电解质的溶解平衡 溶度积常数相关计算解读
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理
试卷题型(共 4题)
题型
数量
单选题
4
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积规则及其应用 溶度积常数相关计算 | |
| 2 | 0.65 | 沉淀溶解平衡的应用 浓度对难溶电解质溶解平衡的影响 温度对难溶电解质溶解平衡的影响 同离子效应对难溶电解质溶解平衡的影响 | |
| 3 | 0.65 | 温度对难溶电解质溶解平衡的影响 溶度积规则及其应用 溶度积常数相关计算 | |
| 4 | 0.4 | 弱电解质的电离平衡 难溶电解质的溶解平衡 溶度积常数相关计算 | |



