反应2C+O2=2CO的能量变化如图所示。下列说法正确的是( )
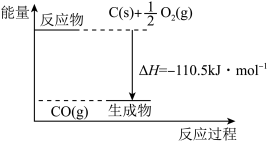

| A.12gC(s)与一定量O2(g)反应生成14gCO(g)放出的热量为110.5kJ |
| B.2molC(s)与足量O2(g)反应生成CO2(g)放出的热量大于221kJ |
| C.该反应的热化学方程式是2C(s)+O2(g)=2CO(g) ΔH=-221kJ |
| D.该反应的反应热等于生成的CO(g)中所具有的能量与参加反应的O2(g)中所具有的能量的差 |
更新时间:2020-04-13 19:26:25
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列说法不正确的是
| A.已知2C(s)+O2(g)=2CO(g) ∆H=-221kJ/mol,则碳的燃烧热大于110.5 kJ•mol-1 |
| B.稀醋酸与稀氢氧化钠溶液反应生成1 mol水时放出的热量小于57.3 kJ |
| C.升高温度和使用正催化剂都可以提高反应体系内活化分子百分数 |
| D.一个化学反应有且只有一个对应的焓变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
真题
名校
【推荐2】在298.15 K、100 kPa条件下,N2(g) +3H2 (g)=2NH3(g) ΔH=-92.4 kJ·mol-1,N2 (g) 、H2(g)和NH3(g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N2(g) +3H2(g)]、生成物[2NH3(g)]的能量随温度T的变化示意图合理的是
A.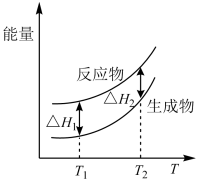 | B.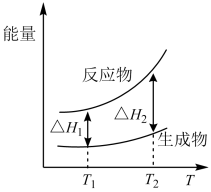 |
C.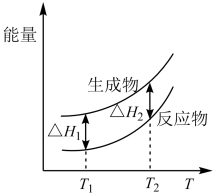 | D.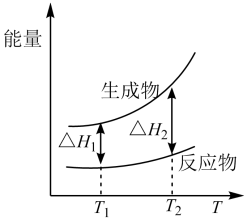 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
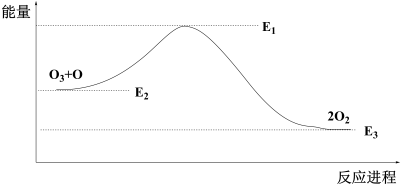
【推荐1】已知某化学反应A2(g)+2B2(g)=2AB2(g)(AB2的分子结构为B—A—B)的能量变化如图所示,下列有关叙述中正确的是
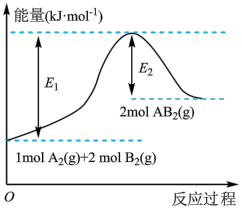

| A.由2molA(g)和4molB(g)形成4 mol A—B键吸收E2 kJ能量 |
| B.该反应的ΔH=-(E1-E2) kJ· mol-1 |
| C.该反应中反应物的键能总和大于生成物的键能总和 |
| D.该反应是放热反应 |
您最近一年使用:0次
【推荐2】下图为反应 2H2(g)+O2(g)=2H2O(g)的能量变化示意图。 下列说法正确的是
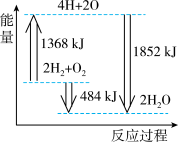

| A.拆开 2 mol H2(g)和 1 mol O2(g)中的化学键成为H、O原子,共放出1368 kJ 能量 |
| B.由 H、O 原子形成 2 mol H2O(g),共吸收1852 kJ 能量 |
| C.2 mol H2(g)和 1 mol O2(g)反应生成 2 mol H2O(g),共放出484 kJ 能量 |
| D.2 mol H2(g)和 1 mol O2(g)反应生成 2 mol H2O(l),ΔH>-484 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】反应2SO2(g)+O2(g)  2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是
2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是
 2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是
2SO3(g) △H<0是工业上合成硫酸过程中的一步反应,下列关于该反应的说法正确的是| A.反应物的总能量高于生成物的总能量 |
| B.催化剂可以降低硫氧键键能 |
| C.加压有利于SO3生成,所以工业上压强越高越好 |
| D.升高温度可以增大正反应速率,降低逆反应速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实与对应的方程式不符合 的是
A.自然界正常雨水pH=5.6是因为: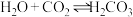 , ,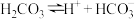 |
B.用CH3COOH溶液和NaOH溶液反应测定中和热: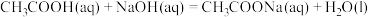 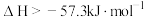 |
C.硫代硫酸钠溶液与稀硫酸混合出现浑浊: |
D.甲烷的燃烧热为 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: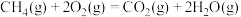 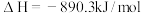 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】接触法制硫酸生产中的关键工序是SO2的催化氧化,该反应过程中能量变化如图所示,下列说法正确的是( )

A.该反应的热化学方程式为:SO2(g)+ O2(g)=SO3(g)ΔH=+98kJ·mol-1 O2(g)=SO3(g)ΔH=+98kJ·mol-1 |
| B.使用催化剂能增大SO2的平衡转化率 |
| C.降低温度,正反应速率增大,逆反应速率降低 |
| D.增大O2浓度,平衡向正方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】有关能量的判断或表示方法正确的是
| A.由: H+(aq)+ OH -(aq)= H2O(l) △H = -57.3kJ/mol,可知:含0.5mol H2SO4的浓溶液与含1molNaOH的溶液混合,放出热量为57.3 kJ |
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)  2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| C.等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 |
| D.甲烷的标准燃烧热为890.3kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为 CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =-890.3kJ·mol-1 |
您最近一年使用:0次