有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A→B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为:C2++2e-→C,B-2e-→B2+则A、B、C、D金属性由强到弱的顺序为( )
| A.A>B>C>D | B.A>B>D>C |
| C.D>C>A>B | D.D>A>B>C |
更新时间:2020-04-28 18:42:21
|
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐1】下列关于原电池的叙述正确的是
| A.原电池将化学能转化为电能 |
| B.原电池正极发生的是氧化反应 |
| C.原电池在工作时其正极不断产生电子并经过外电路流向负极 |
| D.用导线连接的两种不同金属同时插入液体中,能形成原电池 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】科学家设计了锂-空气电池,它直接使用金属锂作负极,让从空气中获得的 通过多孔碳电极。该电池具有较高的能量密度(单位质量的电池所放出的能量)。下列关于这种电池的说法正确的是
通过多孔碳电极。该电池具有较高的能量密度(单位质量的电池所放出的能量)。下列关于这种电池的说法正确的是
 通过多孔碳电极。该电池具有较高的能量密度(单位质量的电池所放出的能量)。下列关于这种电池的说法正确的是
通过多孔碳电极。该电池具有较高的能量密度(单位质量的电池所放出的能量)。下列关于这种电池的说法正确的是| A.放电时氧气发生氧化反应 | B.放电时电子向负极移动 |
| C.放电时电能转化为化学能 | D.能量密度高可能是因为锂的相对原子质量小 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】根据下列实验事实:
(1)X+Y2+===X2++Y
(2)Z+2H2O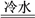 Z(OH)2+H2↑
Z(OH)2+H2↑
(3)Z2+离子的氧化性比X2+弱
(4)由Y、W作电极组成的原电池反应为:Y-2e-===Y2+
由此可知,X、Y、Z、W的还原性由强到弱的顺序是
(1)X+Y2+===X2++Y
(2)Z+2H2O
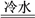 Z(OH)2+H2↑
Z(OH)2+H2↑(3)Z2+离子的氧化性比X2+弱
(4)由Y、W作电极组成的原电池反应为:Y-2e-===Y2+
由此可知,X、Y、Z、W的还原性由强到弱的顺序是
| A.X>Y>Z>W | B.Y>X>W>Z |
| C.Z>X>Y>W | D.Z>Y>X>W |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】某金属能跟稀盐酸作用放出氢气,该金属与锌组成原电池时,锌为负极,此金属可能是
| A.镁 | B.铜 | C.铝 | D.铁 |
您最近一年使用:0次



