下列关于物质“反应程度”的说法正确的是( )
| A.一定条件下,1molN2与3molH2反应可制备1.0molNH3 |
| B.一定条件下,2molSO2与足量O2反应可得到2molSO3 |
| C.10mL18.0mol/LH2SO4与足量铜加热反应可制备0.09molSO2 |
| D.含4molHCl的浓盐酸与足量的MnO2加热反应可制备1molCl2 |
更新时间:2020-04-30 12:50:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】实验室用下列装置制备无水AlCl3(183℃升华),无水AlC13遇潮湿空气即产生大量白雾。下列说法错误的是
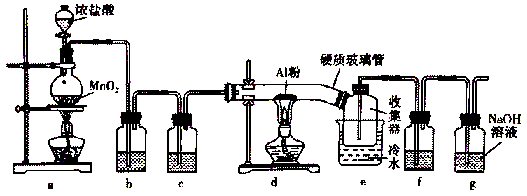

| A.b、c、f中依次盛装饱和食盐水、浓硫酸、浓硫酸 |
| B.g中发生的反应为Cl2+2NaOH=NaCl+NaClO+H2O |
| C.e装置的收集器必须保持干燥 |
| D.实验时,a和d处酒精灯应同时点燃 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式书写正确的是( )
| A.醋酸溶解水垢(CaCO3):CaCO3+2H+ =Ca2++H2O+CO2↑ |
B.在NaHCO3溶液中加入少量的Ba(OH)2溶液: Ba2+ +2OH- +2HCO =BaCO3↓+2H2O+CO =BaCO3↓+2H2O+CO |
| C.氢氧化铜和盐酸反应: H+ +OH- =H2O |
| D.实验室制氯气:MnO2+4H ++4Cl-= Mn2++2Cl2 ↑+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向蔗糖中加入浓硫酸, | 蔗糖变成疏松多孔的海绵状 | 浓硫酸具有吸水性和强氧化性 |
| B | 将0.1mol/L MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/L CuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的溶解度比Mg(OH)2的小 |
| C | FeCl3和BaCl2混合溶液中通入足量SO2 | 溶液变为浅绿色且有白色沉淀生成 | Fe3+被还原为Fe2+,沉淀为BaSO3 |
| D | 常温下,将铁片浸入足量浓硫酸中 | 铁片上无明显现象 | 常温下,铁与浓硫酸没有发生化学反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用下列实验装置进行实验,能达到实验目的的是
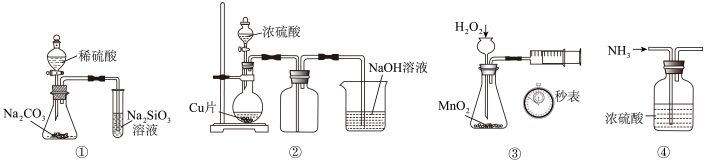

| A.图①可比较硫、碳、硅三种元素的非金属性强弱 |
B.图②可用于制备和收集 |
C.图③可测定在 催化作用下 催化作用下 的分解速率 的分解速率 |
D.图④可用于干燥 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应的离子方程式正确的是
| A.用H2SO4中和废氨水:H++OH-=H2O |
| B.用稀盐酸除水垢中的氢氧化镁:Mg(OH)2+2H+=Mg2++2H2O |
C.用碳酸氢钠作为抗酸药中和胃酸:2H++ =H2O+CO2↑ =H2O+CO2↑ |
D.用稀硝酸溶解铜:Cu+2 +4H+=Cu2++2NO2↑+H2O +4H+=Cu2++2NO2↑+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列反应的离子方程式书写正确的是
A.铜片与稀 反应生成气体: 反应生成气体: |
B. 溶液中加入稀硫酸: 溶液中加入稀硫酸: |
C.大理石溶于醋酸中: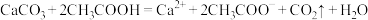 |
D.硫化亚铁溶于稀硝酸中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向火箭燃料液态联氨(N2H4)中加入催化剂,发生反应:N2H4(l)=N2(g)+2H2(g) △H。
已知: ①3N2H4(l)=4NH3(g)+ N2(g) △H1=-336.6kJ·mol-1
②N2(g)+3H2(g) 2NH3(g)△H2=-92.4kJ·mol-1。
2NH3(g)△H2=-92.4kJ·mol-1。
下列说法错误的 是
已知: ①3N2H4(l)=4NH3(g)+ N2(g) △H1=-336.6kJ·mol-1
②N2(g)+3H2(g)
 2NH3(g)△H2=-92.4kJ·mol-1。
2NH3(g)△H2=-92.4kJ·mol-1。下列说法
| A.使用催化剂后,反应②的正、逆反应的活化能都减小,但△H1不变 |
| B.△H=-151.8kJ·mol-1 |
| C.将28g N2和10mol H2混合充分反应,放出的热量一定小于92.4 kJ |
| D.联氨作为火箭燃料是一种清洁能源 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.32g环状 ( ( )分子中含有S—S键的数目为 )分子中含有S—S键的数目为 |
B.1mol 与足量氧气充分反应,生成 与足量氧气充分反应,生成 的分子数为 的分子数为 |
C.12g 固体中含有 固体中含有 的数目为 的数目为 |
D. 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是一种重要的化工产品,目前的重要生产方法是“接触法”,反应原理为:2SO2+O2 2SO3,已知该反应为放热反应。则下列说法正确的是
2SO3,已知该反应为放热反应。则下列说法正确的是
 2SO3,已知该反应为放热反应。则下列说法正确的是
2SO3,已知该反应为放热反应。则下列说法正确的是| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.由反应可知,2mol SO2的能量大于2mol SO3的能量 |
| D.工业在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
您最近一年使用:0次



