今年是门捷列夫发现元素周期律150周年。下表为元素周期表的一部分。
回答下列问题:
(1)X元素的名称是______________ 。
(2)Y元素的氢化物H2Y的稳定性_____________ (填“>”或“<”)H2S。
(3)表中元素的最高价氧化物对应的水化物酸性最强的是____________ (填化学式)。
(4)写出W的最高价含氧酸的稀溶液与足量铁粉反应的离子方程式_____________ 。
(5)碳与镁可形成化合物M,若1molM与水反应生成2 mol Mg(OH)2和1mol烃N,N分子中碳氢质量比为9:1, M与水反应的化学方程式为___________ 。
| 碳 | W | Y | |
| X | 硫 | Z |
回答下列问题:
(1)X元素的名称是
(2)Y元素的氢化物H2Y的稳定性
(3)表中元素的最高价氧化物对应的水化物酸性最强的是
(4)写出W的最高价含氧酸的稀溶液与足量铁粉反应的离子方程式
(5)碳与镁可形成化合物M,若1molM与水反应生成2 mol Mg(OH)2和1mol烃N,N分子中碳氢质量比为9:1, M与水反应的化学方程式为
更新时间:2020-04-30 17:21:01
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
(1)X和W的元素符号分别为___ 、___ 。
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式___ ,工业合成Y的氢化物的化学方程式为___ 。
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是___ 。此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为___ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所含阴、阳离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子。试回答下列问题:
(1)写出下列元素的符号:A_______ ,B_______ ,C_______ ,D_______ ,E_______
(2)用电子式表示离子化合物A2B的形成过程:_______
(3)写出D、C、E形成的离子化合物的化学式:_______
(1)写出下列元素的符号:A
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出D、C、E形成的离子化合物的化学式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,按要求填空(填元素符号 或化学式 ):
(1)写出下列元素的元素符号 :①___ ,②___ ;
(2)在这些元素中,最活泼的金属元素 是___ ,最不活泼的元素 是___ 。
(3)在这些元素的最高价氧化物对应水化物 中,酸性最强的是___ ,碱性最强的是___ ,呈两性的氢氧化物 是___ 。
(4)写出③和⑧的单质反应产物的电子式___ 。
(5)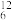 C在周期表中的位置:第
C在周期表中的位置:第___ 周期___ 族,它与氧气完全燃烧的产物的电子式___ 。
(6)在③与④的单质 中,化学性质较活泼的是___ ,判断的实验依据是___ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)在这些元素中,最活泼的
(3)在这些元素的最高价氧化物对应
(4)写出③和⑧的单质反应产物的电子式
(5)
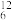 C在周期表中的位置:第
C在周期表中的位置:第(6)在③与④的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下图为元素周期表的一部分:

I.(1)元素③的基态原子轨道表示式为_________________ 。
(2)元素③④⑤的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)以下组合的原子间反应最容易形成离子键的是_____ (选填A、B、C、D,下同)。
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式_________________________________ 。
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。
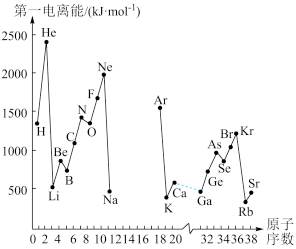
①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为___ < S <___ (填元素符号)
②图中第一电离能最小的元素在周期表中的位置____________________
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表( )
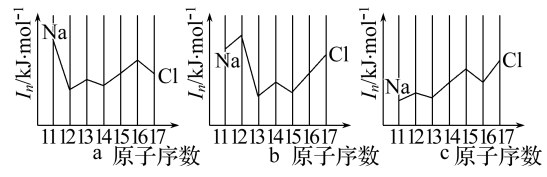
A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________________________________________

I.(1)元素③的基态原子轨道表示式为
(2)元素③④⑤的第一电离能由大到小的顺序为
(3)以下组合的原子间反应最容易形成离子键的是
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。

①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为
②图中第一电离能最小的元素在周期表中的位置
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表

A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
| 电离能/kJ/mol | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
(1) ①的元素符号是__________
(2) ②和⑥两种元素的原子半径大小关系:_________ (填“>”或“<”);
(3) ③和⑤两种元素的金属性强弱关系:________ (填“>”或“<”);
(4)③和⑦形成的化合物属于_________ (填“离子化合物”或“共价化合物”);写出该化合物的电子式为:______________________ ;
(5)写出元素②在周期表中的位置_______________________ ;
(6)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:_____________ 。
| ⅠA | 0 | ||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | B | ① | ② | Ne | |||||
| 3 | ③ | ④ | ⑤ | Si | ⑥ | ⑦ | |||
(2) ②和⑥两种元素的原子半径大小关系:
(3) ③和⑤两种元素的金属性强弱关系:
(4)③和⑦形成的化合物属于
(5)写出元素②在周期表中的位置
(6)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表中主族的一部分,其中c是地壳中含量最多的元素,回答下列问题:__________ , 的结构式为
的结构式为___________ 。
(2)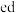 为
为__________ (填“离子”或“共价”)化合物,能证明该结论的实验依据为___________ .
(3)用电子式表示物质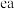 的形成过程
的形成过程__________________ ,该物质能与 反应生成
反应生成 ,反应中
,反应中 作
作________ 剂。
(4) 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为_________ (用化学式表示)。
(5)若 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: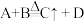 ,写出该反应的离子方程式
,写出该反应的离子方程式____________________ 。
(6)下列有关说法正确的是__________ 。
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用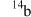 测定一些文物的年代
测定一些文物的年代
C.科学家常在 等元素区域寻找新型农药
等元素区域寻找新型农药
D.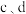 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
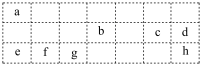
 的结构式为
的结构式为(2)
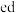 为
为(3)用电子式表示物质
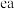 的形成过程
的形成过程 反应生成
反应生成 ,反应中
,反应中 作
作(4)
 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为(5)若
 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: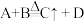 ,写出该反应的离子方程式
,写出该反应的离子方程式(6)下列有关说法正确的是
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用
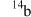 测定一些文物的年代
测定一些文物的年代C.科学家常在
 等元素区域寻找新型农药
等元素区域寻找新型农药D.
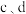 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质为黄绿色有毒气体。请回答下列问题:
(1)Q的离子结构示意图是__________________ 。
(2)六种元素中,原子半径最大的是___________ 。(写元素符号)
(3)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)____________ 。
(4)Y和Z的气态氢化物中,热稳定性强的是________ (用物质化学式表示)。
(5)Y的气态氢化物与X和M形成的化合物反应,产物的化学式为________ ,其中存在的化学键类型为____________________ 。
(6)X与Z可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:_______________________________________________________________ 。
(7)单质M与水反应的离子方程式为____________________________________________ 。
(1)Q的离子结构示意图是
(2)六种元素中,原子半径最大的是
(3)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)
(4)Y和Z的气态氢化物中,热稳定性强的是
(5)Y的气态氢化物与X和M形成的化合物反应,产物的化学式为
(6)X与Z可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:
(7)单质M与水反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】I.1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:_______ (任写一种)。
(2)请写出元素⑦的氧化物与元素③的氢化物的水溶液反应的化学方程式_______ 。
(3)元素①和元素⑦最高价氧化物的水化物中酸性较强的是_______ (填化学式)。
II.硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(4)硅元素在自然界中通常以石英石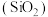 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。 的SiO2中含有Si-O键
的SiO2中含有Si-O键_______ 个。
(5)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”);
iii.由于硅酸盐组成比较复杂,通常用氧化物的形式表示:请用氧化物的形式表示钾云母K(Al3Si3O10)(OH)2的组成_______ 。
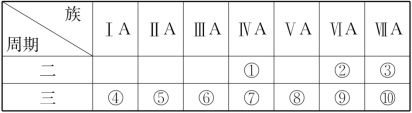
(2)请写出元素⑦的氧化物与元素③的氢化物的水溶液反应的化学方程式
(3)元素①和元素⑦最高价氧化物的水化物中酸性较强的是
II.硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(4)硅元素在自然界中通常以石英石
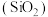 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 的SiO2中含有Si-O键
的SiO2中含有Si-O键(5)高纯硅单质可由石英砂(主要成分是
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:
ii.流程①焦炭体现了
iii.由于硅酸盐组成比较复杂,通常用氧化物的形式表示:请用氧化物的形式表示钾云母K(Al3Si3O10)(OH)2的组成
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某研究性学习小组设计了一组实验验证元素周期律。
I.甲同学在a、b、c、d四只烧杯中分别加入50 mL冷水,再各滴加几滴酚酞试液,依次加入大小相同的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的:验证同一主族,从上到下金属元素原子失电子能力逐渐增强;同一周期主族元素从左到右金属元素原子失电子能力逐渐_______ 。
(2)烧杯中反应最剧烈的金属是_______(填字母)。
(3)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法_______(填字母)。
II.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题。
(4)实验装置:
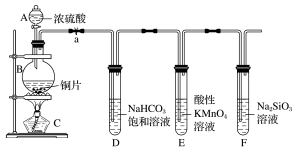
仪器B的名称为_______ 。
(5)实验步骤:连接仪器、_______ 、加药品,打开a,然后滴入浓硫酸,加热。
(6)问题探究:(已知酸性亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是_______ ;装置E中酸性KMnO4溶液的作用是_______ 。
②能说明碳元素的非金属性比硅元素的非金属性强的实验现象是_______ ;试管F中发生反应的离子方程式为_______ 。
③依据试管D中的反应,能否证明S的非金属性强于C的非金属性?_______ (填“能”或“否”)。说明理由_______ 。
I.甲同学在a、b、c、d四只烧杯中分别加入50 mL冷水,再各滴加几滴酚酞试液,依次加入大小相同的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的:验证同一主族,从上到下金属元素原子失电子能力逐渐增强;同一周期主族元素从左到右金属元素原子失电子能力逐渐
(2)烧杯中反应最剧烈的金属是_______(填字母)。
| A.钠 | B.镁 | C.铝 | D.钾 |
| A.把镁、铝的金属块换成金属粉末 | B.把烧杯中的冷水换成热水 |
| C.把烧杯中的冷水换成等量的同浓度的盐酸 | D.把烧杯中的冷水换成氢氧化钠溶液 |
II.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题。
(4)实验装置:

仪器B的名称为
(5)实验步骤:连接仪器、
(6)问题探究:(已知酸性亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是
②能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
③依据试管D中的反应,能否证明S的非金属性强于C的非金属性?
您最近一年使用:0次



