下图为元素周期表的一部分:

I.(1)元素③的基态原子轨道表示式为_________________ 。
(2)元素③④⑤的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)以下组合的原子间反应最容易形成离子键的是_____ (选填A、B、C、D,下同)。
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式_________________________________ 。
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。
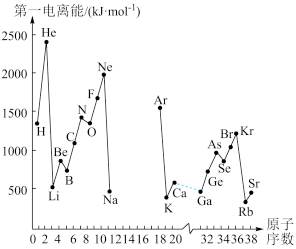
①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为___ < S <___ (填元素符号)
②图中第一电离能最小的元素在周期表中的位置____________________
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表( )
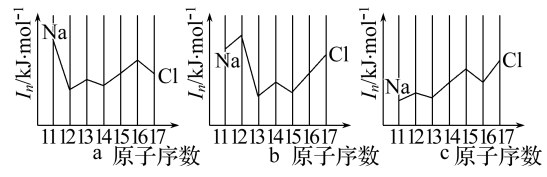
A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________________________________________

I.(1)元素③的基态原子轨道表示式为
(2)元素③④⑤的第一电离能由大到小的顺序为
(3)以下组合的原子间反应最容易形成离子键的是
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。

①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为
②图中第一电离能最小的元素在周期表中的位置
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表

A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
| 电离能/kJ/mol | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是
更新时间:2020-05-02 21:41:36
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表列出了①~⑩十种元素在周期表中的位置,请回答下列问题:
(1)表中10种元素中,某元素的原子最外层电子数是其核外电子层数的3倍,其中子数为10,该核素符号是___________ 。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是___________ 。(用离子符号表示)
(3)由元素①④形成的具有强氧化性的物质的电子式为___________ ;由元素⑥和⑨形成化合物乙,用电子式表示物质乙的形成过程___________ 。
(4)华为 技术遥遥领先,镓
技术遥遥领先,镓 的化合物氮化镓
的化合物氮化镓 和砷化镓
和砷化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为
作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为___________ ,砷的最高价氧化物的水化物的化学式为___________ 。
(5)可以比较⑤、⑥两元素金属性强弱的是___________。
(6)喝温水解口渴也能解体渴,但喝冰水效果差一些,这是有科学依据的。当温度较低时,水是以大分子水团形式存在的;当温度较高时水以小分子水团形式存在的,小分子水团更有利于人体吸收。当温度升高时主要破坏了水分子之间的___________ 。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
(1)表中10种元素中,某元素的原子最外层电子数是其核外电子层数的3倍,其中子数为10,该核素符号是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是
(3)由元素①④形成的具有强氧化性的物质的电子式为
(4)华为
 技术遥遥领先,镓
技术遥遥领先,镓 的化合物氮化镓
的化合物氮化镓 和砷化镓
和砷化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为
作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为(5)可以比较⑤、⑥两元素金属性强弱的是___________。
| A.将⑤的单质投入到⑥的盐溶液中 |
| B.比较这两种元素最高价氧化物的水化物的碱性 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
(6)喝温水解口渴也能解体渴,但喝冰水效果差一些,这是有科学依据的。当温度较低时,水是以大分子水团形式存在的;当温度较高时水以小分子水团形式存在的,小分子水团更有利于人体吸收。当温度升高时主要破坏了水分子之间的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表为元素周期表中的一部分.
用化学式或元素符号回答下列问题:
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是____________ .
(2)②③④中形成的简单离子半径由大到小的顺序是____________ .
(3)⑨的最高价氧化物对应水化物的化学式为____________ .①和⑨两元素形成化合物的化学式为____________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为____________ .
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是____________ ,三者非金属性的强弱顺序为____________ .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是
(2)②③④中形成的简单离子半径由大到小的顺序是
(3)⑨的最高价氧化物对应水化物的化学式为
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】2024年是元素周期表诞生155周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。部分元素在元素周期表中的位置如图所示。请回答:
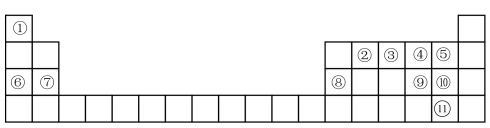
(1)元素③在周期表中的位置为______ 。
(2)元素④的一种核素的中子数是10,表示该核素的符号为_______ 。
(3)元素①和②形成的五原子分子的空间结构为________ 。
(4)⑨⑩⑪三种元素的最高价氧化物对应的水化物中,酸性最强的是_____ (填化学式)。
(5)⑤和⑦两种元素形成的化合物有重要的用途。用电子式表示该化合物的形成过程为_______ 。
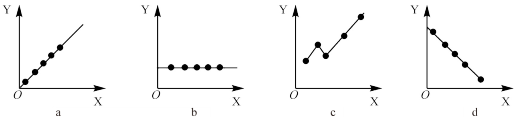
(6)下图分别表示元素的某种结构或性质与核电荷数的关系(X为核电荷数,Y为元素的有关结构或性质),下列说法正确的是________。(用选项字母表示)。

(1)元素③在周期表中的位置为
(2)元素④的一种核素的中子数是10,表示该核素的符号为
(3)元素①和②形成的五原子分子的空间结构为
(4)⑨⑩⑪三种元素的最高价氧化物对应的水化物中,酸性最强的是
(5)⑤和⑦两种元素形成的化合物有重要的用途。用电子式表示该化合物的形成过程为
(6)下图分别表示元素的某种结构或性质与核电荷数的关系(X为核电荷数,Y为元素的有关结构或性质),下列说法正确的是________。(用选项字母表示)。

| A.a图表示元素④⑤⑥⑦⑧的离子半径变化趋势 |
| B.b图表示元素⑤所在主族元素的最高化合价的变化趋势 |
C. 图表示元素①所在主族金属单质密度的变化趋势 图表示元素①所在主族金属单质密度的变化趋势 |
| D.d图表示⑥⑦⑧⑨⑩五种元素的电子层数的变化趋势 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E是前四周期元素。A、B、C同周期,C、D同主族且原子半径C>D,A原子结构示意图为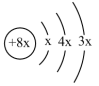 ,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:
(1)元素A、C、D的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(2)元素B、C、D中,其最高价氧化物对应水化物酸性最强的是_______ (填化学式,下同),简单离子半径最小的是_______ 。
(3)写出基态D原子的价电子轨道表示式_______ ,其电子占据最高能级的电子云轮廓图为_______ 形。
(4)E元素位于周期表中的_______ 区,其原子的价电子排布式为_______ 。
 ,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C最外层有三个未成对电子,E单质是目前生产生活中用量最大的金属。回答下列问题:(1)元素A、C、D的第一电离能由大到小的顺序是
(2)元素B、C、D中,其最高价氧化物对应水化物酸性最强的是
(3)写出基态D原子的价电子轨道表示式
(4)E元素位于周期表中的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层p能级的电子数等于次外层的电子总数,其基态原子的电子排布图为_______ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,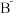 的结构示意图为
的结构示意图为_______ ,C元素在元素周期表的_______ 区。
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式_______ 。试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:_______ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为_______ 。
(1)A元素基态原子的最外层p能级的电子数等于次外层的电子总数,其基态原子的电子排布图为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,
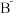 的结构示意图为
的结构示意图为(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.硫是一种重要的非金属元豢,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是______ ,最高能级电子所在的原子轨道为______ 形。
(2)比较沸点高低: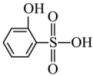
______ (填“>”或“<”)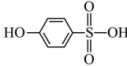 ,并解释原因:
,并解释原因:____________ 。
(3)ZnS晶胞如图所示:
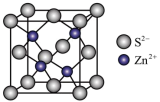
已知该晶胞密度为ρg/cm ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为______ pm。
Ⅱ.锂离子电池充放电过程中,正极材料晶胞的组成变化如图所示。
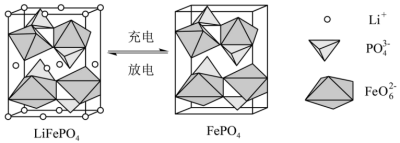
(4)①由于 的空间构型为
的空间构型为______ ,且磷氧键键能较大,锂离子嵌入和脱出时,磷酸铁锂的空间骨架不易发生形变,具有良好的循环稳定性。
②正极材料在 和
和 之间转化时,经过中间产物
之间转化时,经过中间产物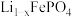 。
。 转化为
转化为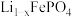 的过程中,每摩晶胞转移电子的物质的量为
的过程中,每摩晶胞转移电子的物质的量为______ 摩。
(1)基态硫原子的价层电子排布图是
(2)比较沸点高低:

 ,并解释原因:
,并解释原因:(3)ZnS晶胞如图所示:

已知该晶胞密度为ρg/cm
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为Ⅱ.锂离子电池充放电过程中,正极材料晶胞的组成变化如图所示。

(4)①由于
 的空间构型为
的空间构型为②正极材料在
 和
和 之间转化时,经过中间产物
之间转化时,经过中间产物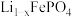 。
。 转化为
转化为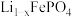 的过程中,每摩晶胞转移电子的物质的量为
的过程中,每摩晶胞转移电子的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为_______ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)_______ (填“大于”或“小于”)I1(Cu),原因是_______ 。
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为_______ ,C原子的杂化形式为_______ 。
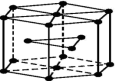
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______ 。
(1)Zn原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)基态e原子中电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形,核外共有___________ 种不同运动状态的电子。
(2)元素b在元素周期表中的位置为___________ ,元素i位于元素周期表的___________ 区。
(3)g的元素符号为___________ ,其基态原子的价电子排布式为___________ 。
(4)元素b、c、d的第一电离能从大到小的顺序是___________ (用元素符号表示)。
(5)元素h的价层电子排布图为___________ 。
(6)元素d的简单氢化物的空间构型为___________ ,该分子属于___________ (填“极性”或“非极性”)分子,d原子采取的杂化方式为___________ 。
(7)元素b、c的简单氢化物中,沸点较高的是___________ (填化学式),原因是___________ 。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | |||||||||||||||||
| g | h | i | |||||||||||||||
(2)元素b在元素周期表中的位置为
(3)g的元素符号为
(4)元素b、c、d的第一电离能从大到小的顺序是
(5)元素h的价层电子排布图为
(6)元素d的简单氢化物的空间构型为
(7)元素b、c的简单氢化物中,沸点较高的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)基态Li原子的电子排布式为___________ ,其处于元素周期表中的___________ (填“s”、“d”、“ds”或“p”)区。
(2)现有4种元素的基态原子的电子排布式如下:① ;②
;② ;③
;③ ;④
;④ 。则下列比较中,正确的是___________。
。则下列比较中,正确的是___________。
(3)由硅原子核形成的三种微粒,电子排布式分别为:① 、②
、②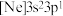 、③
、③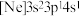 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(4)在第四周期元素中,未成对电子数最多的元素是___________ (写元素符号),它的价层电子的轨道表达式___________ 。
(5)Cu与Zn相比,第二电离能与第一电离能差值更大的是___________ (写元素符号),原因是___________ 。
(1)基态Li原子的电子排布式为
(2)现有4种元素的基态原子的电子排布式如下:①
 ;②
;② ;③
;③ ;④
;④ 。则下列比较中,正确的是___________。
。则下列比较中,正确的是___________。| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高化合价:④>③=②>① |
 、②
、②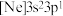 、③
、③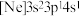 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.微粒半径:③>①>② |
| B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.得电子能力:①>② |
(5)Cu与Zn相比,第二电离能与第一电离能差值更大的是
您最近一年使用:0次
【推荐1】依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是_____ 基态硫原子的价电子排布式是_____
(2)基态的铁原子有___________ 个未成对电子,基态Fe2+的价电子排布图为_____
(3)Cu、K、O、F四种元素中第一电离能最小的是_____ ,电负性最大的是_____
(4)下列有关微粒性质的排列顺序错误的是___________ 。
A、元素的电负性: P<O<F B、元素的第一电离能: C<N<O
C、离子半径: O2->Na+>Mg2+ D、原子的未成对电子数 :Mn>Si>Cl
(5)下列基态原子或离子的电子排布式或排布图正确的是___________ (填序号,下同),违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利原理的是___________ 。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P: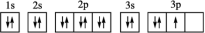
④Fe:1s22s22p63s23p63d64s2
⑤Mg2+:1s22s22p6
⑥C:
(1)基态硅原子的电子排布式是
(2)基态的铁原子有
(3)Cu、K、O、F四种元素中第一电离能最小的是
(4)下列有关微粒性质的排列顺序错误的是
A、元素的电负性: P<O<F B、元素的第一电离能: C<N<O
C、离子半径: O2->Na+>Mg2+ D、原子的未成对电子数 :Mn>Si>Cl
(5)下列基态原子或离子的电子排布式或排布图正确的是
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:

④Fe:1s22s22p63s23p63d64s2
⑤Mg2+:1s22s22p6
⑥C:

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】铁及其化合物在国民生产、生活中用途广泛。
(1)向 溶液中加入少量的
溶液中加入少量的 溶液,生成红色的
溶液,生成红色的 。N、C、H元素的第一电离能由大到小的顺序为
。N、C、H元素的第一电离能由大到小的顺序为____ ,O、N、C、H四种元素电负性最大的是____ (填元素符号)。
(2) 与
与 溶液混合生成
溶液混合生成 沉淀。配体
沉淀。配体 中C原子的杂化方式为
中C原子的杂化方式为_______ ,CH2=CHCH2CN分子中σ键与π键的数目之比为_______ 。
(3)用邻二氮菲(phen,结构为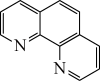 )与琥珀酸亚铁生成稳定的橙色配合物,可测定
)与琥珀酸亚铁生成稳定的橙色配合物,可测定 的浓度,发生反应:
的浓度,发生反应: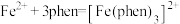 。
。
① 中,存在的化学键有
中,存在的化学键有_______ (填字母)。
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定 浓度时应控制pH为2~9的适宜范围,请解释原因:
浓度时应控制pH为2~9的适宜范围,请解释原因:_______ 。
(1)向
 溶液中加入少量的
溶液中加入少量的 溶液,生成红色的
溶液,生成红色的 。N、C、H元素的第一电离能由大到小的顺序为
。N、C、H元素的第一电离能由大到小的顺序为(2)
 与
与 溶液混合生成
溶液混合生成 沉淀。配体
沉淀。配体 中C原子的杂化方式为
中C原子的杂化方式为(3)用邻二氮菲(phen,结构为
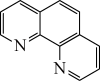 )与琥珀酸亚铁生成稳定的橙色配合物,可测定
)与琥珀酸亚铁生成稳定的橙色配合物,可测定 的浓度,发生反应:
的浓度,发生反应: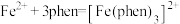 。
。①
 中,存在的化学键有
中,存在的化学键有a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定
 浓度时应控制pH为2~9的适宜范围,请解释原因:
浓度时应控制pH为2~9的适宜范围,请解释原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式_______ ,C、O、Si三种元素的电负性由大到小的顺序为_______ 。C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(2)基态铬原子和基态锰原子中第一电离能较大的是_______ (填元素符号),原因为_______ 。
(3)SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为_______ 。
(4)氧化物XO的电子总数与SiC的相等,则X为_______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是_______ 。
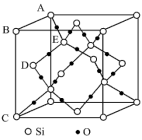
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含_______ 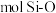 键。
键。
(1)写出Si的基态原子核外最外层电子排布式
(2)基态铬原子和基态锰原子中第一电离能较大的是
(3)SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为
(4)氧化物XO的电子总数与SiC的相等,则X为

(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含
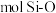 键。
键。
您最近一年使用:0次



