依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是_____ 基态硫原子的价电子排布式是_____
(2)基态的铁原子有___________ 个未成对电子,基态Fe2+的价电子排布图为_____
(3)Cu、K、O、F四种元素中第一电离能最小的是_____ ,电负性最大的是_____
(4)下列有关微粒性质的排列顺序错误的是___________ 。
A、元素的电负性: P<O<F B、元素的第一电离能: C<N<O
C、离子半径: O2->Na+>Mg2+ D、原子的未成对电子数 :Mn>Si>Cl
(5)下列基态原子或离子的电子排布式或排布图正确的是___________ (填序号,下同),违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利原理的是___________ 。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P: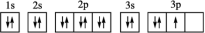
④Fe:1s22s22p63s23p63d64s2
⑤Mg2+:1s22s22p6
⑥C:
(1)基态硅原子的电子排布式是
(2)基态的铁原子有
(3)Cu、K、O、F四种元素中第一电离能最小的是
(4)下列有关微粒性质的排列顺序错误的是
A、元素的电负性: P<O<F B、元素的第一电离能: C<N<O
C、离子半径: O2->Na+>Mg2+ D、原子的未成对电子数 :Mn>Si>Cl
(5)下列基态原子或离子的电子排布式或排布图正确的是
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:

④Fe:1s22s22p63s23p63d64s2
⑤Mg2+:1s22s22p6
⑥C:

更新时间:2021-05-27 22:48:51
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】已知A、B、C三种元素的原子中,质子数:A<B<C,且都小于18,A元素原子的最外层电子数是次外层电子数的4倍;B元素的原子核外M层电子数是L层电子数的一半;C元素原子的次外层电子数比最外层电子数多3。试回答下列问题:
(1)写出三种元素的名称和符号:A___________ ,B___________ ,C___________ 。
(2)写出三种元素的原子核外电子排布式A___________ ,B___________ ,C___________ 。
(1)写出三种元素的名称和符号:A
(2)写出三种元素的原子核外电子排布式A
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】废旧锌锰电池中的黑锰粉含有MnO2、MnO(OH)、NH4Cl和少量ZnCl2、Fe2O3及炭黑等,为了保护环境、充分利用锰资源,通过如下流程制备MnSO4。

回答下列问题:
(1)Mn的原子结构示意图为___________ 。
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因___________ 。
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、___________ 、洗涤、干燥,得NH4Cl固体。

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为___________ 。
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是___________ ,实验II中H2O2的作用是___________ 。
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是___________ 。
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加___________ (填试剂),观察到___________ (填现象)。

回答下列问题:
(1)Mn的原子结构示意图为
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】天门冬氨酸锌是一种补锌剂,可以用天门冬氨酸(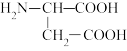 )和锌的化合物为原料制备。
)和锌的化合物为原料制备。
(1)天门冬氨酸分子中氮原子的轨道杂化类型为___ ;天门冬氨酸所含σ键和π键的数目之比为___ ;其所含四种元素电负性由大到小的顺序为___ 。
(2)Zn(NO3)2中所含NO 的空间构型为
的空间构型为___ (用文字描述)。
(3)工业ZnCl2中常混有杂质TiCl4,TiCl4室温下为无色液体,熔沸点低,易升华,可溶于甲苯和氯代烃等非极性溶剂中,它的晶体类型是___ 。Ti的核外电子排布式为___ 。
(4)ZnO的晶胞结构如图所示,Zn2+的配位数为___ 。

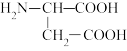 )和锌的化合物为原料制备。
)和锌的化合物为原料制备。(1)天门冬氨酸分子中氮原子的轨道杂化类型为
(2)Zn(NO3)2中所含NO
 的空间构型为
的空间构型为(3)工业ZnCl2中常混有杂质TiCl4,TiCl4室温下为无色液体,熔沸点低,易升华,可溶于甲苯和氯代烃等非极性溶剂中,它的晶体类型是
(4)ZnO的晶胞结构如图所示,Zn2+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】锂—磷酸氧铜电池正极的活性物质是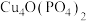 ,可通过下列反应制备:
,可通过下列反应制备: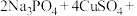
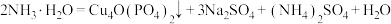 。
。
(1)写出基态 的电子排布式:
的电子排布式:_______________ 。
(2)P、S元素第一电离能大小关系为_______________ ,原因是_______________ 。
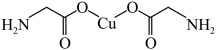
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为_______________ ,基态碳原子核外电子有_______________ 种运动状态。 ,生成配合物
,生成配合物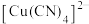 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为_______________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为_______________ ,铜的原子半径为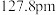 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为_______________  (列出计算式即可)。
(列出计算式即可)。
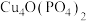 ,可通过下列反应制备:
,可通过下列反应制备: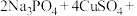
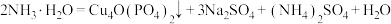 。
。(1)写出基态
 的电子排布式:
的电子排布式:(2)P、S元素第一电离能大小关系为
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为
 ,生成配合物
,生成配合物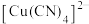 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为
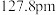 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为 (列出计算式即可)。
(列出计算式即可)。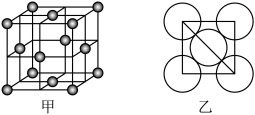
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】根据下表五种元素第一至第四电离能数据(单位: ),回答下面各题:
),回答下面各题:
(1)在周期表中,最可能处于同一族的是___________ 。
(2)T元素最多可能是___________ 区元素。若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物其中心原子的杂化方式为___________ 。
 ),回答下面各题:
),回答下面各题:| 元素 |  |  |  |  |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
(2)T元素最多可能是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】元素周期表是元素周期律的具体表现,是学习和研究化学的重要工具.下图是元素周期表的一部分:
请完成下列填空:
(1)元素①的简单气态氢化物的空间构型是_____________ 。
(2)元素②、③、④的简单离子半径由大到小的顺序为_____________ (用离子符号表示)。
(3) 元素在周期表中的位置是
元素在周期表中的位置是____ ,最后一行元素的基态原子中只有1个未成对电子的是_____ (填元素名称)。
(4)元素④、⑤非金属性更强的是________ (填元素符号),请从原子结构的角度解释:_________ 。并写出一个证明它们非金属性强弱的化学反应方程式________________________ 。
(5)表中第一电离能最大的元素是_____________ ,理由是__________________________ 。
| ① | ② | ||||
| ③ | ④ | ⑤ | ⑥ | ||
 |  |  |  |  |
(1)元素①的简单气态氢化物的空间构型是
(2)元素②、③、④的简单离子半径由大到小的顺序为
(3)
 元素在周期表中的位置是
元素在周期表中的位置是(4)元素④、⑤非金属性更强的是
(5)表中第一电离能最大的元素是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)基态Ge原子价电子排布图为_______ 、属于_______ 区。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ;二锗酸钠:
;二锗酸钠: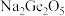 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。
① 中阴离子的空间结构是
中阴离子的空间结构是_______ 。
②推测1mol 中含有的σ键的数目是
中含有的σ键的数目是_______ (用 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。
(3)利用离子液体[EMIM][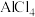 ]可电沉积还原金属Ge,其熔点只有7℃,其中
]可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
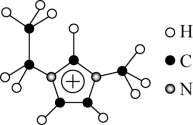
①该物质的晶体类型是_______ 。
② 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是_______ 。
(4)独立的 分子中H−N−H的键角为107.3°,
分子中H−N−H的键角为107.3°, 离子中H−N−H的键角
离子中H−N−H的键角_______ 107.3°(填“大于”、“小于”或“等于”)。
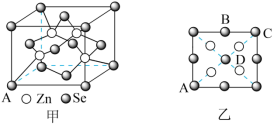
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,该晶胞中两个Zn原子之间的间距是_______ ;乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为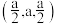 ,则D点坐标为
,则D点坐标为_______ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_______ (只列出计算式)。
(1)基态Ge原子价电子排布图为
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ;二锗酸钠:
;二锗酸钠: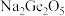 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。①
 中阴离子的空间结构是
中阴离子的空间结构是②推测1mol
 中含有的σ键的数目是
中含有的σ键的数目是 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。(3)利用离子液体[EMIM][
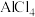 ]可电沉积还原金属Ge,其熔点只有7℃,其中
]可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是(4)独立的
 分子中H−N−H的键角为107.3°,
分子中H−N−H的键角为107.3°, 离子中H−N−H的键角
离子中H−N−H的键角(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,该晶胞中两个Zn原子之间的间距是
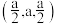 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】自然界中存在大量的金属元素,在工农业生产中有着广泛的应用。回答下列问题:
(1)下列有关微粒性质的排列顺序错误的是___________。
(2)基态Ni原子核外电子运动状态有___________ 种,其核外电子排布式中未成对电子数为___________ 个。
(3)钌−多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是___________ ,N原子的杂化类型为___________ 。

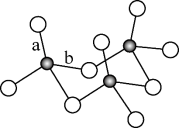
(4)SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___________ ;该结构中S−O键长有两类,一类键长约140pm,另一类键长约为160pm,较长的键为___________ (填图中字母),该分子中含有___________ 个σ键。
(1)下列有关微粒性质的排列顺序错误的是___________。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
| C.离子半径:O2−>Na+>Mg2+ | D.原子的未成对电子数:Mn>Si>Cl |
(3)钌−多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是

(4)SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】近年来,我国的材料技术如陶瓷基复合材料氮化硼(BN)、太阳能电池材料砷化镓(GaAs)、新型储氢材料、光电材料等发展迅猛,请按要求回答下列问题。
(1)基态N原子的轨道表示式为_______ ,B与N的电负性由大到小的顺序为_______ (用元素符号表示)。
(2)基态砷原子的价层电子排布式为_______ ,占据最高能级的电子所在的原子轨道为_______ 形。
(3)硼氢化钠(NaBH4,其中氢元素显-1价)是研究最广泛的储氢材料之一,硼原子在成键时,能将一个2s电子激发进入2p能级参与形成化学键,该过程形成的原子光谱为_______ 光谱(填“吸收”或“发射”),与硼处于同一周期的元素中,第一电离能大于硼的主族元素有_______ 种。
(4)铜配合物在光电材料方面的应用非常广泛,其中基态Cu原子的核外电子排布式为_______ ,Cu在元素周期表中属于_______ 区。
(1)基态N原子的轨道表示式为
(2)基态砷原子的价层电子排布式为
(3)硼氢化钠(NaBH4,其中氢元素显-1价)是研究最广泛的储氢材料之一,硼原子在成键时,能将一个2s电子激发进入2p能级参与形成化学键,该过程形成的原子光谱为
(4)铜配合物在光电材料方面的应用非常广泛,其中基态Cu原子的核外电子排布式为
您最近一年使用:0次



