废旧锌锰电池中的黑锰粉含有MnO2、MnO(OH)、NH4Cl和少量ZnCl2、Fe2O3及炭黑等,为了保护环境、充分利用锰资源,通过如下流程制备MnSO4。

回答下列问题:
(1)Mn的原子结构示意图为___________ 。
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因___________ 。
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、___________ 、洗涤、干燥,得NH4Cl固体。

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为___________ 。
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是___________ ,实验II中H2O2的作用是___________ 。
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是___________ 。
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加___________ (填试剂),观察到___________ (填现象)。

回答下列问题:
(1)Mn的原子结构示意图为
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加
2023·陕西咸阳·二模 查看更多[3]
(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)陕西省咸阳市2023届高三下学期模拟检测(二)理综化学试题
更新时间:2023-03-23 11:34:45
|
相似题推荐
【推荐1】电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。从腐蚀废液中回收铜,并重新获得FeCl3溶液的处理流程如下:

(1)FeCl3溶液腐蚀绝缘板上的铜箔的离子方程式是_______ 。
(2)步骤(Ⅰ)中分离操作名称是_______ 。
(3)沉淀B中主要含有_______ ,气体D的化学式是_______ 。
(4)在滤液A中加入NaOH溶液,现象是_______ ,用化学方程式表示最后现象出现的原因_______ 。
(5)取少量最后所得溶液于试管中,然后滴加_______ (写名称),溶液,若变红,则证明有Fe3+存在。
(6)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出换成H2O2后反应的离子方程式:_______ 。

(1)FeCl3溶液腐蚀绝缘板上的铜箔的离子方程式是
(2)步骤(Ⅰ)中分离操作名称是
(3)沉淀B中主要含有
(4)在滤液A中加入NaOH溶液,现象是
(5)取少量最后所得溶液于试管中,然后滴加
(6)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出换成H2O2后反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A为一种常见的金属单质,B、E、F、G是含有A元素的常见化合物。回答下列问题:

(1)写出化学式:B_______ ,F_______ 。
(2)写出E到F转化过程的化学方程式_______ 。
(3)检验G溶液中金属阳离子的常用试剂为_______ ,证明该离子存在的现象为_______ 。
(4)写出G到B转化过程的化学方程式_______ ,该反应中还原剂为_______ 。
(5)若标准状况下A与盐酸反应产生44.8L气体,则消耗A的质量为_______ g。

(1)写出化学式:B
(2)写出E到F转化过程的化学方程式
(3)检验G溶液中金属阳离子的常用试剂为
(4)写出G到B转化过程的化学方程式
(5)若标准状况下A与盐酸反应产生44.8L气体,则消耗A的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某兴趣小组用部分氧化的FeSO4为原料,制取高纯度的Fe2O3,并测定产品中铁元素含量,主要操作步骤如下∶
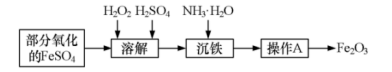
(1)写出加入H2O2发生反应的离子方程式∶___________ 。
(2)简述检验溶解过程中Fe2+是否已被完全氧化成Fe3+的实验操作∶___________ (可选择的试剂∶ 酸性KMnO4溶液、KSCN 溶液、氯水)。
(3)操作A包括___________ 、洗涤、___________ ; 简述检验Fe(OH)3是否洗净的操作∶___________ 。
(4)准确称取4.00gFe2O3产品,经酸溶、还原为Fe2+,准确配成100mL溶液。取25.00mL于锥形瓶中,加入20.50mL 0.10 mol·L-1 K2Cr2O7溶液恰好完全反应。(假设K2Cr2O7不与杂质反应,与Fe2+反应为∶ )
)
① 配成 100mL 溶液所用的主要仪器有∶玻璃棒、烧杯、___________ 。
②产品中铁元素的含量为___________ 。

(1)写出加入H2O2发生反应的离子方程式∶
(2)简述检验溶解过程中Fe2+是否已被完全氧化成Fe3+的实验操作∶
(3)操作A包括
(4)准确称取4.00gFe2O3产品,经酸溶、还原为Fe2+,准确配成100mL溶液。取25.00mL于锥形瓶中,加入20.50mL 0.10 mol·L-1 K2Cr2O7溶液恰好完全反应。(假设K2Cr2O7不与杂质反应,与Fe2+反应为∶
 )
)① 配成 100mL 溶液所用的主要仪器有∶玻璃棒、烧杯、
②产品中铁元素的含量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
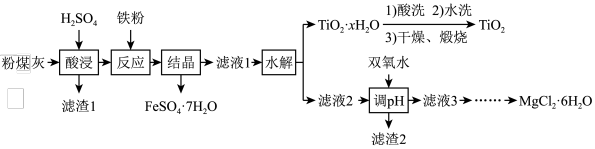
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO 和一种阳离子。
和一种阳离子。
②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有___________ (任写一种)。
(2)钛元素发生“水解”反应的离子方程式为___________ 。
(3)加入双氧水的目的是___________ 。滤渣2中的成分分别为Al(OH)3和___________ ,Al(OH)3沉淀完全时(溶液中离子浓度小于10−5mol/L),溶液中的c(OH−)为___________ 。
(4)将MgCl2·6H2O制成无水MgCl2时应注意___________ 。
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因___________ 。

已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO
 和一种阳离子。
和一种阳离子。②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有
(2)钛元素发生“水解”反应的离子方程式为
(3)加入双氧水的目的是
(4)将MgCl2·6H2O制成无水MgCl2时应注意
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系:
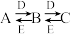
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,且B为白色沉淀物,则A的化学式为____ ,D的化学式为_____ ;A、C反应生成B的离子方程式为___________ 。
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因___________ ,C与E反应生成B的化学方程式为________ 。
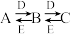
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,且B为白色沉淀物,则A的化学式为
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E、F六种常见物质存在如图所示转化关系(部分生成物和反应条件略去)。

(1)若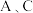 均为氧化物:
均为氧化物:
①若 为单质,向
为单质,向 溶液中滴加
溶液中滴加 溶液,溶液显红色,
溶液,溶液显红色, 为
为___________ (填化学式);写出 的离子方程式:
的离子方程式:___________ 。
②若 是含钠正盐,其水溶液呈碱性,
是含钠正盐,其水溶液呈碱性, 是一种温室气体,写出
是一种温室气体,写出 的一条用途:
的一条用途:___________ ; 的水溶液呈碱性的原因为
的水溶液呈碱性的原因为___________ (用离子方程式表示)。
(2)若 为固体氧化物,
为固体氧化物, 为气体单质,
为气体单质, 进行焰色试验时,火焰呈黄色,写出化合物
进行焰色试验时,火焰呈黄色,写出化合物 的电子式:
的电子式:___________ ;每生成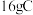 ,转移的电子的物质的量为
,转移的电子的物质的量为___________  。
。
(3)若 为
为 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。

(1)若
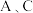 均为氧化物:
均为氧化物:①若
 为单质,向
为单质,向 溶液中滴加
溶液中滴加 溶液,溶液显红色,
溶液,溶液显红色, 为
为 的离子方程式:
的离子方程式:②若
 是含钠正盐,其水溶液呈碱性,
是含钠正盐,其水溶液呈碱性, 是一种温室气体,写出
是一种温室气体,写出 的一条用途:
的一条用途: 的水溶液呈碱性的原因为
的水溶液呈碱性的原因为(2)若
 为固体氧化物,
为固体氧化物, 为气体单质,
为气体单质, 进行焰色试验时,火焰呈黄色,写出化合物
进行焰色试验时,火焰呈黄色,写出化合物 的电子式:
的电子式: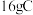 ,转移的电子的物质的量为
,转移的电子的物质的量为 。
。(3)若
 为
为 ,写出
,写出 与
与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D四种元素核电荷数均小于18。A元素原子核内无中子,B元素的原子L层电子数是K层电子数的3倍,C元素原子的M层电子数比K层电子数多1个,D2-离子比C3+离子多一个电子层。请回答:
(1)写出元素名称:A___ 、B___ 、C___ 、D___ 。
(2)画处C3+离子结构示意图_____ 。
(3)画出D2-离子的电子式_____ 。
(4)写出B、C形成的化合物的化学式____ 。
(1)写出元素名称:A
(2)画处C3+离子结构示意图
(3)画出D2-离子的电子式
(4)写出B、C形成的化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】已知A、B、C三种元素的原子中,质子数:A<B<C,且都小于18,A元素原子的最外层电子数是次外层电子数的4倍;B元素的原子核外M层电子数是L层电子数的一半;C元素原子的次外层电子数比最外层电子数多3。试回答下列问题:
(1)写出三种元素的名称和符号:A___________ ,B___________ ,C___________ 。
(2)写出三种元素的原子核外电子排布式A___________ ,B___________ ,C___________ 。
(1)写出三种元素的名称和符号:A
(2)写出三种元素的原子核外电子排布式A
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】三草酸合铁酸钾可用氯化铁与草酸钾混合直接合成:FeCl3+3K2C2O4=K3[Fe(C2O4)3]+3KCl
(1)FeCl3中铁离子基态核外电子排布式为___________ 。
(2)上述反应涉及的主族元素中,第一电离能最小的是___________ (填元素符号)。
(3)K3[Fe(C2O4)3]中化学键的类型有___________ 。
A.离子键 B.共价键 C.氢键 D.配位键 E.范德华力
(4)草酸(H2C2O4)中C原子的杂化类型为___________ ,1mol草酸(H2C2O4)中含有σ键的数目为___________ 。
(5)与 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。 中存在大π键,大π键通常表达为(
中存在大π键,大π键通常表达为(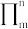 )
) 中存在大π键为
中存在大π键为___________ 。
(1)FeCl3中铁离子基态核外电子排布式为
(2)上述反应涉及的主族元素中,第一电离能最小的是
(3)K3[Fe(C2O4)3]中化学键的类型有
A.离子键 B.共价键 C.氢键 D.配位键 E.范德华力
(4)草酸(H2C2O4)中C原子的杂化类型为
(5)与
 互为等电子体的一种分子为
互为等电子体的一种分子为 中存在大π键,大π键通常表达为(
中存在大π键,大π键通常表达为(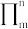 )
) 中存在大π键为
中存在大π键为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学制取氧气,并回收提纯氯化钾和二氧化锰的流程如图。
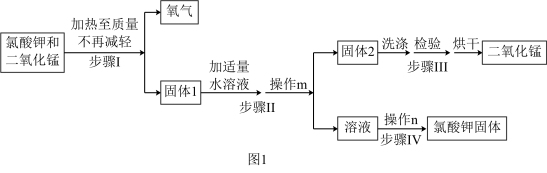
(1)写出上述流程中制取氧气的化学方程式___ 。
(2)步骤Ⅱ中加适量水的目的___ (填编号)。
a提高实验效率 b.保证固体1全部溶解
c.加快固体溶解速度 d.减少固体2的损失
(3)步骤Ⅱ中的操作m应选择图中____ 装置(选填“甲”或“乙”,下同),步骤Ⅳ中的操作n应选择图中___ 装置,操作n中玻璃棒的作用是___ 。
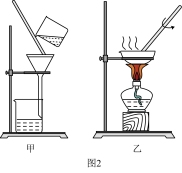
(4)实验结束后,称得回收到的二氧化锰的质量比原来氯酸钾中的大,可能的原因有___ (写一点)。
(5)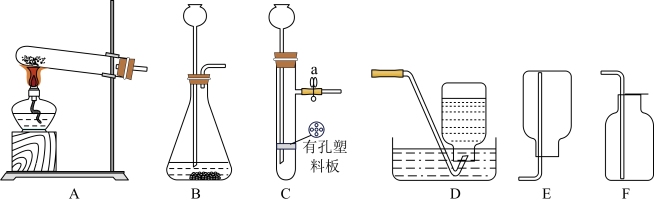
该同学制取氧气时可选用的发生装置是___ ,收集装置是___ (均填字母)。

(1)写出上述流程中制取氧气的化学方程式
(2)步骤Ⅱ中加适量水的目的
a提高实验效率 b.保证固体1全部溶解
c.加快固体溶解速度 d.减少固体2的损失
(3)步骤Ⅱ中的操作m应选择图中

(4)实验结束后,称得回收到的二氧化锰的质量比原来氯酸钾中的大,可能的原因有
(5)

该同学制取氧气时可选用的发生装置是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置_______ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置_______ 。
(2)从碘水中分离出I2,选择装置______ ,该分离方法的名称为________ 。
(3)装置A中仪器①的名称是________ ,装置B在分液时为使液体顺利滴下,应进行的具体操作是______________________________________________ 。

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中仪器①的名称是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】请根据要求回答问题:
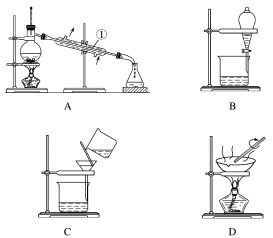
(1)从氯化钾溶液中得到氯化钾固体,选择装置_________ (填代表装置的字母,下同);除去自来水中Cl-等杂质,选择装置_________ 。
(2)从油水混合物中分离出植物油,选择装置_________ ,该分离方法的名称为_________ 。
(3)装置A中①的名称是_________ ,进水的方向是从_________ 口进水。装置B在分液时打开活塞后,下层液体从_________ ,上层液体从_________ 。
(4)实验时,仪器A中除加入溶液外,还需加入少量_________ ,其作用是_________ 。

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从油水混合物中分离出植物油,选择装置
(3)装置A中①的名称是
(4)实验时,仪器A中除加入溶液外,还需加入少量
您最近一年使用:0次



