下表列出了①~⑩十种元素在周期表中的位置,请回答下列问题:
(1)表中10种元素中,某元素的原子最外层电子数是其核外电子层数的3倍,其中子数为10,该核素符号是___________ 。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是___________ 。(用离子符号表示)
(3)由元素①④形成的具有强氧化性的物质的电子式为___________ ;由元素⑥和⑨形成化合物乙,用电子式表示物质乙的形成过程___________ 。
(4)华为 技术遥遥领先,镓
技术遥遥领先,镓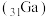 的化合物氮化镓
的化合物氮化镓 和砷化镓
和砷化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为
作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为___________ ,砷的最高价氧化物的水化物的化学式为___________ 。
(5)可以比较⑤、⑥两元素金属性强弱的是___________。
(6)喝温水解口渴也能解体渴,但喝冰水效果差一些,这是有科学依据的。当温度较低时,水是以大分子水团形式存在的;当温度较高时水以小分子水团形式存在的,小分子水团更有利于人体吸收。当温度升高时主要破坏了水分子之间的___________ 。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
(1)表中10种元素中,某元素的原子最外层电子数是其核外电子层数的3倍,其中子数为10,该核素符号是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是
(3)由元素①④形成的具有强氧化性的物质的电子式为
(4)华为
 技术遥遥领先,镓
技术遥遥领先,镓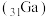 的化合物氮化镓
的化合物氮化镓 和砷化镓
和砷化镓 作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为
作为第三代半导体材料,具有耐高温、耐高电压等特性。镓在元素周期表中位置为(5)可以比较⑤、⑥两元素金属性强弱的是___________。
| A.将⑤的单质投入到⑥的盐溶液中 |
| B.比较这两种元素最高价氧化物的水化物的碱性 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
(6)喝温水解口渴也能解体渴,但喝冰水效果差一些,这是有科学依据的。当温度较低时,水是以大分子水团形式存在的;当温度较高时水以小分子水团形式存在的,小分子水团更有利于人体吸收。当温度升高时主要破坏了水分子之间的
更新时间:2024-02-03 21:31:23
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
【推荐1】现有部分短周期元素的性质或原子结构如下表:
回答下列问题:
(1)A元素在周期表中的位置___________ 。
(2)B元素的最高价氧化物对应的水化物与C元素的最高价氧化物对应的水化物反应的离子反应方程式是___________ 。
(3)单质B与单质D反应所得产物的电子式为___________ 。
(4)元素D与元素A相比,非金属性较强的是___________ (用元素符号表示),下列表述中不能证明这一事实的是___________ (填选项序号)。
a.一定条件下D和A的单质都能与钠反应
b.D的氢化物比A的氢化物稳定
c.D单质能与A的氢化物反应生成A单质
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价为+7 |
(1)A元素在周期表中的位置
(2)B元素的最高价氧化物对应的水化物与C元素的最高价氧化物对应的水化物反应的离子反应方程式是
(3)单质B与单质D反应所得产物的电子式为
(4)元素D与元素A相比,非金属性较强的是
a.一定条件下D和A的单质都能与钠反应
b.D的氢化物比A的氢化物稳定
c.D单质能与A的氢化物反应生成A单质
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】根据表中的10种元素,完成以下各小题。
(1)地壳中含量最多的元素是____ (填名称)。化学性质最不活泼的元素是____ (填元素符号)。
(2)I离子的电子式为____ 。
(3)A与B相比,原子半径较小的是____ (填元素符号)。
(4)在最高价氧化物对应的水化物中,碱性最强的碱是____ (填化学式),酸性最强的酸是____ (填化学式)。呈两性的元素是____ (填字母编号)。
(5)气体单质有颜色的是____ ,单质还原性最强的是____ 。
(6)将形状相同的F、G单质分别投入到相同体积和相同浓度的盐酸中,试预测实验结果:____ 与盐酸反应更剧烈;从原子结构解释上述现象的原因:____ 。
(7)向I形成的钠盐溶液中通入J的单质出现黄色浑浊,可证明非金属性____ 强于____ (填元素符号),反应的离子方程式为____ 。
| 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | A | B | C | D | ||||
| 3 | E | F | G | H | I | J |
(2)I离子的电子式为
(3)A与B相比,原子半径较小的是
(4)在最高价氧化物对应的水化物中,碱性最强的碱是
(5)气体单质有颜色的是
(6)将形状相同的F、G单质分别投入到相同体积和相同浓度的盐酸中,试预测实验结果:
(7)向I形成的钠盐溶液中通入J的单质出现黄色浑浊,可证明非金属性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E是原子序数依次增大的五种短周期元素。B、E同主族,且满足最高正化合价+最低负化合价=0;A与C、D与C之间都能形成原子个数之比分别为2∶1和1∶1的两种化合物。试回答下列有关问题:
(1)在A2C2分子中含有的化学键是________ 和________ 。
(2)C与D形成化合物的电子式分别为________ 、________ 。
(3)实验室可用由B、C、D组成的化合物为反应物之一制取由A、C、D组成的化合物,反应的化学方程式为________ 。
(4)写出比E原子序数小1的元素形成的单质与A、C、D形成的化合物的水溶液反应的离子方程式:________________ 。
(1)在A2C2分子中含有的化学键是
(2)C与D形成化合物的电子式分别为
(3)实验室可用由B、C、D组成的化合物为反应物之一制取由A、C、D组成的化合物,反应的化学方程式为
(4)写出比E原子序数小1的元素形成的单质与A、C、D形成的化合物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素周期表反映了元素之间的内在联系,学习、研究和应用化学的重要工具。如图列出①~⑤五种元素在周期表中的位置。
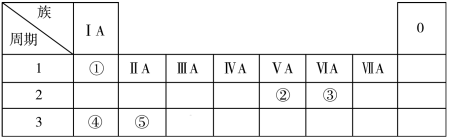
回答下列问题:
(1)⑤的元素名称是________ 。
(2)①~⑤五种元素中,原子半径最大的是________ (填元素符号)。
(3)②和③两种元素的最简单氢化物中,稳定性较强的是________ (填化学式)。
(4)②和④两种元素的最高价氧化物的水化物发生反应,其离子方程式是________ 。
(5)由图可知金属性:④>⑤。原因是在同一周期中,元素的原子核外电子层数相同,从左到右,________ ,原子半径逐渐减小,失电子能力逐渐减弱。因此,金属性逐渐减弱。

回答下列问题:
(1)⑤的元素名称是
(2)①~⑤五种元素中,原子半径最大的是
(3)②和③两种元素的最简单氢化物中,稳定性较强的是
(4)②和④两种元素的最高价氧化物的水化物发生反应,其离子方程式是
(5)由图可知金属性:④>⑤。原因是在同一周期中,元素的原子核外电子层数相同,从左到右,
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表列出了①~⑥六种元素在元素周期表中的位置:
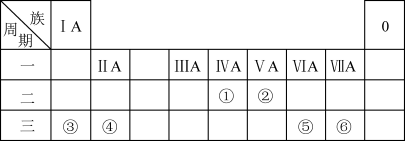
请按要求回答下列问题:
(1)元素②的单质的电子式是___________ 。
(2)元素⑤与⑥的简单气态氢化物的热稳定性比较:___________ (填化学式)。
(3)这六种元素中,位于第三周期且原子半径最小的元素的原子结构示意图为___________ 。
(4)这六种元素中,能与氧结合,生成物可做耐火材料的是___________ (填元素符号)。
(5)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为___________ ;向上述反应后的溶液中再通入元素⑥的单质,发生反应的化学方程式为___________ 。

请按要求回答下列问题:
(1)元素②的单质的电子式是
(2)元素⑤与⑥的简单气态氢化物的热稳定性比较:
(3)这六种元素中,位于第三周期且原子半径最小的元素的原子结构示意图为
(4)这六种元素中,能与氧结合,生成物可做耐火材料的是
(5)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
(1) ①的元素符号是__________
(2) ②和⑥两种元素的原子半径大小关系:_________ (填“>”或“<”);
(3) ③和⑤两种元素的金属性强弱关系:________ (填“>”或“<”);
(4)③和⑦形成的化合物属于_________ (填“离子化合物”或“共价化合物”);写出该化合物的电子式为:______________________ ;
(5)写出元素②在周期表中的位置_______________________ ;
(6)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:_____________ 。
| ⅠA | 0 | ||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | B | ① | ② | Ne | |||||
| 3 | ③ | ④ | ⑤ | Si | ⑥ | ⑦ | |||
(2) ②和⑥两种元素的原子半径大小关系:
(3) ③和⑤两种元素的金属性强弱关系:
(4)③和⑦形成的化合物属于
(5)写出元素②在周期表中的位置
(6)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A是形成化合物种类最多的元素;C原子能形成分别含10电子、18电子的两种阴离子,且C与F位于同一主族;D单质投入冷水中反应缓慢,投入沸水中迅速产生气泡;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。请回答下列问题:
(1)B位于周期表第_______ 周期第_______ 族。
(2)元素M位于E与F元素之间,且M的单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为_______ (用化学式表示)。
(3)若选择三种试剂设计实验能证明非金属性:B>A>M,用化学方程式表示实验原理:_______ 。
(4)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为_______ (用化学式表示)。
(5)下列实验方法能证明D与E的金属性强弱关系的是_______ (填字母)。
A.比较D和E的单质分别与稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物
(1)B位于周期表第
(2)元素M位于E与F元素之间,且M的单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为
(3)若选择三种试剂设计实验能证明非金属性:B>A>M,用化学方程式表示实验原理:
(4)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为
(5)下列实验方法能证明D与E的金属性强弱关系的是
A.比较D和E的单质分别与稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表为某元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素______ (填元素编号),非金属性最强的元素是____________ (填元素编号)。
(2)该表中金属性最强的元素单质与水反应的离子方程式为_____________ 。
(3)①③⑤三种元素的最高价氧化物水化物中,碱性最强的是______________ (填物质的化学式)。
(4)④⑤⑧三种元素的原子半径由大到小的顺序为_______________ (用元素符号回答)。
(5)元素⑧的最高价氧化物对应的水化物是_______________ (填化学式),元素②⑤的最高价氧化物对应的水化物反应的离子方程式是_______________ 。
族 周期 | ⅠA | ⅡΑ | ⅢΑ | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ⑪ | |||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(2)该表中金属性最强的元素单质与水反应的离子方程式为
(3)①③⑤三种元素的最高价氧化物水化物中,碱性最强的是
(4)④⑤⑧三种元素的原子半径由大到小的顺序为
(5)元素⑧的最高价氧化物对应的水化物是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:
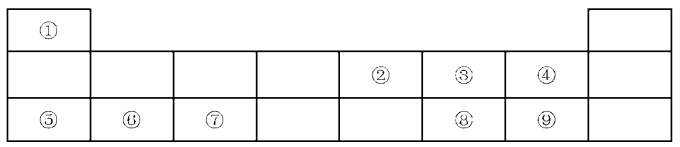
(1)⑥在元素周期表中的位置是______ ;②、③、④三种元素的原子半径最小的是______ (写元素符号)。①分别与③、④形成化合物的稳定性强弱的顺序是______ (用化学式表示)。
(2)①、③、⑤形成的化合物中含有化学键的类型是______ ;写出①和②形成的化合物的电子式______ ;⑤和⑧可形成离子化合物,用电子式表示其形成过程______ 。
(3)⑤和⑦分别形成的最高价氧化物对应的水化物发生反应的离子方程式是______ 。
(4)从原子结构的角度解释⑧和⑨非金属性的强弱______ 。
(5)⑤、⑥和⑦形成的简单离子的半径大小顺序为______ ;下列事实能判断⑤和⑥的金属性强弱的是______ (填字母,下同)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小

(1)⑥在元素周期表中的位置是
(2)①、③、⑤形成的化合物中含有化学键的类型是
(3)⑤和⑦分别形成的最高价氧化物对应的水化物发生反应的离子方程式是
(4)从原子结构的角度解释⑧和⑨非金属性的强弱
(5)⑤、⑥和⑦形成的简单离子的半径大小顺序为
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】元素周期表对化学的发展有很大影响,下表是元素周期表的一部分,数字①~⑩代表十种常见的短周期元素,请按题目要求回答下列问题:

(1)①在周期表中的位置为___________ 。
(2)写出②最高价氧化物的电子式___________ 。
(3)在②~⑤元素中,原子半径最大的是___________ (填化学符号)。
(4)比较④、⑤、⑥、⑦离子的半径大小___________ (用化学符号表示且用“>”连接)。
(5)以上这些元素中,最不活泼的金属元素是___________ (填化学符号,下同),这些元素的最高价氧化物对应的水化物中,碱性最强的是___________ ,呈两性的氢氧化物是___________ ,写出二者之间相互反应的化学方程式___________ 。
(6)⑥的金属性强于⑦,试用实验证明(简述简单操作、主要现象和结论)___________ 。用原子结构解释原因:二者在同一周期,核电荷数依次增多,___________ 失电子能力逐渐减弱,因此金属性逐渐减弱。
(7)砷( )是人体必需的微量元素,与③同一主族,
)是人体必需的微量元素,与③同一主族, 原子比③原子多两个电子层,则砷的原子结构示意图为
原子比③原子多两个电子层,则砷的原子结构示意图为___________ ,该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是___________ (用化学符号表示且用“>”连接)。

(1)①在周期表中的位置为
(2)写出②最高价氧化物的电子式
(3)在②~⑤元素中,原子半径最大的是
(4)比较④、⑤、⑥、⑦离子的半径大小
(5)以上这些元素中,最不活泼的金属元素是
(6)⑥的金属性强于⑦,试用实验证明(简述简单操作、主要现象和结论)
(7)砷(
 )是人体必需的微量元素,与③同一主族,
)是人体必需的微量元素,与③同一主族, 原子比③原子多两个电子层,则砷的原子结构示意图为
原子比③原子多两个电子层,则砷的原子结构示意图为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表为元素周期表中的一部分,表中列出8种元素在周期表中的位置,按要求回答下列问题。
(1)在①~⑧元素中化学性质最不活泼的元素的名称是____ ,金属性最强的元素的名称是____ 。
(2)③、④、⑥三种元素中的原子半径最小的是_____________ (填元素符号)。
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是____ (用离子符号填写)。
(4)④与⑥形成的化合物的电子式为_____________ 。
(5)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑥ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
(1)在①~⑧元素中化学性质最不活泼的元素的名称是
(2)③、④、⑥三种元素中的原子半径最小的是
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是
(4)④与⑥形成的化合物的电子式为
(5)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。针对表中①~⑩号元素回答下列问题。______ ,⑨元素的原子结构示意图为______ 。
(2)②、③、④、⑤、⑥这五种元素分别形成的简单离子中离子半径最小的是______ (填离子符号)。
(3)镓(Ga)与⑥同主族,其氢氧化物为两性氢氧化物,请写出氢氧化镓与NaOH反应的化学方程式______ 。
(4)表中元素⑦和⑩的最高价氧化物对应水化物的酸性最强的是______ (填化学式)。
(5)元素④和⑥相比,金属性较强的是______ (填元素符号),下列能证明这一事实的有______ (填序号)。
A.在化合物中④的化合价比⑥的低
B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强
D.④单质的熔点比⑥单质的低
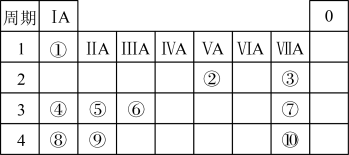
(2)②、③、④、⑤、⑥这五种元素分别形成的简单离子中离子半径最小的是
(3)镓(Ga)与⑥同主族,其氢氧化物为两性氢氧化物,请写出氢氧化镓与NaOH反应的化学方程式
(4)表中元素⑦和⑩的最高价氧化物对应水化物的酸性最强的是
(5)元素④和⑥相比,金属性较强的是
A.在化合物中④的化合价比⑥的低
B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强
D.④单质的熔点比⑥单质的低
您最近一年使用:0次



