Ⅰ.硫是一种重要的非金属元豢,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是______ ,最高能级电子所在的原子轨道为______ 形。
(2)比较沸点高低: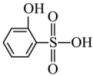
______ (填“>”或“<”)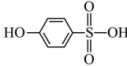 ,并解释原因:
,并解释原因:____________ 。
(3)ZnS晶胞如图所示: ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为______ pm。
Ⅱ.锂离子电池充放电过程中,正极材料晶胞的组成变化如图所示。 的空间构型为
的空间构型为______ ,且磷氧键键能较大,锂离子嵌入和脱出时,磷酸铁锂的空间骨架不易发生形变,具有良好的循环稳定性。
②正极材料在 和
和 之间转化时,经过中间产物
之间转化时,经过中间产物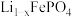 。
。 转化为
转化为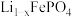 的过程中,每摩晶胞转移电子的物质的量为
的过程中,每摩晶胞转移电子的物质的量为______ 摩。
(1)基态硫原子的价层电子排布图是
(2)比较沸点高低:

 ,并解释原因:
,并解释原因:(3)ZnS晶胞如图所示:
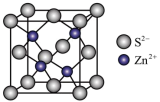
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为Ⅱ.锂离子电池充放电过程中,正极材料晶胞的组成变化如图所示。
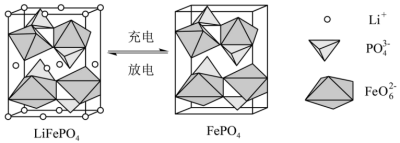
 的空间构型为
的空间构型为②正极材料在
 和
和 之间转化时,经过中间产物
之间转化时,经过中间产物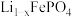 。
。 转化为
转化为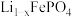 的过程中,每摩晶胞转移电子的物质的量为
的过程中,每摩晶胞转移电子的物质的量为
23-24高三下·海南·阶段练习 查看更多[2]
更新时间:2024-04-04 09:41:16
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】铁及其化合物在生产和生活中具有广泛的用途。请回答下列问题。
(1)铁制品暴露在潮湿空气中容易发生腐蚀,通过图甲所示装置可验证铁钉是否发生电化学腐蚀,正极反应式是___________ 。

(2)利用图乙装置可模拟工业生产高铁酸盐,阳极反应为___________ ,阴极区的溶液
___________ (填“增大”“减小”或“不变”)。利用高铁酸盐可制作新型可充电电池,该电池的总反应为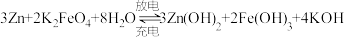 ,充电时阳极反应为
,充电时阳极反应为___________ ,放电时每转移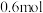 电子,正极有
电子,正极有___________ 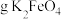 被还原。
被还原。
(1)铁制品暴露在潮湿空气中容易发生腐蚀,通过图甲所示装置可验证铁钉是否发生电化学腐蚀,正极反应式是

(2)利用图乙装置可模拟工业生产高铁酸盐,阳极反应为

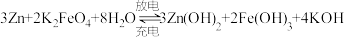 ,充电时阳极反应为
,充电时阳极反应为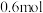 电子,正极有
电子,正极有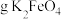 被还原。
被还原。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】化学能在一定条件下可转化为电能。
(1)某原电池装置如图所示。其中,Zn电极为原电池的_______ 极(填“正”或“负”),电极反应式是_______ 。能证明化学能转化为电能的实验现象是:_______ 、铜片上产生大量气泡。
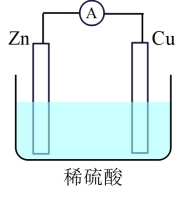
当铜表面析出22.4mL氢气(标准状况)时,导线中通过了_______ mol电子。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:

①NiO电极上发生的是_______ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从_______ 电极流向_______ 电极(填“NiO”或“Pt”)。
③Pt电极上的电极反应式为_______ 。
(1)某原电池装置如图所示。其中,Zn电极为原电池的

当铜表面析出22.4mL氢气(标准状况)时,导线中通过了
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:

①NiO电极上发生的是
②外电路中,电子的流动方向是从
③Pt电极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成原电池。
①H2SO4所含化学键为____________ ;
②若有0.4mole-流过导线,则理论上负极质量减少____________ g;
③若将稀硫酸换成硫酸铜溶液,电极质量增加的是____________ (填“锌极”或“铜极”),原因是____________ (用电极方程式表示);
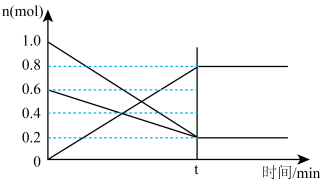
(2)①T1温度时,在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g) 2NO2(g)。容器中各反应物和生成物的物质的量随时间变化如图所示。下列能判断达到化学平衡的是
2NO2(g)。容器中各反应物和生成物的物质的量随时间变化如图所示。下列能判断达到化学平衡的是____________
A.反应中NO与O2的物质的量之比为2:1
B.混合气体的总质量不随时间的变化而变化
C.单位时间内每消耗2nmolNO2,同时生成nmolO2
D.2v正(O2)=v逆(NO)
E.混合气体的压强不变
②0~t时间段,反应速率v(NO2)=____________ 。
①H2SO4所含化学键为
②若有0.4mole-流过导线,则理论上负极质量减少
③若将稀硫酸换成硫酸铜溶液,电极质量增加的是
(2)①T1温度时,在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g)
 2NO2(g)。容器中各反应物和生成物的物质的量随时间变化如图所示。下列能判断达到化学平衡的是
2NO2(g)。容器中各反应物和生成物的物质的量随时间变化如图所示。下列能判断达到化学平衡的是
A.反应中NO与O2的物质的量之比为2:1
B.混合气体的总质量不随时间的变化而变化
C.单位时间内每消耗2nmolNO2,同时生成nmolO2
D.2v正(O2)=v逆(NO)
E.混合气体的压强不变
②0~t时间段,反应速率v(NO2)=
您最近一年使用:0次
【推荐1】X、Y、Z、M、Q是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如表所示:
(1)X最外层电子的轨道表达式是 ___________ 。
(2)M元素的名称是___________ 。
(3)Z元素基态原子中能量最高的电子的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(4)小范同学写了基态原子P的两个价电子的表达形式,分析其分别违背了什么原理:
①3s13p4:___________ ,
②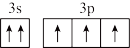 :
:___ 。
(5)元素Q可形成Q2+和Q3+,其中较稳定的是Q3+,原因是___ 。
| 元素 | 相关信息 |
| X | 次外层电子数是最外层电子数的 |
| Y | 形成的氧化物和强酸、强碱都可以反应 |
| Z | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| M | 前4周期元素原子核外电子排布中未成对电子数最多的元素 |
| Q | 基态原子核外有7个能级上有电子且能量最高的能级上有6个电子 |
(2)M元素的名称是
(3)Z元素基态原子中能量最高的电子的电子云在空间有
(4)小范同学写了基态原子P的两个价电子的表达形式,分析其分别违背了什么原理:
①3s13p4:
②
 :
:(5)元素Q可形成Q2+和Q3+,其中较稳定的是Q3+,原因是
您最近一年使用:0次
【推荐2】有机-无机杂化钙钛矿卤化物(ABX3)材料,因其具有优异的光电性能,在太阳能电池领域引起了广泛的关注,如CH3NH3PbI3、(C4H9NH3)2PbBr4等。
(1)下列表示碳原子激发态轨道表示式的是_______ 。
A.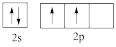 B.
B.
C. D.
D.
(2)N原子和O原子第二电离能N_______ O (填“>”或“<”)。
(3)CH3NH 中氮原子的杂化方式为
中氮原子的杂化方式为_______ ;甲胺(CH3NH2)与乙烷摩尔质量相同,甲胺的沸点比乙烷的沸点_______ (填“高”或“低”);甲胺结合质子的能力比NH3结合质子的能力强,原因是_______ 。
(4)某钙钛矿晶胞结构如图1,沿x、y、z轴方向的投影均为图2。与Pb2+、CH3NH 距离最近I- 的数目分别是
距离最近I- 的数目分别是_______ 、_______ 。设钙钛矿的最简式的式量为Mr,晶体密度为ρg·cm-3,则晶胞中相邻两个Pb2+之间的最短距离为_______ nm(列出计算式,NA为阿伏加德罗常数的值)。

(1)下列表示碳原子激发态轨道表示式的是
A.
 B.
B.
C.
 D.
D.
(2)N原子和O原子第二电离能N
(3)CH3NH
 中氮原子的杂化方式为
中氮原子的杂化方式为(4)某钙钛矿晶胞结构如图1,沿x、y、z轴方向的投影均为图2。与Pb2+、CH3NH
 距离最近I- 的数目分别是
距离最近I- 的数目分别是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】有四种前四周期的元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)基态A原子的核外电子排布式为_______ 。
(2)B元素在元素周期表中第_______ 族。
(3)C的基态原子的轨道表示式为_______ ,其原子核外有_______ 个未成对电子,能量最高的电子为_______ 轨道上的电子。
(4)B的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为_______ ;与D的氢化物的水溶液反应的化学方程式为_______ 。
| 元素 | 结构、性质等 |
| A | 单质是应用最广泛的金属 |
| B | 第三周期元素,其最高价氧化物对应的水化物呈两性 |
| C | 气态氢化物极易溶于水,可用作制冷剂 |
| D | 海水中除氢、氧元素外含量最多的元素,其单质或化合物是自来水处理过程中常用的消毒杀菌剂 |
(1)基态A原子的核外电子排布式为
(2)B元素在元素周期表中第
(3)C的基态原子的轨道表示式为
(4)B的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】中国早在周朝已能冶炼铸铁了。目前,铁及其化合物广泛地应用到各个领域。请回答下列问题:
(1)基态铁原子的电子排布式为___________ 。
(2)我国菱铁矿FeCO3储量较为丰富。其中CO 的空间结构为
的空间结构为___________ 。
(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是___________ 。
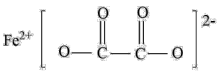
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20 ℃、103.6℃左右。因此可知Fe(CO)5属于___________ 晶体;CO与Fe之间从电子对给予来看形成___________ 键。
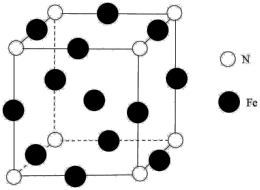
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是___________ 。若该晶体的密度是d g·cm-3,则两个最近的Fe间的距离为___________ cm(设NA为阿伏加德罗常数的值)。
(1)基态铁原子的电子排布式为
(2)我国菱铁矿FeCO3储量较为丰富。其中CO
 的空间结构为
的空间结构为(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是
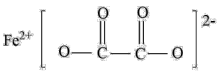
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20 ℃、103.6℃左右。因此可知Fe(CO)5属于
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是
您最近一年使用:0次
【推荐2】根据题意填空
(1)CH3COOH中C原子的杂化轨道类型为___________ 。
(2)化合物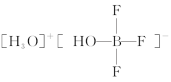 中阳离子的空间构型为
中阳离子的空间构型为___________ ,阴离子的中心原子轨道采用___________ 杂化。
(3) S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是___________ 。
(4)乙醇(CH3CH2OH)与二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是___________ 。
(5)AlCl3分子构型为平面三角形,则AlCl3分子为___________ (填“极性”或“非极性”,下同)分子,其分子中的共价键类型为___________ 键。
(6)BF3的熔点比BCl3___________ (填“高”“低”或“无法确定”)。
(7)下列含氧酸中酸性最强的是___________
A.HClO2 B.H2SeO3 C.H3BO3 D.HMnO4
(8)S、Cl组成的一种化合物的分子结构与H2O2相似,则此化合物的结构式为___________ ;
(9)已知CO与N2互为等电子体,则CO的电子式为___________ 。
(1)CH3COOH中C原子的杂化轨道类型为
(2)化合物
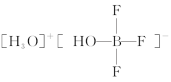 中阳离子的空间构型为
中阳离子的空间构型为(3) S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(4)乙醇(CH3CH2OH)与二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是
(5)AlCl3分子构型为平面三角形,则AlCl3分子为
(6)BF3的熔点比BCl3
(7)下列含氧酸中酸性最强的是
A.HClO2 B.H2SeO3 C.H3BO3 D.HMnO4
(8)S、Cl组成的一种化合物的分子结构与H2O2相似,则此化合物的结构式为
(9)已知CO与N2互为等电子体,则CO的电子式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】铜是人类最早使用的金属之一,最近科学家发现Cu元素有很强的杀菌作用,还可代替 布线在硅芯片上。用黄铜矿(主要成分为
布线在硅芯片上。用黄铜矿(主要成分为 )生产粗铜,其反应原理如下:
)生产粗铜,其反应原理如下:
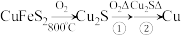
回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ 。 的熔点
的熔点___________  的熔点(填写“<”、“>”或“=”)。
的熔点(填写“<”、“>”或“=”)。
(2)反应①、②中生成的气体 ,
, 分子的
分子的 模型为
模型为___________ (填名称)。
(3) 能与
能与 形成配位数为4的配合物,向
形成配位数为4的配合物,向 溶液中加入氨水,最终形成配合物
溶液中加入氨水,最终形成配合物 。请判断:
。请判断: 中存在的化学键的类型有
中存在的化学键的类型有___________ (填序号)。
a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氧化物晶体的晶胞结构。该化合物的化学式为___________ ,每个 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有___________ 个,每个 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有___________ 个。
 布线在硅芯片上。用黄铜矿(主要成分为
布线在硅芯片上。用黄铜矿(主要成分为 )生产粗铜,其反应原理如下:
)生产粗铜,其反应原理如下: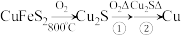
回答下列问题:
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为 的熔点
的熔点 的熔点(填写“<”、“>”或“=”)。
的熔点(填写“<”、“>”或“=”)。(2)反应①、②中生成的气体
 ,
, 分子的
分子的 模型为
模型为(3)
 能与
能与 形成配位数为4的配合物,向
形成配位数为4的配合物,向 溶液中加入氨水,最终形成配合物
溶液中加入氨水,最终形成配合物 。请判断:
。请判断: 中存在的化学键的类型有
中存在的化学键的类型有a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氧化物晶体的晶胞结构。该化合物的化学式为
 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有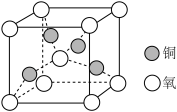
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】(1)氢键作用常表示为“A—H…B”,其中A、B为电负性很强的一类原子,用氢键的表示方法写出HF溶液中存在的所有氢键________________________ 。
(2)已知某配合物中有如下结构,则N原子的杂化方式为___________ ,在结构式上用“→”标出配位键。___________
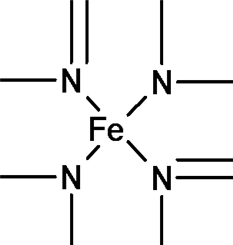
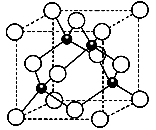
(3)Al和N组成的晶胞结构如下图一所示(“O”表示Al原子):
①则其化学式为_____ ,Al原子的配位数是___ ;
②一个N原子周围距离最近且等距的N原子有_____ 个。
(2)已知某配合物中有如下结构,则N原子的杂化方式为
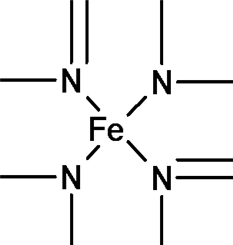
(3)Al和N组成的晶胞结构如下图一所示(“O”表示Al原子):
①则其化学式为
②一个N原子周围距离最近且等距的N原子有

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
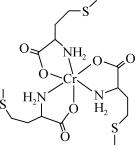
【推荐2】蛋氨酸铬(Ⅲ)配合物是一种治疗Ⅱ型糖尿病的药物,其结构简式如图所示。回答下列相关问题:
(1)基态Cr原子核外有___________ 种运动状态的电子,下列不同状态的Cr微粒中,电离最外层一个电子所需能量最大的是___________ (填标号)。
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(Ⅲ)配合物的中心铬离子的配位数为___________ ;N的___________ 杂化轨道与Cr的空轨道形成配位键。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+___________ (填“能”或“不能”)催化双氧水分解。
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:l,则呈亮绿色的配合物,其内界离子的化学式为___________ 。
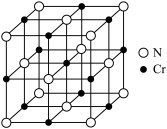
(5)氮化铬的晶胞结构如图所示。已知氮化铬的晶体密度为dg·cm-3,摩尔质量为M mol/L,NA为阿伏加德罗常数的值,则晶胞参数为___________ cm。

(1)基态Cr原子核外有
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(Ⅲ)配合物的中心铬离子的配位数为
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:l,则呈亮绿色的配合物,其内界离子的化学式为
(5)氮化铬的晶胞结构如图所示。已知氮化铬的晶体密度为dg·cm-3,摩尔质量为M mol/L,NA为阿伏加德罗常数的值,则晶胞参数为

您最近一年使用:0次
【推荐3】Fe、Cu、Cr都是第四周期过渡元素,回答下列问题。
(1)FeCl3是一种常用的净水剂,Cl元素的原子核外有___ 种不同运动状态的电子;有___ 种不同能级的电子,基态Fe3+的电子排布式为___ 。
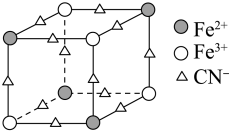
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是___ ;K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为___ 。
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图: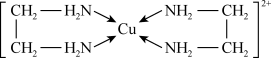 ,该配离子中含有的化学键类型有
,该配离子中含有的化学键类型有___ (填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有___ 个σ键,C原子的杂化方式为___ 。
(4)金属铜的晶胞为面心立方最密堆积,边长为361pm。则铜原子的直径约为___ pm。
(1)FeCl3是一种常用的净水剂,Cl元素的原子核外有
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是
 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
 ,该配离子中含有的化学键类型有
,该配离子中含有的化学键类型有a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有
(4)金属铜的晶胞为面心立方最密堆积,边长为361pm。则铜原子的直径约为
您最近一年使用:0次



