有四种前四周期的元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)基态A原子的核外电子排布式为_______ 。
(2)B元素在元素周期表中第_______ 族。
(3)C的基态原子的轨道表示式为_______ ,其原子核外有_______ 个未成对电子,能量最高的电子为_______ 轨道上的电子。
(4)B的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为_______ ;与D的氢化物的水溶液反应的化学方程式为_______ 。
| 元素 | 结构、性质等 |
| A | 单质是应用最广泛的金属 |
| B | 第三周期元素,其最高价氧化物对应的水化物呈两性 |
| C | 气态氢化物极易溶于水,可用作制冷剂 |
| D | 海水中除氢、氧元素外含量最多的元素,其单质或化合物是自来水处理过程中常用的消毒杀菌剂 |
(1)基态A原子的核外电子排布式为
(2)B元素在元素周期表中第
(3)C的基态原子的轨道表示式为
(4)B的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为
更新时间:2023-03-03 09:21:43
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学兴趣小组试利用镁铝合金废料(不含其它杂质 )制备硫酸铝晶体,其实验流程如下:

(1)在镁铝合金中加入NaOH溶液,发生反应的化学方程式为_________ ,固体B的化学式________ 。
(2)向滤液中通入足量二氧化碳的离子方程式_______________
(3)操作Ⅱ包含的实验步骤有:________ 、冷却结晶、过滤、洗涤、干燥。
(4)若初始时称取的镁铝合金废料的质量为7.65 g,得到固体A的质量为3.6 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%)。计算所得硫酸铝晶体的化学式为______ 。

(1)在镁铝合金中加入NaOH溶液,发生反应的化学方程式为
(2)向滤液中通入足量二氧化碳的离子方程式
(3)操作Ⅱ包含的实验步骤有:
(4)若初始时称取的镁铝合金废料的质量为7.65 g,得到固体A的质量为3.6 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%)。计算所得硫酸铝晶体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】短周期元素A、B、C、D在元素周期表中的位置如图所示,其中C所处的周期序数与主族序数相等,请回答下列问题:
(1)C的原子结构示意图为___________ ,A元素用于考古学的一种同位素的符号为___________ 。
(2)元素A的最高价氧化物对应水化物呈___________ (填“酸”“碱”或“中”)性,A与D的原子半径大小比较:A___________ D(填“>”或“<”);
(3)元素B与氢形成的原子个数比为 的化合物的电子式为
的化合物的电子式为___________ ,实验室常用该化合物的溶液加少量 制取B的单质,该反应中
制取B的单质,该反应中 做
做___________ (填“氧化剂”“还原剂”或“催化剂”);
(4)C的最高价氧化物是___________ (填“酸性”“碱性”或“两性”)氧化物,写出C的最高价氧化物对应水化物与D的氢化物在水溶液中反应的离子方程式___________ 。
| A | B | |||
| C | D |
(2)元素A的最高价氧化物对应水化物呈
(3)元素B与氢形成的原子个数比为
 的化合物的电子式为
的化合物的电子式为 制取B的单质,该反应中
制取B的单质,该反应中 做
做(4)C的最高价氧化物是
您最近一年使用:0次
【推荐3】粉煤灰的综合利用既有利于节约资源,又有利于保护环境。以粉煤灰(主要含 、
、 、
、 等)为原料制取
等)为原料制取 的一种工艺流程如下:
的一种工艺流程如下:

(1)酸浸时 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2)沉铝、铁后,检验溶液中是否还含有 的方法是
的方法是_______ 。
(3)蒸氨时反应的离子方程式为_______ 。
(4)过滤所得 和
和 经过分离后可以制取
经过分离后可以制取 溶液。
溶液。
①过滤后沉淀需要洗涤,检验沉淀是否洗涤干净的方法是_______ 。
②设计由 和
和 制取
制取 溶液的实验方案:
溶液的实验方案:_______ 。(实验中可以使用的试剂是盐酸和NaOH溶液)
 、
、 、
、 等)为原料制取
等)为原料制取 的一种工艺流程如下:
的一种工艺流程如下:
(1)酸浸时
 发生反应的离子方程式为
发生反应的离子方程式为(2)沉铝、铁后,检验溶液中是否还含有
 的方法是
的方法是(3)蒸氨时反应的离子方程式为
(4)过滤所得
 和
和 经过分离后可以制取
经过分离后可以制取 溶液。
溶液。①过滤后沉淀需要洗涤,检验沉淀是否洗涤干净的方法是
②设计由
 和
和 制取
制取 溶液的实验方案:
溶液的实验方案:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族元素原子中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层电子数多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)D在周期表中的位置为___ ;B的原子结构示意图为___ 。
(2)E元素形成的最高价氧化物对应水化物的化学式为___ 。
(3)元素C、D、E的原子半径大小关系是___ (用元素符号表示)。
(4)C、D可形成化合物D2C2,D2C2含有的化学键是___ 。
(1)D在周期表中的位置为
(2)E元素形成的最高价氧化物对应水化物的化学式为
(3)元素C、D、E的原子半径大小关系是
(4)C、D可形成化合物D2C2,D2C2含有的化学键是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:C___________ 、F___________ 。
②A、B、C三种元素的电负性由大到小的顺序是:___________ 。
③B、C、D、E四种元素的第一电离能由大到小的顺序是:___________ 。
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ (填元素符号)。
(3)F元素位于周期表的_______ 区,此区元素的价电子层结构特点是_______ 。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用元素符号完成下列空白:
①元素:C
②A、B、C三种元素的电负性由大到小的顺序是:
③B、C、D、E四种元素的第一电离能由大到小的顺序是:
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
| 元素 | 电离能/( | ||||
 |  |  |  |  | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素, D单质燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称: A_______ B_______ D _______
(2)E在周期表中的位置:_______
(3)F离子结构示意图:_______
(4)A、B组成的最简单化合物的名称是_______
(5)用电子式表示BC2的形成过程:_______
(6)C单质与D单质在常温下反应的产物的电子式_______
(7)C单质与D单质在点燃条件下反应的产物W中所含化学键类型为_______ ,将W溶于水的化学方程式_______ ,W的用途有_______ (填一种)
(8)能说明E的非金属性比F的非金属性_______ (填“强”或“弱”)的事实是: _______ (举一例)。
(1)元素名称: A
(2)E在周期表中的位置:
(3)F离子结构示意图:
(4)A、B组成的最简单化合物的名称是
(5)用电子式表示BC2的形成过程:
(6)C单质与D单质在常温下反应的产物的电子式
(7)C单质与D单质在点燃条件下反应的产物W中所含化学键类型为
(8)能说明E的非金属性比F的非金属性
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1)基态S原子核外电子排布式为_______ ,S原子电子占据最高能级的电子云轮廓图为_______ 形,基态Cu原子价电子的电子排布图(轨道表达式)为_______ ,与Cu同周期的过渡元素中,未成对电子数最多的基态原子的核外电子排布式为_______ 。
(2)抗坏血酸的分子结构如图1所示,推测抗坏血酸在水中的溶解性:_______ (填“难溶于水”或“易溶于水”)。

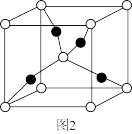
(3)O(白点)和Cu(黑点)元素形成的化合物的晶胞结构如图2所示,则该化合物的化学式为_______ 。
(4)苯胺(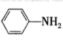 )的晶体类型是
)的晶体类型是_______ 。苯胺与甲苯(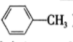 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(1)基态S原子核外电子排布式为
(2)抗坏血酸的分子结构如图1所示,推测抗坏血酸在水中的溶解性:

(3)O(白点)和Cu(黑点)元素形成的化合物的晶胞结构如图2所示,则该化合物的化学式为

(4)苯胺(
 )的晶体类型是
)的晶体类型是 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
您最近一年使用:0次
【推荐2】N,P,As等元素的化合物在生产和研究中有许多重要用途。请回答下列问题:
(1)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为_______ ,N—N键的键角为____ 。
(2)基态砷原子的价电子排布图为_______ ,砷与同周期相邻元素的第一电离能由大到小的顺序为______ 。
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是__________  填PH4”或“
填PH4”或“ ”
” 。
。
(4)SCl3+和 是等电子体,
是等电子体,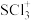 的空间构型是
的空间构型是_________ 。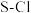 键键长
键键长____ 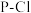 键键长
键键长 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,原因是
,原因是____________ 。
(1)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为
(2)基态砷原子的价电子排布图为
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。
 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是 填PH4”或“
填PH4”或“ ”
” 。
。(4)SCl3+和
 是等电子体,
是等电子体,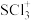 的空间构型是
的空间构型是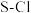 键键长
键键长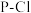 键键长
键键长 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,原因是
,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】亚铁氰化钾( )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。
(1)O元素位于___________ 区,基态O原子核外电子的空间运动状态有___________ 种。
(2)Fe在元素周期表中的位置___________ ,基态Fe原子的价电子轨道表示式为___________ 。
(3)黄血盐( )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是___________ , 该原子能量最高的电子所在能级符号为___________ 。
(4)亚铁氰化钾( )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为___________ 。
(5)普鲁士蓝( )中C的杂化方式为
)中C的杂化方式为___________ 。
 )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。(1)O元素位于
(2)Fe在元素周期表中的位置
(3)黄血盐(
 )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是(4)亚铁氰化钾(
 )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为(5)普鲁士蓝(
 )中C的杂化方式为
)中C的杂化方式为
您最近一年使用:0次

 )
)

