已知下列两个热化学方程式:
H2(g)+ O2(g)=H2O(l) ΔH=-285.8kJ/mol
O2(g)=H2O(l) ΔH=-285.8kJ/mol
C3H8(g)+5O2(g)=4H2O(l)+3CO2(g) ΔH=-2220.0kJ/mol
已知:H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出丙烷燃烧生成CO2和气态水的热化学方程式___ 。
H2(g)+
 O2(g)=H2O(l) ΔH=-285.8kJ/mol
O2(g)=H2O(l) ΔH=-285.8kJ/molC3H8(g)+5O2(g)=4H2O(l)+3CO2(g) ΔH=-2220.0kJ/mol
已知:H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出丙烷燃烧生成CO2和气态水的热化学方程式
更新时间:2020-05-16 15:45:41
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是________________________
(2)如图是某温度下,N2与H2反应过程中能量变化的曲线图。

a、b两条曲线产生区别的原因很可能是________________ 。
(3)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol H2O(l)时放出571.6 kJ热量,则H2的热值为________
(4)已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g) ΔH=489.0 kJ·mol-1
CO(g)+ O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
由Fe(s)和O2(g)反应生成Fe2O3(s)的热化学方程式为_______________________________ 。
(2)如图是某温度下,N2与H2反应过程中能量变化的曲线图。

a、b两条曲线产生区别的原因很可能是
(3)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol H2O(l)时放出571.6 kJ热量,则H2的热值为
(4)已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g) ΔH=489.0 kJ·mol-1
CO(g)+
 O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1C(石墨)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
由Fe(s)和O2(g)反应生成Fe2O3(s)的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知16.0 g CH4完全燃烧生成CO2和液态水时,放出890kJ热量。现有CH4和CO混合气体共0.75 mol,完全燃烧后生成CO2和18 g液态水,并放出516 kJ热量。求:
(1)混合气体中CH4的物质的量为___________ , CO的物质的量为__________ ;
(2)混合气体中由CO完全燃烧所放出的热量为__________ kJ?
(1)混合气体中CH4的物质的量为
(2)混合气体中由CO完全燃烧所放出的热量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】填空。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式_______ 。
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=_______ kJ∙mol-1。
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
则N2(g)+O2(g)=2NO(g) ΔH=_______ kJ·mol-1。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
| 物质 | N2 | O2 | NO |
| 能量(kJ·mol-1) | 946 | 498 | 632 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是______ (填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径① 通过化学键的键能计算。已知:
计算可得:2H2(g)+ O2(g) =2H2O(g) ∆H=____________ kJ·mol-1
②通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+ O2(g) =Na2O(s)△H=-414kJ·mol-1
O2(g) =Na2O(s)△H=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g) =Na2O2(s)△H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式__________ 。
③ 利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________ (填序号)。
A.50 mL 0.50 mol·L-1NaOH溶液B.50 mL 0.55 mol·L-1NaOH溶液 C.1.0 g NaOH固体
(1)下列反应中,属于吸热反应的是
A.Na2O与水反应 B.甲烷的燃烧反应C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径① 通过化学键的键能计算。已知:
| 化学键种类 | H—H | O=O | O—H |
| 键能(kJ/mol) | 436 | 498 | 463.4 |
计算可得:2H2(g)+ O2(g) =2H2O(g) ∆H=
②通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+
 O2(g) =Na2O(s)△H=-414kJ·mol-1
O2(g) =Na2O(s)△H=-414kJ·mol-1Ⅱ.2Na(s)+O2(g) =Na2O2(s)△H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式
③ 利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入
A.50 mL 0.50 mol·L-1NaOH溶液B.50 mL 0.55 mol·L-1NaOH溶液 C.1.0 g NaOH固体
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在恒压下化学反应所吸收或放出的热量,称为化学反应的焓变。回答下列问题:
(1)25℃、101 kPa时,1 g氨气完全燃烧放出18.6 kJ的热量,则4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=______ kJ·mol-1。
(2)常压下,某铝热反应的温度与能量变化如图所示:
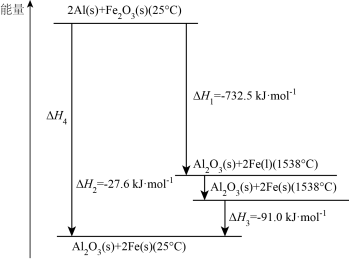
①常压、1538℃时,Fe(s)→Fe(l) △H=______ kJ·mol-1。
②常压、25℃时,该铝热反应的热化学方程式为__________ 。
(3)在稀溶液中酸与碱发生中和反应生成1 mol水时所释放的热量称为中和热。部分酸与碱反应的中和热如下表:
①I、IV的热化学方程式(用离子方程式形式表示)依次为_____ 、_____ 。
②I、II的△H相同,III、IV、V的△H比I、II大,其原因是__________ 。
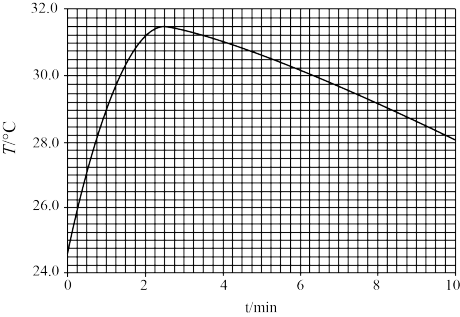
③体积和浓度均为25.0 mL 1.00 mol·L-1的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为1.00 g·mL-1,混合溶液的比热容为4.18 J·g-1·℃-1。由实验数据可计算出该反应的中和热△H为______ kJ·mol-1(结果保留1位小数)。
(1)25℃、101 kPa时,1 g氨气完全燃烧放出18.6 kJ的热量,则4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=
(2)常压下,某铝热反应的温度与能量变化如图所示:

①常压、1538℃时,Fe(s)→Fe(l) △H=
②常压、25℃时,该铝热反应的热化学方程式为
(3)在稀溶液中酸与碱发生中和反应生成1 mol水时所释放的热量称为中和热。部分酸与碱反应的中和热如下表:
| 组别 | 酸与碱 | 中和热△H/(kJ/mol) |
| Ⅰ | HCl+NaOH | -57.1 |
| Ⅱ | HNO3+KOH | -57.1 |
| Ⅲ | CH3COOH+NaOH | -56.1 |
| Ⅳ | HCl+NH3·H2O | -53.4 |
| Ⅴ | CH3COOH+NH3·H2O | -50.4 |
②I、II的△H相同,III、IV、V的△H比I、II大,其原因是
③体积和浓度均为25.0 mL 1.00 mol·L-1的硝酸和NaOH溶液(起始温度相同)混合时,测得混合溶液的温度与时间的关系如图所示,已知硝酸和NaOH溶液的密度均为1.00 g·mL-1,混合溶液的比热容为4.18 J·g-1·℃-1。由实验数据可计算出该反应的中和热△H为

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜)=S(s,斜方) ΔH= -0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是____ [填“S(单斜)”或“S(斜方)”]。
(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH= -183 kJ·mol-1,则HCl(g)= H2(g)+
H2(g)+ Cl2(g) ΔH=
Cl2(g) ΔH=______ ,若破坏1 molH-H键需消耗的能量436kJ,破坏1 molH-Cl键需消耗的能量431kJ,则破坏1 molCl-Cl键需消耗的能量是_________ 。
(3)标准状况下,6.72 L C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2燃烧热的热化学方程式:____ 。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变为______ 。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成1 mol N2理论上放出的热量为____ 。

(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH= -183 kJ·mol-1,则HCl(g)=
 H2(g)+
H2(g)+ Cl2(g) ΔH=
Cl2(g) ΔH=(3)标准状况下,6.72 L C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成1 mol N2理论上放出的热量为

您最近一年使用:0次



