A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体。
(1)写出以下元素的名称:B________________ ;C______________ 。
(2)写出D元素在周期表中的位置___________________________
(3)用电子式表示C2D的形成过程:_______________________________
(4)写出由B、C两元素所形成的原子个数比为1:1的化合物的的电子式_______ ;属于_______ (填“离子”或“共价”)化合物,存在的化学键的种类有______________________ ;写出它与水反应的离子方程式_______________________________
(1)写出以下元素的名称:B
(2)写出D元素在周期表中的位置
(3)用电子式表示C2D的形成过程:
(4)写出由B、C两元素所形成的原子个数比为1:1的化合物的的电子式
19-20高一下·江西宜春·期中 查看更多[2]
(已下线)易错专题29 化学键-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)江西省宜春市高安中学2019-2020学年高一下学期期中考试化学(B)试题
更新时间:2020-05-31 06:09:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知亚硫酸钠隔绝空气加热到 600℃可以分解,实验流程如下图(所得气体是纯净物):

(1)硫元素在元素周期表中的位置_________________ 亚硫酸钠中含有的化学键类型 _________________ .
(2)写出亚硫酸钠受热分解的化学方程式_________________ .
(3)下列说法正确的是_________________ .
A.加热分解后的固体中氧元素质量为 1.92 克
B.生成白色沉淀的物质的量 0.04mol
C.分解后固体溶于水后,溶液中离子浓度大小顺序为c(Na+)> c(SO42-)>c(S2-)>c(OH-)>c(HS-)>c(H+)
D.将适量亚硫酸钠与分解后的固体混合,再加稀盐酸可能会出现沉淀

(1)硫元素在元素周期表中的位置
(2)写出亚硫酸钠受热分解的化学方程式
(3)下列说法正确的是
A.加热分解后的固体中氧元素质量为 1.92 克
B.生成白色沉淀的物质的量 0.04mol
C.分解后固体溶于水后,溶液中离子浓度大小顺序为c(Na+)> c(SO42-)>c(S2-)>c(OH-)>c(HS-)>c(H+)
D.将适量亚硫酸钠与分解后的固体混合,再加稀盐酸可能会出现沉淀
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】短周期元素X、Y、Z在周期中位置关系如图所示。

(1)X元素的单质分子式是____ ,若X核内中子数与质子数相等,X单质的摩尔质量是___ 。
(2)Z元素的单质是一种___ 色的____ 体。该单质与铁粉反应的化学方程式为____ 。
(3)Y元素的单质与H2O反应的化学方程式为____ ,若1 mol Y单质反应,转移____ mol电子。

(1)X元素的单质分子式是
(2)Z元素的单质是一种
(3)Y元素的单质与H2O反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题。
(1)下列叙述中,正确的是_______
(2)请利用原子结构知识对下列结论进行说明和论证。
结论1:同周期的主族元素,从左到右,元素原子失电子能力越来越弱。______ 。
结论2:碱金属元素,从上到下,元素原子失电子能力越来越强。______ 。
(1)下列叙述中,正确的是_______
| A.同周期元素中,ⅦA族元素的原子半径最大 |
| B.ⅥA族元素的原子,其原子半径越大,越容易得到电子 |
| C.常温时,0族元素的单质都是气体 |
| D.在元素周期表中,从ⅢB族到ⅡB族10个纵列的元素都是金属元素 |
结论1:同周期的主族元素,从左到右,元素原子失电子能力越来越弱。
结论2:碱金属元素,从上到下,元素原子失电子能力越来越强。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8。A元素原子的第二层电子数与第一、第三层电子数之和相等,D元素原子的第一、第二层电子数之和等于电子总数的一半。试回答下列问题。
(1)四种元素的符号依次是A___ ,B___ ,C__ ,D__ ;它们的原子半径由大到小的顺序是___ 。
(2)试写出四种元素的离子结构示意图:A___ ,B___ ,C___ ,D___ 。它们的离子半径由大到小的顺序是___ (用离子符号表示)。
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:__ 。
(4)分别写出A、B两元素的气态氢化物的化学式:__ 。
(1)四种元素的符号依次是A
(2)试写出四种元素的离子结构示意图:A
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:
(4)分别写出A、B两元素的气态氢化物的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】四种常见元素的性质或结构信息如下表,回答有关问题.
(1)B原子的电子排布式____________ .C原子核外电子运动状态共有_______ 种.
(2)上述某种元素形成的最简单气态氢化物为非极性分子,该分子的电子式为_________ ,A元素最高价氧化物对应的水化物和气态氢化物发生化合反应的生成物中含有的化学键为_____________ .
(3)D与同主族相邻元素的最高价氧化物的熔点比较:__________ (填“前者高”或“前者低”),其原因是____________________ .
(4)B和C两元素非金属性较强的是(写元素符号)_________________ .写出证明这一结论的一个化学方程式____________________ .
| 元素 | A | B | C | D |
| 性质 结构 信息 | 最高价氧化物对应的水化物和气态氢化物可以发生化合反应 | 原子的M层有1对成对的p电子 | 原子核外有5种能量不同的电子,最外层电子为7 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)B原子的电子排布式
(2)上述某种元素形成的最简单气态氢化物为非极性分子,该分子的电子式为
(3)D与同主族相邻元素的最高价氧化物的熔点比较:
(4)B和C两元素非金属性较强的是(写元素符号)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 是6种短周期主族元素,
是6种短周期主族元素,原子半径依次增大 ,其中U与X同主族并能形成共价化合物 与X同周期,Y的最外层电子数等于其电子层数,V与Y最外层电子数相同,Z的单核离子与
与X同周期,Y的最外层电子数等于其电子层数,V与Y最外层电子数相同,Z的单核离子与 具有相同的电子数与质子数。请按要求回答下列问题:
具有相同的电子数与质子数。请按要求回答下列问题:
(1)请写出Y在元素周期表中的位置:___________ 。
(2)元素 的最简单氢化物中,最稳定的是
的最简单氢化物中,最稳定的是___________ (用电子式表示)。
(3)Z的某种氧化物可用于潜水艇中的供氧剂,请写出其与 反应的化学方程式:
反应的化学方程式:___________ 。
(4)元素W、X、Y、Z的简单离子的半径由大到小的顺序是___________ (用离子符号表示)。
(5)元素的非金属性:W___________ X(填“>”或“<”);下列事实不能证明该结论的是___________ 。
A.W的单质与X的氢化物的水溶液反应,生成单质X
B.简单氢化物的酸性W强于X
C.W、X的氢化物受热分解,前者的分解温度高
D.氧化物对应水化物的酸性W比X强
(6)通常情况下,最外层电子数相同的元素,化学性质相似。则单质V与足量氢氧化钠溶液反应的离子方程式为___________ 。
 是6种短周期主族元素,
是6种短周期主族元素, 与X同周期,Y的最外层电子数等于其电子层数,V与Y最外层电子数相同,Z的单核离子与
与X同周期,Y的最外层电子数等于其电子层数,V与Y最外层电子数相同,Z的单核离子与 具有相同的电子数与质子数。请按要求回答下列问题:
具有相同的电子数与质子数。请按要求回答下列问题:(1)请写出Y在元素周期表中的位置:
(2)元素
 的最简单氢化物中,最稳定的是
的最简单氢化物中,最稳定的是(3)Z的某种氧化物可用于潜水艇中的供氧剂,请写出其与
 反应的化学方程式:
反应的化学方程式:(4)元素W、X、Y、Z的简单离子的半径由大到小的顺序是
(5)元素的非金属性:W
A.W的单质与X的氢化物的水溶液反应,生成单质X
B.简单氢化物的酸性W强于X
C.W、X的氢化物受热分解,前者的分解温度高
D.氧化物对应水化物的酸性W比X强
(6)通常情况下,最外层电子数相同的元素,化学性质相似。则单质V与足量氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知某元素A能与ⅦA族某一元素B生成A的最高价化合物X,在化合物X中B的含量为92.2%,而在与此相应的A的氧化物Y中,氧的含量为72.7%。A与B生成的化合物X为一无色透明液体,沸点77℃,对氢气的相对密度为77。
回答下列问题(不必给出计算过程):
(1)A元素名称___ ,并指出属于第几周期第几族___ ;
(2)X的分子式___ ,分子空间构型和键角___ 、___ ;
(3)Y的分子式___ ,分子空间构型和键角___ 、___ ;
(4)列举化合物X的两种用途___ 。
回答下列问题(不必给出计算过程):
(1)A元素名称
(2)X的分子式
(3)Y的分子式
(4)列举化合物X的两种用途
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知W、X、Y、Z是原子序数依次增大的短周期元素,W、X 、Z都是非金属元素,常温下单质都为气态。X、Z在同一主族, Y单质为银白色金属固体,且W和Y的最外层电子数相等,Y和Z同周期且化合物YZ是海水主要的成份之一。
(1)W的氧化物可电解生成W单质和O2,该反应中转移的电子总数为 ;
(2)X2可与水反应生成WX和O2,该反应的化学方程式为 ;
(3)Y可与水反应生成YOH和W2,该反应的化学方程式为 ;
(4)Z2是黄绿色有刺激性气味的气体,可与水反应生成HZ和HZO,
该反应的化学方程式为 ;
(5)比较HX、HZ气态氢化物的稳定性: > (用化学式表示)
(6)YOH是一种强碱,0.25 mol的该物质与一定量HZ稀溶液(呈酸性)发生中和反
应,并放出 Q kJ的热量。写出该反应的热化学方程式:
(1)W的氧化物可电解生成W单质和O2,该反应中转移的电子总数为 ;
(2)X2可与水反应生成WX和O2,该反应的化学方程式为 ;
(3)Y可与水反应生成YOH和W2,该反应的化学方程式为 ;
(4)Z2是黄绿色有刺激性气味的气体,可与水反应生成HZ和HZO,
该反应的化学方程式为 ;
(5)比较HX、HZ气态氢化物的稳定性: > (用化学式表示)
(6)YOH是一种强碱,0.25 mol的该物质与一定量HZ稀溶液(呈酸性)发生中和反
应,并放出 Q kJ的热量。写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】X、Y、Z三种常见的短周期元素,可形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子具有相同的电子层结构,X离子比Y离子多一个电子层,试回答:
(1)X、Y、Z的单质的晶体分别属于_______ 晶体,________ 晶体,_____ 晶体
(2)Z2Y2的电子式为___________ ,Z2Y2溶于水的化学方程式为__________ 。
(3)XY3在标准状态下是针状晶体,它属于___________ 晶体,XY3的水溶液与Z2Y2反应可生成一种具有漂白性的氧化剂H2Y2,其化学方程式为_______ 。
(1)X、Y、Z的单质的晶体分别属于
(2)Z2Y2的电子式为
(3)XY3在标准状态下是针状晶体,它属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Mn(NO3)2中的化学键是___________ 、___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是_____ (填序号,下同);仅发生离子键破坏的是_____ 。
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是_____ ;既存在离子键又存在极性键的是_____ 。
(3)写出下列物质的电子式。
①Na2O2_____ 。
②HClO_____ 。
③NH4Cl_____ 。
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是
(3)写出下列物质的电子式。
①Na2O2
②HClO
③NH4Cl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C、X是中学化学中常见的4种物质,它们均由短周期元素组成,转化关系如图所示。请针对以下三种情况回答下列问题。
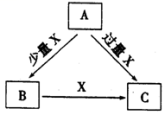
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得白色胶状沉淀B。
①A中含有的金属元素为__________ (填元素名称)
② 该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,反应的化学反应方程式是_______________
(2)若A为固态非金属单质,A与X同周期,常温常压下C 为 白色固体,B分子中各原子最外层均为8电子结构。
① B的电子式为_____________ 。
② C与水剧烈反应,生成两种常见酸,反应的化学方程式为___________________ 。
(3) 若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
① A中所含有的化学键是_____________ 。
② 自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________ g。

(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得白色胶状沉淀B。
①A中含有的金属元素为
② 该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,反应的化学反应方程式是
(2)若A为固态非金属单质,A与X同周期,常温常压下C 为 白色固体,B分子中各原子最外层均为8电子结构。
① B的电子式为
② C与水剧烈反应,生成两种常见酸,反应的化学方程式为
(3) 若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
① A中所含有的化学键是
② 自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为
您最近一年使用:0次



