选择装置,完成实验。
(1)分离水和植物油,选用___ (填序号,下同)。
(2)配制100mL0.1mol·L-1NaOH溶液,选用___ 。
(3)鉴别Na2CO3和NaHCO3固体,选用__ 。
(4)用乙酸、乙醇和浓硫酸制备乙酸乙酯,选用__ 。
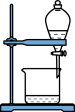 |  | 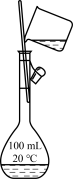 |  |
| ① | ② | ③ | ④ |
(2)配制100mL0.1mol·L-1NaOH溶液,选用
(3)鉴别Na2CO3和NaHCO3固体,选用
(4)用乙酸、乙醇和浓硫酸制备乙酸乙酯,选用
更新时间:2020-06-02 10:24:18
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)0.3molNH3分子中所含氢原子数与__________ 个H2O分子中所含氢原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是________ 。
(3)3.01×1022个OH-的物质的量为_______ ,质量为__________ ,含有质子的物质的量为_____________ ,含有电子的物质的量为_____________ 。
(4)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏伽德罗常数)______________ 。
(5)标准状况下,336L的NH3溶于1L水中,所得溶液的溶质质量分数为____________ ,若该溶液的密度为a g/cm3,则物质的量浓度为______ (结果保留一位小数)。将上述氨水全部转化为NH4Cl,所需2mol/L的盐酸的体积为______ 。(已知NH3+HCl=NH4Cl)
(2)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是
(3)3.01×1022个OH-的物质的量为
(4)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏伽德罗常数)
(5)标准状况下,336L的NH3溶于1L水中,所得溶液的溶质质量分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】物质的量浓度和溶质质量分数的比较
| 物质的量浓度c | 溶质质量分数w | |
| 概念 | 以单位体积溶液中所含溶质的 | 以溶质质量与溶液质量的 |
| 溶质的单位 | ||
| 溶液的单位 | ||
| 表达式 | ||
| 两者关系 |  (M:摩尔质量,单位: (M:摩尔质量,单位: ; ; :密度,单位: :密度,单位: ) ) | |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】现有以下物质:①Na;②O2;③H2SO4;④KOH;⑤蔗糖;⑥H2O;⑦NaCl;⑧空气;⑨NaHSO4;⑩Na2CO3;按要求填空:
(1)属于氧化物的是:_______ ;属于酸的是:_______ ;属于电解质的是_______ ;写出一种与②互为同素异形体的物质的化学式_______ 。
(2)写出③在水溶液中电离的电离方程式_______ 。
(3)NaCl分散在酒精中可形成胶体,则区别该分散系和氯化钠溶液最简单的方法是该分散系可出现_______ 。
(4)检验NaCl中是否含有 ,需选择的化学试剂及实验方法为_______。
,需选择的化学试剂及实验方法为_______。
(5)写出①与水反应的化学方程式为_______ 。
(6)防烟面具中氧气的来源是过氧化钠,写出Na2O2与二氧化碳反应的化学方程式:_______ 。
(7)Na2CO3溶液中Na+的浓度为 0.3 mol•L-1,则该溶液中c(Na2CO3)_______ mol•L-1。
(1)属于氧化物的是:
(2)写出③在水溶液中电离的电离方程式
(3)NaCl分散在酒精中可形成胶体,则区别该分散系和氯化钠溶液最简单的方法是该分散系可出现
(4)检验NaCl中是否含有
 ,需选择的化学试剂及实验方法为_______。
,需选择的化学试剂及实验方法为_______。A.加入 浓溶液加热,观察现象 浓溶液加热,观察现象 | B.加稀HNO3和AgNO3溶液,观察现象 |
C.加入 溶液,观察现象 溶液,观察现象 | D.滴加酚酞试液,观察现象 |
(6)防烟面具中氧气的来源是过氧化钠,写出Na2O2与二氧化碳反应的化学方程式:
(7)Na2CO3溶液中Na+的浓度为 0.3 mol•L-1,则该溶液中c(Na2CO3)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某汽车安全气囊的气体发生剂主要含有叠氮化钠、三氧化二铁、高氯酸钾、碳酸氢钠等物质。
(1)叠氮化钠是气体发生剂,受热分解产生氮气和金属钠。反应的化学方程式为_____ 。
(2)高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。氧化钠中化学键的类型为_____ 。
(3)碳酸氢钠的作用是_____ 。
(1)叠氮化钠是气体发生剂,受热分解产生氮气和金属钠。反应的化学方程式为
(2)高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。氧化钠中化学键的类型为
(3)碳酸氢钠的作用是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】用化学用语表达。
(1)小苏打受热易分解,化学方程式为__ 。
(2)金属钠着火不能用水扑灭,用离子方程式解释其原因__ 。
(3)工业上用氯气和熟石灰制备漂白粉,化学方程式为__ 。
(1)小苏打受热易分解,化学方程式为
(2)金属钠着火不能用水扑灭,用离子方程式解释其原因
(3)工业上用氯气和熟石灰制备漂白粉,化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知有如下反应:2CH3CHO+O2→2CH3COOH。请以乙烯,空气,水为主要原料,写出合成乙酸乙酯的化学方程式。
⑴___________________________________________________________________________________________ 。
⑵____________________________________________________________________________________________ 。
⑶_____________________________________________________________________________________ 。
⑷____________________________________________________________________________________________ 。
⑴
⑵
⑶
⑷
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】丙烯酸乙酯(CH2 =CHCOOC2H5)存在于菠萝等水果中,是一种香料,可用于配制朗姆酒,也可用作有机合成的中间体。可通过下列途径合成丙烯酸乙酯:
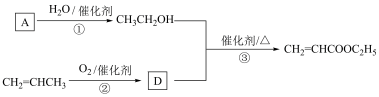
回答下列问题:
(1)丙烯酸乙酯中含有的官能团名称是_______ 。
(2)有机物A 被誉为“石化工业之母”,其产量可用来衡量一个国家的石油化学工业的发展水平,A的电子式为_______ 。
(3)反应①的反应类型为_______ 。
(4)反应③的反应方程式为_______ 。
(5)久置的丙烯酸乙酯自身会发生聚合反应,所得聚合物具有很好的弹性,该聚合物的结构简式为_______ 。
(6)该方法合成的丙烯酸乙酯中主要含有的杂质是_______ (填名称),除去杂质可选用的试剂名称是_______ 。

回答下列问题:
(1)丙烯酸乙酯中含有的官能团名称是
(2)有机物A 被誉为“石化工业之母”,其产量可用来衡量一个国家的石油化学工业的发展水平,A的电子式为
(3)反应①的反应类型为
(4)反应③的反应方程式为
(5)久置的丙烯酸乙酯自身会发生聚合反应,所得聚合物具有很好的弹性,该聚合物的结构简式为
(6)该方法合成的丙烯酸乙酯中主要含有的杂质是
您最近一年使用:0次
【推荐3】某学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10 min;

③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置;
④分离出乙酸乙酸层、洗涤、干燥。
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式:_______ 。
(2)上述实验中饱和碳酸钠溶液的作用是_______(填字母)。
(3)浓硫酸的作用是_______ ;
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是_______ ;
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是_______ ;
①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10 min;

③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置;
④分离出乙酸乙酸层、洗涤、干燥。
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式:
(2)上述实验中饱和碳酸钠溶液的作用是_______(填字母)。
| A.中和乙醇 |
| B.和乙酸反应并溶解乙醇 |
| C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出 |
| D.加速酯的生成,提高其产率 |
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是
您最近一年使用:0次



