如图是元素周期表的一部分,按要求回答问题:
(1)请写出下列元素的元素符号:①________ ③_________ ⑨___________ 。
(2)元素①④按2:1组成的化合物中化学键为_________ 。(填“共价键”或“离子键”)
(3)②的单质与⑧的最高价氧化物水化物热的浓溶液反应的化学方程式为____________ 。
(4)⑤⑥⑦的最高价氧化物水化物的碱性从大到小的顺序____________ 。(填化学式)
(5)④⑤⑥⑧形成的简单离子,其离子半径由小到大的顺序为____________ (填离子符号)。
(6)④和⑧的氢化物稳定性从大到小的顺序为______________________ 。(填化学式)
(7)元素④的氢化物与⑤发生反应的方程式_____________ ,所得溶液PH____ 7(填“>”或“<”或“=”)。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)请写出下列元素的元素符号:①
(2)元素①④按2:1组成的化合物中化学键为
(3)②的单质与⑧的最高价氧化物水化物热的浓溶液反应的化学方程式为
(4)⑤⑥⑦的最高价氧化物水化物的碱性从大到小的顺序
(5)④⑤⑥⑧形成的简单离子,其离子半径由小到大的顺序为
(6)④和⑧的氢化物稳定性从大到小的顺序为
(7)元素④的氢化物与⑤发生反应的方程式
更新时间:2020-06-02 12:26:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了①~⑩10种元素在周期表中的位置。
(1)上述元素中,金属性最强的是(填元素符号,下同)________ ,③④⑤三种元素的原子半径由大到小的顺序是____________ 。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________ (填化学式)
(3)元素⑥的氢化物的电子式为____________ ,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为____________ 。
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是____________ (填化学式)。
| 族 周期 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑩ | |||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | |||
| 4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是
(3)元素⑥的氢化物的电子式为
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、D、E、F五种元素的原子序数依次增大,除F为过渡元素外,其余四种均是短周期元素。已知:①F的单质为生活中最常见的金属之一,原子最外层有2个电子;②E原子的价电子排布为msnmpn,B原子的核外L层电子数为奇数;③A、D原子p轨道的电子数分别为2和4.请回答下列问题:
(1)F的稳定价态离子的电子排布式是__________________________ ;A、B、D、E四种元素的第一电离能由大到小的顺序为________________ (用元素符号表示)。
(2)对于B的简单氢化物,其中心原子的轨道杂化类型是________________ 。分子的立体构型为________________ ,该氢化物易溶于D的简单氢化物的主要原因是________________ 。
(3)D原子分别与A、B原子形成的单键中,键的极性较强是________________ (用具体的化学键表示)。
(4)如图所示的晶胞是由AD两元素组成的,下列有关该晶体的说法中正确的是_______ 。
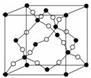
a.该晶体的化学式为AD
b.该晶体中A、D原子间形成的是双键
c.该晶体熔点可能比SiO2晶体高
d.该晶体可溶于水
(1)F的稳定价态离子的电子排布式是
(2)对于B的简单氢化物,其中心原子的轨道杂化类型是
(3)D原子分别与A、B原子形成的单键中,键的极性较强是
(4)如图所示的晶胞是由AD两元素组成的,下列有关该晶体的说法中正确的是

a.该晶体的化学式为AD
b.该晶体中A、D原子间形成的是双键
c.该晶体熔点可能比SiO2晶体高
d.该晶体可溶于水
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】冬季当大雪飘落后,我们都会看到环卫工人往雪地里撒一种叫融雪剂的物质,其作用是为城市道路、高速公路、机场等设施融雪化冰,有的融雪剂还可用作建筑工程冬季施工冰雪融化的速融剂和防冻外加剂等。

一种融雪剂主要成分的化学式为XY2,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的电子式是____ ,XY2中离子半径由大到小的顺序是____ (用离子符号表示)。
(2)主族元素C原子的最外层电子数是其电子层数的2倍,C与Y相邻,则C与Y的最高价氧化物对应的水化物酸性较弱的是_____ (填化学式);D是地壳中含量最多的一种元素,D的单质的同素异形体有____ 和_____ 。
(3)元素W与Y同周期,0.1 mol的W单质能从酸中置换出2.24 L H2(标准状况),则W单质的元素名称为_____ ;W单质与热水反应的化学方程式为_____ 。
(4)Y与G同族,且G的单质常温下呈液态,Y和G两种元素相比较,非金属性较强的是___ (填元素名称),可以验证该结论的是____ (填序号)。
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的含氧酸的酸性

一种融雪剂主要成分的化学式为XY2,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的电子式是
(2)主族元素C原子的最外层电子数是其电子层数的2倍,C与Y相邻,则C与Y的最高价氧化物对应的水化物酸性较弱的是
(3)元素W与Y同周期,0.1 mol的W单质能从酸中置换出2.24 L H2(标准状况),则W单质的元素名称为
(4)Y与G同族,且G的单质常温下呈液态,Y和G两种元素相比较,非金属性较强的是
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的含氧酸的酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,请依据该表回答问题。
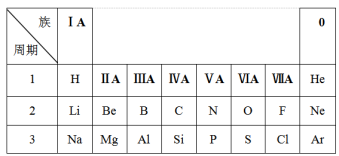
(1)第2周期VIIA族元素的原子结构示意图是___________ ,该元素与同周期IA族元素组成的化合物类型是___________ (填“离子化合物”或“共价化合物”)。
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是___________ (填化学式,下同);具有两性的是___________ 。加热时,碳单质能与S的最高价氧化物对应的水化物的浓溶液反应,写出该反应的化学方程式___________ 。
(3)下列判断正确的是___________(填标号)。

(1)第2周期VIIA族元素的原子结构示意图是
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是
(3)下列判断正确的是___________(填标号)。
| A.最低负化合价的绝对值:P>S |
| B.非金属性:P>N |
| C.离子半径:Mg2+>O2− |
| D.还原性:S2−>Cl− |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】同一周期相邻的A、B、C三种元素,都是短周期元素,A的最高价氧化物的化学式是A2O,11.6gB的氢氧化物恰好能与200mL2mol/L盐酸完全反应,B原子核中质子数与中子数相等。回答以下问题:
(1)B的相对原子质量______ ,原子序数______ 。
(2)A和C各是什么元素?A______ ,B______ 。
(3)写出A、C最高价氧化物对应水合物反应的离子方程式:________________
(1)B的相对原子质量
(2)A和C各是什么元素?A
(3)写出A、C最高价氧化物对应水合物反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,针对表中的①〜⑩种元素,填写下列空白(涉及具体元素对应化学符号表示):
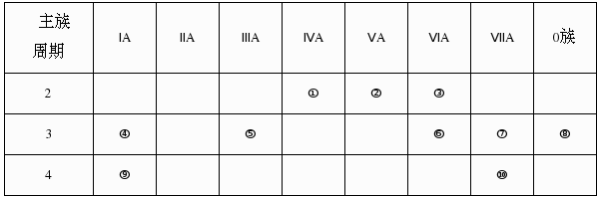
(1)在这些元素中,化学性质最不活泼的是_______ (填元素符号)元素⑩在周期表中的位置______ 。形成化合物最多的元素______ (填序号)
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是:______ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:_________________ .
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是________ 。
(5)元素③的氢化物的结构式为_____ ;该氢化物在一定条件下可以生成另一种③的氢化物和③的单质。

(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(5)元素③的氢化物的结构式为
您最近一年使用:0次



