某兴趣小组用下图装置研究原电池的工作原理。
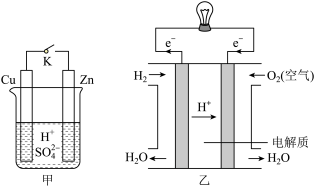
(1)甲中K断开时,装置中发生反应的离子方程式为_______________________ ;K闭合时,Cu棒上的现象为________ ,它为原电池的________ (填“正”或“负”)极。
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的________ (填“正”或“负”)极,发生________ (填“氧化”或“还原”)反应。
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式:_______________________________________________ 。

(1)甲中K断开时,装置中发生反应的离子方程式为
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式:
更新时间:2020-06-04 15:30:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】将铁片、铜片通过导线相连,置于稀硫酸中,构成原电池。
(1)该原电池的负极是______ (填“铁片”或“铜片”),其电极反应式______ ;
(2)正极产生的现象是______ ,其发生的反应的类型是______ 反应;(填“氧化”或“还原”)
(3)若导线中通过了0.4mol电子,负极材料的质量理论上减少______ 克。
(1)该原电池的负极是
(2)正极产生的现象是
(3)若导线中通过了0.4mol电子,负极材料的质量理论上减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。回答下列问题:

(1)下列叙述中,不正确的是___________ 。
A.B 中铁片是负极,C 中铁片是正极 B.三个烧杯中铁片表面均无气泡产生 C.产生气泡的速率 A 中比B中慢 D.C 溶液中 向Zn片电极移动
向Zn片电极移动
(2)装置 B中能量转化的主要形式是________________ ;
(3)装置 B中正极反应式为__________________ ;
(4)装置 C负极反应式为________________________ ;
(5)装置 A 中发生反应的离子方程式________________ ;
(6)Ba(OH)2·8H2O 晶体与 NH4C1晶体的反应属于_______ 反应(填“吸热”或“放热”)若把此反应设计成原电池,你认为是否可行?_______ (填“是”或“否”)。

(1)下列叙述中,不正确的是
A.B 中铁片是负极,C 中铁片是正极 B.三个烧杯中铁片表面均无气泡产生 C.产生气泡的速率 A 中比B中慢 D.C 溶液中
 向Zn片电极移动
向Zn片电极移动(2)装置 B中能量转化的主要形式是
(3)装置 B中正极反应式为
(4)装置 C负极反应式为
(5)装置 A 中发生反应的离子方程式
(6)Ba(OH)2·8H2O 晶体与 NH4C1晶体的反应属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是一个化学过程的示意图,回答下列问题:

(1)甲池是___________ 装置,电极B的名称是___________ 。
(2)甲装置中通入C3H8的电极反应____________ ,丙装置中D极的产物是___________ (写化学式)。
(3)一段时间,当乙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=__________ 。(已知:NaCl溶液足量,电解后溶液体积为200 mL)。
(4)若要使乙池恢复电解前的状态,应向乙池中加入__________ (写物质化学式)。

(1)甲池是
(2)甲装置中通入C3H8的电极反应
(3)一段时间,当乙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=
(4)若要使乙池恢复电解前的状态,应向乙池中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据原电池原理,人们研制出了性能各异的化学电池。
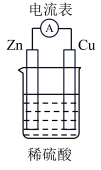
(1)如图装置中,Cu片作_______ (填“正极”或“负极”),Zn片上发生反应的电极反应式为_______ ,能证明化学能转化为电能的实验现象是_______ 。
(2)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示。其总反应为:2Mg+O2+2H2O=2Mg(OH)2。下列说法正确的是_______ (填字母)。
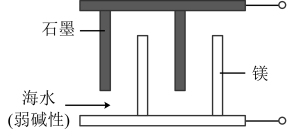
a.石墨是电池的负极 b.Mg发生氧化反应
(1)如图装置中,Cu片作

(2)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示。其总反应为:2Mg+O2+2H2O=2Mg(OH)2。下列说法正确的是

a.石墨是电池的负极 b.Mg发生氧化反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2022年11月,“神舟十五号”载人飞船成功发射,创下了我国在超低温天气成功发射载人飞船的新纪录。肼(N2H4)是火箭常用高能燃料,可与O2发生反应:N2H4(g)+O2(g)=N2(g)+2H2O(g)。请回答下列问题:
(1)相关化学键的键能[常温常压下,断裂或形成1mol(理想)气体分子化学键所吸收或放出的能量]数据如表所示:
①O(g)+O(g)→O2(g),生成0.5molO2(g)会_____ (填“吸收”或“放出”)_____ kJ能量。
②1molN2H4(g)在O2中完全燃烧_____ (填“吸收”或“放出”)_____ kJ能量。
(2)N2H4(g)+O2(g)=N2(g)+2H2O(l)可设计为燃料电池,装置如图所示。
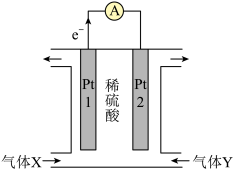
①气体Y为_____ (填化学式),该装置工作时,SO 移向电极
移向电极_____ (填“Pt1”或“Pt2”)。
②电极Pt1为_____ (填“负极”或“正极”),发生的电极反应为_____ 。
③该装置工作一段时间后,电解质溶液的酸性_____ (填“增强”、“减弱”或“不变”)。
(1)相关化学键的键能[常温常压下,断裂或形成1mol(理想)气体分子化学键所吸收或放出的能量]数据如表所示:
| 化学键 | N-N | H-N | O=O | N≡N | H-O |
| 键能E/(kJ•mol-1) | 159 | 389 | 498 | 946 | 465 |
①O(g)+O(g)→O2(g),生成0.5molO2(g)会
②1molN2H4(g)在O2中完全燃烧
(2)N2H4(g)+O2(g)=N2(g)+2H2O(l)可设计为燃料电池,装置如图所示。

①气体Y为
 移向电极
移向电极②电极Pt1为
③该装置工作一段时间后,电解质溶液的酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A. ;B.
;B. 。上述反应中能设计成原电池的是
。上述反应中能设计成原电池的是___________ (填字母)。
(2)将纯锌片和纯铜片按如图甲、乙所示方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:___________ (填字母)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ (填“>”、“<”或“=”)乙。
③请写出图中构成原电池的装置负极的电极反应式___________ 。
④当乙中产生11.2L(标准状况)气体时,转移电子为___________ mol。
(1)现有如下两个反应:A.
 ;B.
;B. 。上述反应中能设计成原电池的是
。上述反应中能设计成原电池的是(2)将纯锌片和纯铜片按如图甲、乙所示方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的装置负极的电极反应式
④当乙中产生11.2L(标准状况)气体时,转移电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】图中甲池的总反应式为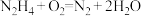 。
。

(1)甲池中负极上的电极反应式为_____________________ 。
(2)乙池中石墨电极上电极反应式为_________________________________ 。
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的_______________ 。
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为_________________ g。
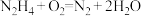 。
。
(1)甲池中负极上的电极反应式为
(2)乙池中石墨电极上电极反应式为
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“化学为了使生活更美好”。人们应用原电池原理制作了多种电池,以满足不同的需要。现有以下三种乙醇燃料电池。

(1)碱性乙醇燃料电池中,电极a上发生的电极反应式为_______ 。
(2)酸性乙醇燃料电池中,电极b上发生的电极反应式为_______ 。
(3)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO32-向电极_______ 移动(填“a”或“b”),电极b上发生的电极反应式为_______ 。
(4)铅酸蓄电池放电时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。若电解液体积为2L(忽略溶液体积变化),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol·L-1下降到_______ mol·L-1。

(1)碱性乙醇燃料电池中,电极a上发生的电极反应式为
(2)酸性乙醇燃料电池中,电极b上发生的电极反应式为
(3)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO32-向电极
(4)铅酸蓄电池放电时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。若电解液体积为2L(忽略溶液体积变化),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol·L-1下降到
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
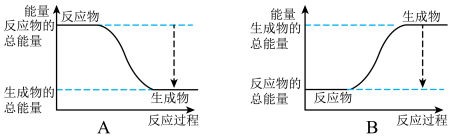
【推荐1】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。
(1)下图能正确表示该反应中能量变化的是________ 。
(2)氢氧燃料电池的总反应方程式为2H2+O2=2H2O。其中,氢气在________ 极发生________ 反应。电路中每转移0.2 mol电子,标准状况下消耗H2的体积是________ L。
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池,并回答下列问题:
①该电池的正极材料是______ ,负极材料是 ______ ,电解质溶液是 ______ 。
②正极上出现的现象是______ ,负极上出现的现象是 ______ 。
(1)下图能正确表示该反应中能量变化的是

(2)氢氧燃料电池的总反应方程式为2H2+O2=2H2O。其中,氢气在
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池,并回答下列问题:
①该电池的正极材料是
②正极上出现的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如下图所示:
(1)该反应为________ 反应(填“吸热”或“放热”)。

(2)若要使该反应的反应速率加快,下列措施可行的是_______ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,画出原电池的装置图,并在图上标出正负极材料、电解质溶液名称_______ ,写出正负极电极反应式:正极__________ ,负极_______ 。
(4)氢氧燃料电池汽车作为上海世博园中的交通工具之一,以稀硫酸为介质的这种电池的正极电极反应式为_________________________ 。
(1)该反应为

(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,画出原电池的装置图,并在图上标出正负极材料、电解质溶液名称
(4)氢氧燃料电池汽车作为上海世博园中的交通工具之一,以稀硫酸为介质的这种电池的正极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.请根据化学反应与热能的有关知识,填写下列空白:
(1)下列属于吸热反应的是___________ (填序号)。
①酸碱中和反应 ②燃烧木炭取暖 ③氢氧化钡晶体和氯化铵晶体反应
④煅烧石灰石制生石灰 ⑤铝热反应 ⑥碘升华
(2)已知H2、O2和H2O分子中的化学键H-H、O=O、O-H键能分别为Q1kJ/mol、Q2kJ/mol、Q3kJ/mol,由此可以推知下列关系正确的是___________ (填字母编号)。
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
II.已知2mol氢气燃烧生成液态水时放出572kJ热量。
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量______ (填“>”“<”或“=”)572kJ。
(4)写出表示氢气燃烧热的热化学方程式____________________________________ 。
(5)若将上述氢气燃烧反应设计成原电池,电解质溶液用KOH,请写出该电池负极的电极反应式:________________________ ,若电解质为熔融氧化物,产物在______ 极附近产生。
(1)下列属于吸热反应的是
①酸碱中和反应 ②燃烧木炭取暖 ③氢氧化钡晶体和氯化铵晶体反应
④煅烧石灰石制生石灰 ⑤铝热反应 ⑥碘升华
(2)已知H2、O2和H2O分子中的化学键H-H、O=O、O-H键能分别为Q1kJ/mol、Q2kJ/mol、Q3kJ/mol,由此可以推知下列关系正确的是
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
II.已知2mol氢气燃烧生成液态水时放出572kJ热量。
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量
(4)写出表示氢气燃烧热的热化学方程式
(5)若将上述氢气燃烧反应设计成原电池,电解质溶液用KOH,请写出该电池负极的电极反应式:
您最近一年使用:0次




