(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氢气从__ 口通入(填“a”或“b”),Y极为电池的___ (填“正”或“负”)极。
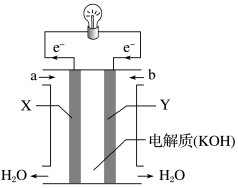
(2)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Ag2O是__ 极,Zn发生__ 反应。
②电子由__ 极流向__ 极(填“Zn”或“Ag2O”),当电路通过0.1mol电子时,负极消耗物质的质量是___ g。

(2)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Ag2O是
②电子由
更新时间:2020-06-25 13:22:26
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
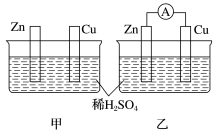
(1)以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液氢离子浓度均减小
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向
F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为_______ ;乙为_______ 。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:_______ ,总反应:_______ 。当电路中转移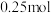 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为_______ g。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液氢离子浓度均减小
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向

F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的主要形式:甲为
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:
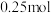 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)某兴趣小组为研究原电池原理,设计如图装置。
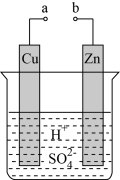
①a和b不连接时,烧杯中发生反应的离子方程式是_____ 。
②a和b用导线连接,Cu极为原电池____ 极(填“正”或“负”),Zn极发生____ 反应,外电路中,电子流向____ 极(填“正”或“负”,下同),内电路溶液中,SO 移向
移向____ 极。
(2)有同学想把CuO与稀H2SO4的反应设计成原电池,你认为是否可行____ (填“是”或“否”),理由是____ 。
(1)某兴趣小组为研究原电池原理,设计如图装置。

①a和b不连接时,烧杯中发生反应的离子方程式是
②a和b用导线连接,Cu极为原电池
 移向
移向(2)有同学想把CuO与稀H2SO4的反应设计成原电池,你认为是否可行
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】利用原电池原理可以探究物质的还原性强弱。实验中,电流表指针的偏转方向均与电子的移动方向一致,阴离子交换膜只允许阴离子通过。回答下列问题:
(1)按照如图连接装置后,电流表指针向Co电极偏转,该原电池的总反应离子方程式为___________ ,由此可以判断:Co的还原性比Zn的还原性___________ (填强或弱)。

(2)上图中Co电极和CoSO4溶液接触的界面两侧存在电势差,称为该电极的电极电势,该电极的电对符号为Co2+/Co,电对中Co2+是氧化型,Co是还原型。金属离子的浓度为1mol/L时部分电极的电极电势如下表所示:
①根据第(1)小题中实验结论和表中数据推测:电极电势越低,电对中还原型的还原性越___________ (填强或弱)。
②为验证上述推测,利用0.34和-0.41两组数据进行实验,请补全原电池装置。

电极X的化学式为___________ ,某浓度的溶液Y为___________ ,某浓度的溶液Z为___________ 。
③若上述推测成立,电流表指针向___________ (填X或Cu)电极偏转,负极的电极反应式为___________ 。
(1)按照如图连接装置后,电流表指针向Co电极偏转,该原电池的总反应离子方程式为

(2)上图中Co电极和CoSO4溶液接触的界面两侧存在电势差,称为该电极的电极电势,该电极的电对符号为Co2+/Co,电对中Co2+是氧化型,Co是还原型。金属离子的浓度为1mol/L时部分电极的电极电势如下表所示:
| 电对符号 | Cu2+/Cu | Co2+/Co | Cd2+/Cd | Zn2+/Zn |
| 电极电势/V | 0.34 | -0.28 | -0.41 | -0.76 |
①根据第(1)小题中实验结论和表中数据推测:电极电势越低,电对中还原型的还原性越
②为验证上述推测,利用0.34和-0.41两组数据进行实验,请补全原电池装置。

电极X的化学式为
③若上述推测成立,电流表指针向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: +4H++3e→NO+2H2O。 KMnO4、Na2CO3、KI、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e→NO+2H2O。 KMnO4、Na2CO3、KI、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的离子方程式:_______________________
(2)反应中若产生0.3mol气体,则转移电子的物质的量是_________ mol。
(3)若把上述反应组成原电池,则在负极发生反应的离子是_________
II. (4)把酸性高锰酸钾溶液缓缓通入Na2S的水溶液中,开始出现黄色沉淀;写出该反应的离子方程式_________________________________________________________________________________ ,随后继续通入酸性高锰酸钾溶液,沉淀逐渐消失,溶液变澄清,写出该反应的离子方程式_____________________________________________________________________________ .
 +4H++3e→NO+2H2O。 KMnO4、Na2CO3、KI、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e→NO+2H2O。 KMnO4、Na2CO3、KI、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。(1)写出并配平该氧化还原反应的离子方程式:
(2)反应中若产生0.3mol气体,则转移电子的物质的量是
(3)若把上述反应组成原电池,则在负极发生反应的离子是
II. (4)把酸性高锰酸钾溶液缓缓通入Na2S的水溶液中,开始出现黄色沉淀;写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据原电池原理,结合装置图,按要求解答问题:
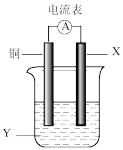
(1)若X为Zn,Y为硫酸铜溶液,则X为____ (填电极名称),判断依据:____ ;铜电极的名称是____ ,溶液中的Cu2+移向____ (填“Cu”或“X”)电极。
(2)若X为银,Y为硝酸银溶液,则X为____ (填电极名称),判断依据:____ ;铜电极的名称是____ ,溶液中的Ag+移向____ (填“Cu”或“X”)电极。
(3)若X为Fe,Y为浓硝酸,则Cu为____ (填电极名称),铜电极可能观察到的现象是____ 。

(1)若X为Zn,Y为硫酸铜溶液,则X为
(2)若X为银,Y为硝酸银溶液,则X为
(3)若X为Fe,Y为浓硝酸,则Cu为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:
A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A._____ ,B._____ 。(填“能”或“不能”)
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是____________ 。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲________ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的负极电极反应式_________________________ 。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入__ 极(填a或b),电子从____ (填a或b)极流出。
(1)现有如下两个反应:
A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A.
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空:

(1)写出电解饱和食盐水的离子方程式_________ 。
(2)离子交换膜的作用除了能得到纯度更高的氢氧化钠溶液外,还可以______ 。
(3)精制饱和食盐水从图中_____ 位置补充,氢氧化钠溶液从图中_____ 位置流出。(选填“a”、“b”、“c”或“d”)
(4)氢气是很有前景的新能源,氢氧燃料电池的能量转化率高。下图是氢氧燃料碱性电池装置图,电解质溶液为氢氧化钾溶液,写出负极的电极反应式_______ 。

(5)氯碱工业制得的化工产品KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式___________ 。
(6)ClO2是高效的消毒杀菌剂,消毒反应原理是高价氯还原为−1价的氯离子。现有1molClO2,其杀菌能力相当于____ L标况下Cl2 的杀菌能力(杀菌能力仅按得电子的物质的量计)。

(1)写出电解饱和食盐水的离子方程式
(2)离子交换膜的作用除了能得到纯度更高的氢氧化钠溶液外,还可以
(3)精制饱和食盐水从图中
(4)氢气是很有前景的新能源,氢氧燃料电池的能量转化率高。下图是氢氧燃料碱性电池装置图,电解质溶液为氢氧化钾溶液,写出负极的电极反应式

(5)氯碱工业制得的化工产品KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(6)ClO2是高效的消毒杀菌剂,消毒反应原理是高价氯还原为−1价的氯离子。现有1molClO2,其杀菌能力相当于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是____ ,负极发生的电极反应方程式为:____ 。若反应消耗32.5 g 负极材料,则电池中转移电子的数目为____ 。

(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是
2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____ 。
①上述反应可以在酸性条件下进行 ②上述反应不是可逆反应
③放电时正极金属Cd的质量增加 ④放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的_____ (填“正”或“负”)极,X极的电极反应方程为_______ 。

(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是

(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是
2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是①上述反应可以在酸性条件下进行 ②上述反应不是可逆反应
③放电时正极金属Cd的质量增加 ④放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化主要形式是___ ,在导线中电子流动方向为___ (用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___ 。
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为___ (填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___ 。
③若A极产生7.00gN2,则此时B极产生___ LH2(标准状况下)。

(1)氢氧燃料电池的能量转化主要形式是
(2)正极反应的电极反应方程式为
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为
②该系统工作时,A极的电极反应式为
③若A极产生7.00gN2,则此时B极产生
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷燃烧生成CO和液态水时放出38kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的 =
=___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。

①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的浓度为___________ mol/L。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(4)某种甲烷燃料电池的工作原理如图所示

甲烷通入的一极为电源的___________ 极,该电极反应式:___________ 当电路中累计有2mol电子通过时,消耗的氧气体积为(在标准状况下)___________ L
(1)已知25℃、101kPa时,1g甲烷燃烧生成CO和液态水时放出38kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的
 =
=(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(4)某种甲烷燃料电池的工作原理如图所示

甲烷通入的一极为电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某校化学兴趣小组为了探究原电池工作原理,进行如下系列实验。

请分析实验结果并回答相应问题。
(1)实验一中,铜片、锌片表面均有红色物质析出,电流表指针偏转,但较短时间内电流明显减小。实验结束时测得锌片减少了3.94 g,铜片增重了3.84 g,则该原电池的工作效率是____ (指参加原电池反应的锌占反应总量的百分率)。
(2)实验二中,刚将铜片、锌片插入溶液中时电流表指针偏转,但立即就归零了。为什么锌的电子不能持续通过导线流向铜极给Cu2+?____________________________________ 。
(3)实验三中,盐桥中K+流向____ (填“ZnSO4”或“CuSO4”)溶液,如果Zn的消耗速率为1×10-3mol·s-1,则K+的迁移速率为____ mol·s-1。与实验一比较,实验三原电池的工作效率大大提高,原因是_______________________________________ 。
(4)根据实验一、二、三可得出的结论是________________________ (写出两点即可)。

请分析实验结果并回答相应问题。
(1)实验一中,铜片、锌片表面均有红色物质析出,电流表指针偏转,但较短时间内电流明显减小。实验结束时测得锌片减少了3.94 g,铜片增重了3.84 g,则该原电池的工作效率是
(2)实验二中,刚将铜片、锌片插入溶液中时电流表指针偏转,但立即就归零了。为什么锌的电子不能持续通过导线流向铜极给Cu2+?
(3)实验三中,盐桥中K+流向
(4)根据实验一、二、三可得出的结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_______(填字母)。
(2)下图为原电池装置示意图:
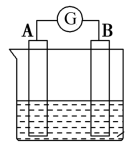
①若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,写出正极的电极反应式:_______ ,反应过程中溶液的酸性_______ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出1.68 L(标准状况)气体时,电路中有_______ 个电子通过了导线(用NA表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为_______ (填“正极”或“负极”);写出该电极的电极反应式:_______ 。
③燃料电池是一种具有应用前景的绿色电源, 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_______ (填“正极”或“负极”),若线路中转移2 mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。

④为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是_______ (填序号)。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_______(填字母)。
A. | B. |
C. | D. |

①若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,写出正极的电极反应式:
②若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为
③燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是 在标准状况下的体积为
在标准状况下的体积为
④为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
您最近一年使用:0次



