能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_______(填字母)。
(2)下图为原电池装置示意图:
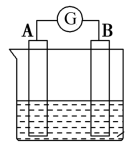
①若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,写出正极的电极反应式:_______ ,反应过程中溶液的酸性_______ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出1.68 L(标准状况)气体时,电路中有_______ 个电子通过了导线(用NA表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为_______ (填“正极”或“负极”);写出该电极的电极反应式:_______ 。
③燃料电池是一种具有应用前景的绿色电源, 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_______ (填“正极”或“负极”),若线路中转移2 mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。

④为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是_______ (填序号)。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_______(填字母)。
A. | B. |
C. | D. |

①若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,写出正极的电极反应式:
②若A为镁片,B为铝片,电解质为NaOH溶液,则铝片为
③燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是 在标准状况下的体积为
在标准状况下的体积为
④为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
更新时间:2022-06-11 16:27:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】Ⅰ.如下图所示,将2molA气体和1molB气体充入一容积可变的密闭容器中,发生反应:2A(g)+B(g) 2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为
2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为__________ ;该条件下的反应的平衡常数为_____________ 。

Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的热化学方程式_____________________________ 。
(2)利用该反应可设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式_______________ 。
(3)用石墨做阳极,铁棒做阴极,电解硫酸铜溶液,则石墨棒上的电极反应式为________________________ ;如果起始时盛有1000mL PH=5的硫酸铜溶液(25℃)(足量),一段时间后溶液的PH变为1,若要使溶液恢复到起始浓度(忽略溶液体积变化),可向溶液中加入__________ (填物质名称),其质量约为___________ 。
 2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为
2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为
Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的热化学方程式
(2)利用该反应可设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式
(3)用石墨做阳极,铁棒做阴极,电解硫酸铜溶液,则石墨棒上的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
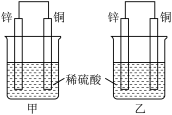
①下列说法正确的是_______ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置正极的电极反应式_______ 。

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的装置正极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】金属的腐蚀
(1)概念:金属或合金与周围的_______ 发生_______ 反应而引起损耗的现象。其实质是金属原子_______ 电子变为阳离子,金属发生_______ 反应。
(2)根据与金属接触的_______ 不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如_______ 等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而_______ 。
②电化学腐蚀:当_______ 的金属与_______ 溶液接触时会发生_______ 反应,比较_______ 的金属发生氧化反应而被腐蚀。
(1)概念:金属或合金与周围的
(2)根据与金属接触的
①化学腐蚀:金属与其表面接触的一些物质(如
②电化学腐蚀:当
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据原电池的工作原理分析判断(填写“正极”或“负极”)。
(1)由组成原电池的电极材料判断。一般是活动性较强的金属为_______ 极,活动性较弱的金属或能导电的非金属为_______ 极。
(2)根据电流方向或电子流动方向判断。电流由_______ 极流向_______ 极;电子由_______ 极流向_______ 极。
(3)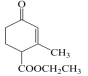 中含有的官能团名称是
中含有的官能团名称是_______ ,_______ ,_______ 。
(1)由组成原电池的电极材料判断。一般是活动性较强的金属为
(2)根据电流方向或电子流动方向判断。电流由
(3)
 中含有的官能团名称是
中含有的官能团名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学设计一个电池(如图所示),探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
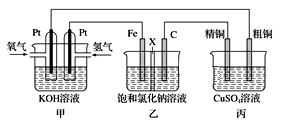
(1)通入氧气的电极为___________ (填正极或负极),该电极反应式为___________ 。
(2)铁电极为___________ (填阳极或阴极),乙中总反应离子方程式为___________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将___________ (填“增大”“减小”或“不变”)。
(4)若甲中消耗0.005mol O2,丙中精铜增重___________ g。

(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若甲中消耗0.005mol O2,丙中精铜增重
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.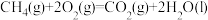
b.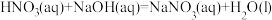
c.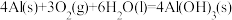
d.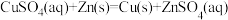
(2)某小组为探究 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。___________ ,B电极的电极反应方程式为___________ 。 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式___________ 。
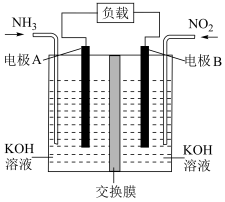
(5)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示: 电极为
电极为___________ (填“正极”或“负极), 电极上发生的电极反应式为
电极上发生的电极反应式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.
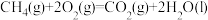
b.
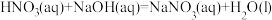
c.
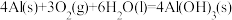
d.
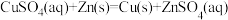
(2)某小组为探究
 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为 向
向
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式(5)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据题中提供的信息,请回答下列问题:
(1)学习原电池原理后,小江同学根据反应 设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是
设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是______ ,正极材料可能是______ (填一种)。
(2)小河同学设计了如图所示的原电池,利用不同的电解质溶液进行实验。______ 。
②当以NaOH溶液作为电解质溶液时,电流表指针也发生了偏转,若负极失去1mol电子,理论上负极的质量变化为______ g。
(3)燃料电池是一种高效化学电池,以稀硫酸为电解质溶液的氢氧燃料电池的工作原理如图所示,a和b都是Pt电极(惰性电极)。______ 。
②该电池工作时,电解质溶液中 的移动方向是
的移动方向是______ 。(填“a向b”或“b向a”,下同),外电路中电子的流动方向是______ 。
③若将a极通入的气体换为 ,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为
,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为______ 。当a极有1mol 发生反应时,理论上b极参加反应的氧气在标准状况下的体积为
发生反应时,理论上b极参加反应的氧气在标准状况下的体积为______ L。
(4)小海同学在做氢气的制备实验时,用锌粒和稀硫酸为原料,结果发现反应速率较慢。其他同学给出以下建议,其中能加快制备 的反应速率的有______(填字母)。
的反应速率的有______(填字母)。
(1)学习原电池原理后,小江同学根据反应
 设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是
设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是(2)小河同学设计了如图所示的原电池,利用不同的电解质溶液进行实验。

②当以NaOH溶液作为电解质溶液时,电流表指针也发生了偏转,若负极失去1mol电子,理论上负极的质量变化为
(3)燃料电池是一种高效化学电池,以稀硫酸为电解质溶液的氢氧燃料电池的工作原理如图所示,a和b都是Pt电极(惰性电极)。

②该电池工作时,电解质溶液中
 的移动方向是
的移动方向是③若将a极通入的气体换为
 ,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为
,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为 发生反应时,理论上b极参加反应的氧气在标准状况下的体积为
发生反应时,理论上b极参加反应的氧气在标准状况下的体积为(4)小海同学在做氢气的制备实验时,用锌粒和稀硫酸为原料,结果发现反应速率较慢。其他同学给出以下建议,其中能加快制备
 的反应速率的有______(填字母)。
的反应速率的有______(填字母)。| A.将稀硫酸换成质量分数为98%的浓硫酸 | B.向反应液中滴入几滴硫酸铜溶液 |
| C.改换合适的装置并适当加热 | D.将锌粒换成质量相等的锌粉 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极b作
的原理示意图。电极b作_______ 极,表面发生的电极反应为_______ 。

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如下图所示,该电池从浓缩海水中提取 的同时又获得了电能。
的同时又获得了电能。
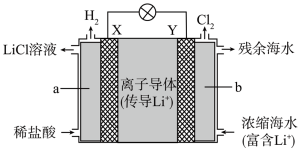
①X为_______ 极,Y极反应式为_______ 。
②Y极生成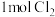 时,
时,_______ 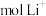 移向
移向_______ (填“X”或“Y”)极。
(3)一种以肼(N2H4)为液体燃料的电池装置如下图所示。该电池用空气中的氧气作氧化剂, 作电解质。负极反应式为
作电解质。负极反应式为_______ ;正极反应式为_______ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以
 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极b作
的原理示意图。电极b作
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如下图所示,该电池从浓缩海水中提取
 的同时又获得了电能。
的同时又获得了电能。
①X为
②Y极生成
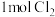 时,
时,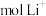 移向
移向(3)一种以肼(N2H4)为液体燃料的电池装置如下图所示。该电池用空气中的氧气作氧化剂,
 作电解质。负极反应式为
作电解质。负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某超市中一种电池外壳的纸层包装上印有如图所示的文字,根据要求回答:

(1)该电池的种类是______ (填序号).
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中,毒性最大的是______ (写元素符号).
(3)该电池的使用和性能,下列说法中不正确的是______
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(4)已知该电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池放电时的正负极反应方程式:
负极___________________________________
正极___________________________________

(1)该电池的种类是
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中,毒性最大的是
(3)该电池的使用和性能,下列说法中不正确的是
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(4)已知该电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池放电时的正负极反应方程式:
负极
正极
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。______ 极,发生______ (填“氧化”或“还原”)反应。
②Cu棒,上发生的电极反应是______ 。
③溶液中H+向______ (填“Zn”或“Cu”)电极定向移动。
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是______ (填“Zn”或“Cu”),正极的电极反应是______ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=______ mol。
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。
该原电池电解质是KOH溶液,写出正极的电极反应______ 。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。

②Cu棒,上发生的电极反应是
③溶液中H+向
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。
该原电池电解质是KOH溶液,写出正极的电极反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.浩瀚的海洋里蕴藏着丰富的化学资源。利用海水可以提取溴和镁,提取过程如下:
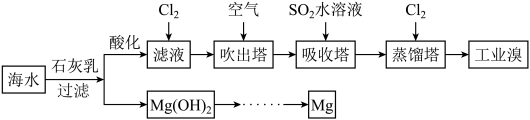
(1)氯元素在周期表中的位置是___________ 。
(2)提取溴的过程中,滤液中通入Cl2生成Br2的离子方程式___________ 。经过2次Br→Br2转化的目的是___________ 。
(3)吸收塔中发生反应的离子方程式是___________ 。
(4)Mg(OH)2的电子式为___________ ,通过将Mg(OH)2转化为无水MgCl2以制备单质Mg,无水MgCl2制取单质Mg的化学方程式是___________ 。
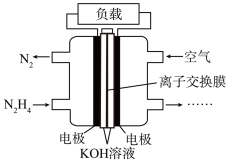
Ⅱ.为减少汽车尾气的污染,逐步向着新能源汽车发展。肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:
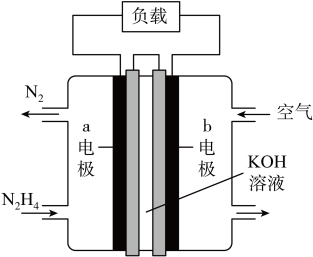
(5)该燃料电池中正极通入的物质是___________ ,负极发生的反应式为___________ 。
(6)电池工作时, 移向
移向___________ 电极(填“a”或“b”)。
(7)当电池放电转移10mol电子时,至少消耗燃料肼___________ g。

(1)氯元素在周期表中的位置是
(2)提取溴的过程中,滤液中通入Cl2生成Br2的离子方程式
(3)吸收塔中发生反应的离子方程式是
(4)Mg(OH)2的电子式为
Ⅱ.为减少汽车尾气的污染,逐步向着新能源汽车发展。肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:

(5)该燃料电池中正极通入的物质是
(6)电池工作时,
 移向
移向(7)当电池放电转移10mol电子时,至少消耗燃料肼
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氢能是发展中的新能源,它的利用包括氢的制备和储存。回答下列问题:
(1)图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
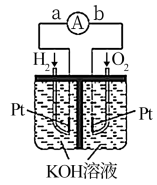
①在导线中电子流动方向为_______ (用a、b表示)
②正极反应式为_______ 。
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此,储氢是关键技术之一。
①某些金属氢化物也可做储氢材料,在恒温恒容的密闭容器中,某储氢反应: 达到化学平衡。下列有关叙述正确的是
达到化学平衡。下列有关叙述正确的是_______ 。
a.v(放氢)=v(吸氢)
b.吸收y mol H2只需1 mol MHx
c.若通入惰性气体Ar,压强增大,反应速率增大
d.容器内气体压强保持不变
②金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2 2LiH
2LiH
Ⅱ.LiH+H2O=LiOH+H2↑
用锂吸收224 L(标准状况)H2,生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为_______ mol。
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______ 。
(1)图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为
②正极反应式为
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此,储氢是关键技术之一。
①某些金属氢化物也可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:
 达到化学平衡。下列有关叙述正确的是
达到化学平衡。下列有关叙述正确的是a.v(放氢)=v(吸氢)
b.吸收y mol H2只需1 mol MHx
c.若通入惰性气体Ar,压强增大,反应速率增大
d.容器内气体压强保持不变
②金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2
 2LiH
2LiH Ⅱ.LiH+H2O=LiOH+H2↑
用锂吸收224 L(标准状况)H2,生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
您最近一年使用:0次



