某超市中一种电池外壳的纸层包装上印有如图所示的文字,根据要求回答:

(1)该电池的种类是______ (填序号).
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中,毒性最大的是______ (写元素符号).
(3)该电池的使用和性能,下列说法中不正确的是______
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(4)已知该电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池放电时的正负极反应方程式:
负极___________________________________
正极___________________________________

(1)该电池的种类是
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中,毒性最大的是
(3)该电池的使用和性能,下列说法中不正确的是
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(4)已知该电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池放电时的正负极反应方程式:
负极
正极
更新时间:2018-05-12 01:37:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)氨的催化氧化反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①反应在第lmin到第2min时,NH3的平均反应速率为_____ 。
②反应在第3min时改变了条件,改变的条件可能是_____ (填序号)。
A.使用催化剂 B.减小压强 C.升高温度 D.增加O2的浓度
③说明4NH3(g)+5O2(g) 4NO(g)+6H2O(g)达到平衡状态的是
4NO(g)+6H2O(g)达到平衡状态的是_____ (填序号)。
A.单位时间内生成nmolNO的同时生成nmolNH3
B.百分含量w(NH3)=w(NO)
C.反应速率v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6
D.在恒温恒容的容器中,混合气体的平均相对分子质量不再变化
(2)图是某燃料电池的结构示意图,电解质为硫酸溶液。回答下列问题。

①若使用甲烷为燃料,则a极的电极反应式为_____ 。
②若使用氢气为燃料,电解质溶液换成NaOH溶液,去掉质子交换膜。a极的电极反应式为_____ 。每转移1mol电子,消耗H2的体积为_____ L。(标准状况下)。
(1)氨的催化氧化反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) △H<0,是工业制硝酸的基础反应,在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:| c(NH3)mol/L | c(O2)mol/L | c(NO)mol/L | |
| 第0min | 0.8 | 1.6 | 0 |
| 第1min | a | 1.35 | 0.2 |
| 第2min | 0.3 | 0.975 | 0.5 |
| 第3min | 0.3 | 0.975 | 0.5 |
| 第4min | 0.7 | 1.475 | 0.1 |
②反应在第3min时改变了条件,改变的条件可能是
A.使用催化剂 B.减小压强 C.升高温度 D.增加O2的浓度
③说明4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)达到平衡状态的是
4NO(g)+6H2O(g)达到平衡状态的是A.单位时间内生成nmolNO的同时生成nmolNH3
B.百分含量w(NH3)=w(NO)
C.反应速率v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6
D.在恒温恒容的容器中,混合气体的平均相对分子质量不再变化
(2)图是某燃料电池的结构示意图,电解质为硫酸溶液。回答下列问题。

①若使用甲烷为燃料,则a极的电极反应式为
②若使用氢气为燃料,电解质溶液换成NaOH溶液,去掉质子交换膜。a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据原电池的本质判断,下列化学(或离子)方程式正确,且能设计成原电池的是___________。
(2)利用反应“ ”设计一个原电池,正极的电极反应式:
”设计一个原电池,正极的电极反应式:___________ 。
(3)以Pt为电极的氢氧燃料电池的工作原理示意图如图所示,稀 为电解质溶液。
为电解质溶液。___________ 极,发生___________ 反应(“氧化”或“还原”),写出b极的电极反应式___________ 。
②该电池提供 ,理论上消耗的氢气在标准状况下的体积为
,理论上消耗的氢气在标准状况下的体积为___________ L。
(1)根据原电池的本质判断,下列化学(或离子)方程式正确,且能设计成原电池的是___________。
A.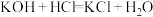 | B.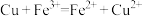 |
C.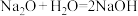 | D.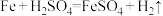 |
(2)利用反应“
 ”设计一个原电池,正极的电极反应式:
”设计一个原电池,正极的电极反应式:(3)以Pt为电极的氢氧燃料电池的工作原理示意图如图所示,稀
 为电解质溶液。
为电解质溶液。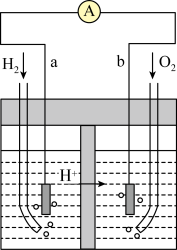
②该电池提供
 ,理论上消耗的氢气在标准状况下的体积为
,理论上消耗的氢气在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
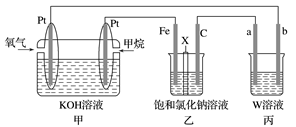
(1)石墨电极(C)作______ 极,甲中甲烷燃料电池的负极反应式为___________ 。
(2)若消耗2.24L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为_______ L。
(3)丙中以 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。
(4)若丙中以稀 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为_________ 。
Ⅱ.依据氧化还原反应: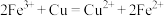 设计的原电池如图所示。请回答下列问题:
设计的原电池如图所示。请回答下列问题:

(5)电极X的材料是_______ (填化学式,下同);电解质Y是________ 。
(6)当X电极的质量减小了3.2g时,流经电流计的电子的物质的量为_______ mol。

(1)石墨电极(C)作
(2)若消耗2.24L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为
(3)丙中以
 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是_______(填字母)。| A.a电极为纯铜 | B.粗铜接电源正极,发生还原反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 | D.利用阳极泥可回收Ag、Pt、Au等金属 |
 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为Ⅱ.依据氧化还原反应:
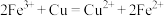 设计的原电池如图所示。请回答下列问题:
设计的原电池如图所示。请回答下列问题:
(5)电极X的材料是
(6)当X电极的质量减小了3.2g时,流经电流计的电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I、依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲烷燃烧生成CO2和液态水时放热55.625 kJ。则表示甲烷燃烧热的热化学方程式为________________________ 。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为______________ 。
(3)在25 ℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(1)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反应热ΔH为________ 。
II、锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-===Zn2+
Y极:2MnO2+2NH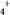 +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O
(1)X是电池的________ (填“正”或“负”,下同)极,Y是电池的________ 极。
(2)该电池总反应的离子方程式为:_______________________ 。
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为________ 。
(1)在25 ℃、101 kPa下,1 g甲烷燃烧生成CO2和液态水时放热55.625 kJ。则表示甲烷燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为
(3)在25 ℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(1)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反应热ΔH为
II、锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-===Zn2+
Y极:2MnO2+2NH
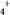 +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O(1)X是电池的
(2)该电池总反应的离子方程式为:
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究电化学原理与应用有非常重要的意义。
(1)锌锰电池(俗称干电池) 是一种一次电池,生活中应用广泛。
①锌锰电池负极上的电极反应式为:______________________________ 。
②与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是____________________ (回答一条即可)。
(2)铅蓄电池是最常见的二次电池:Pb+PbO2+2H2SO4 2PbSO4+2H2O。
2PbSO4+2H2O。
①充电时阴极反应为:________________________________________ 。
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为______ (假设溶液体积不变,产物无损耗)。
(3)图1是金属(M)-空气电池的工作原理,我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,电池反应为:___________________________ 。
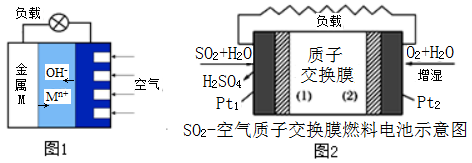
二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图2所示。Pt2上的电极反应式为:_______________________________________ 。
(4)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用电解法制取:Fe+2H2O+2OH− FeO42−+3H2↑,工作原理如图所示。
FeO42−+3H2↑,工作原理如图所示。
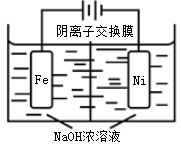
装置通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。电解一段时间后,c(OH−)降低的区域在_____________ (填“阴极室”或“阳极室”);阳极反应为:___________________________ 。
(1)锌锰电池(俗称干电池) 是一种一次电池,生活中应用广泛。
①锌锰电池负极上的电极反应式为:
②与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是
(2)铅蓄电池是最常见的二次电池:Pb+PbO2+2H2SO4
 2PbSO4+2H2O。
2PbSO4+2H2O。①充电时阴极反应为:
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为
(3)图1是金属(M)-空气电池的工作原理,我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,电池反应为:

二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图2所示。Pt2上的电极反应式为:
(4)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用电解法制取:Fe+2H2O+2OH−
 FeO42−+3H2↑,工作原理如图所示。
FeO42−+3H2↑,工作原理如图所示。
装置通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。电解一段时间后,c(OH−)降低的区域在
您最近一年使用:0次
【推荐3】(1)肼(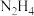 )-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
)-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为_____________________ 。
(2)科研人员新近开发一种由甲醇和氧气为燃料,强碱溶液作电解质溶液的新型手机电池,可供手机连续使用一个月。则通入甲醇的是_______ 填(“正”或“负”)极,写出该电池的负极反应式:_____________________ 。
(3)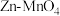 干电池应用广泛,电解质溶液是
干电池应用广泛,电解质溶液是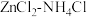 混合溶液。
混合溶液。
①该电池的负极材料是______ 。电池工作时,电子流向__________ 填(“正”或“负”)极。
②若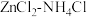 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速某电极的腐蚀,其主要原因是
,会加速某电极的腐蚀,其主要原因是_______ 。
③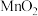 的生产方法之一是以石墨为电极,电解酸化的
的生产方法之一是以石墨为电极,电解酸化的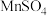 溶液。阳极的主要电极反应式是
溶液。阳极的主要电极反应式是_____________________ 。若电路中通过4mol电子,标准状况下产生气体的物质的量为_________ 。
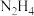 )-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
)-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为(2)科研人员新近开发一种由甲醇和氧气为燃料,强碱溶液作电解质溶液的新型手机电池,可供手机连续使用一个月。则通入甲醇的是
(3)
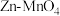 干电池应用广泛,电解质溶液是
干电池应用广泛,电解质溶液是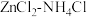 混合溶液。
混合溶液。①该电池的负极材料是
②若
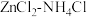 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速某电极的腐蚀,其主要原因是
,会加速某电极的腐蚀,其主要原因是③
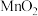 的生产方法之一是以石墨为电极,电解酸化的
的生产方法之一是以石墨为电极,电解酸化的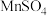 溶液。阳极的主要电极反应式是
溶液。阳极的主要电极反应式是
您最近一年使用:0次



