化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据原电池的本质判断,下列化学(或离子)方程式正确,且能设计成原电池的是___________。
(2)利用反应“ ”设计一个原电池,正极的电极反应式:
”设计一个原电池,正极的电极反应式:___________ 。
(3)以Pt为电极的氢氧燃料电池的工作原理示意图如图所示,稀 为电解质溶液。
为电解质溶液。___________ 极,发生___________ 反应(“氧化”或“还原”),写出b极的电极反应式___________ 。
②该电池提供 ,理论上消耗的氢气在标准状况下的体积为
,理论上消耗的氢气在标准状况下的体积为___________ L。
(1)根据原电池的本质判断,下列化学(或离子)方程式正确,且能设计成原电池的是___________。
A.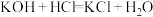 | B.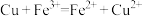 |
C.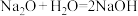 | D.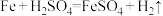 |
(2)利用反应“
 ”设计一个原电池,正极的电极反应式:
”设计一个原电池,正极的电极反应式:(3)以Pt为电极的氢氧燃料电池的工作原理示意图如图所示,稀
 为电解质溶液。
为电解质溶液。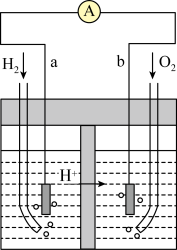
②该电池提供
 ,理论上消耗的氢气在标准状况下的体积为
,理论上消耗的氢气在标准状况下的体积为
更新时间:2024-04-21 17:54:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
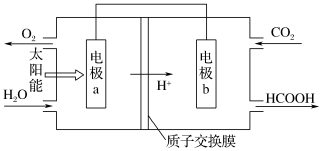
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作___________ 极,发生的电极反应式为___________ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为___________ 极,Y电极反应式为___________ 。
②Y极生成1 mol Cl2时,___________ mol Li+移向X极。
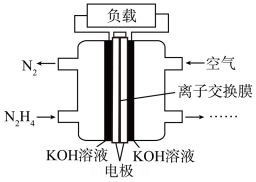
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH溶液作电解质溶液。负极反应式为___________ ,正极反应式为___________ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1 mol Cl2时,
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH溶液作电解质溶液。负极反应式为

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
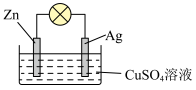
银电极上发生_______ 反应(“氧化”或“还原”),电极反应式为_______ ,该原电池的总反应离子方程式为_______ 。

银电极上发生
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】美国阿波罗宇宙飞船上使用了一种新型发电装置——氢氧燃料电池,其构造如图所示,其中A、B两个电极均由多孔的碳块组成。
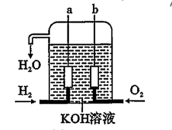
(1)①该电池的正极通入的气体是______ ,一段时间后正极区域溶液的pH值将________ ,负极的电极反应方程式为__________ 。
②若该电池工作时溶液中增加了1 mol H2O,则理论上电路中通过电子的物质的量为____ 。
(2)若将反应:Cu+2FeCl3=CuCl2+2FeCl2,设计成原电池。请写出负极材料_________ ,正极的电极反应方程式为__________ 。
(3)锌锰电池以锌皮、石墨棒为电极材料,电池工作时电流从____ 流向____ (填“锌皮”或“石墨棒”)

(1)①该电池的正极通入的气体是
②若该电池工作时溶液中增加了1 mol H2O,则理论上电路中通过电子的物质的量为
(2)若将反应:Cu+2FeCl3=CuCl2+2FeCl2,设计成原电池。请写出负极材料
(3)锌锰电池以锌皮、石墨棒为电极材料,电池工作时电流从
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】锂空气电池比传统的锂离子电池拥有更强的蓄电能力,是传统锂离子电池容量的10倍,其工作原理示意图如下:
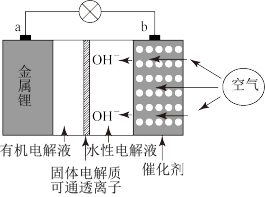
放电时,b电极为电源的________ 极,电极反应式为________

放电时,b电极为电源的
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯铝电池是一种新型的燃料电池,电解质溶液是KOH溶液,试回答下列问题:
(1)通入氯气的电极是___________ 极(填“正”或“负”),电极反应式为:___________ 。
(2)加入铝的电极是___________ 极(填“正”或“负”),电极反应式为:___________ 。
(3)电子从___________ 极流向___________ 极(填“Al”或“Cl2”)。
(1)通入氯气的电极是
(2)加入铝的电极是
(3)电子从
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。根据上述反应式,完成下列题目。

①下列叙述正确的是_________ 。
A.在使用过程中,电解质溶液的pH增大
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
②写出电池的总反应式:_______________________ 。
(2)某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

①电源A极的名称是________________ 。
②乙装置中电解反应的总离子方程式:_______________________ 。
③C电极与E电极产生的气体(相同条件)的体积比是_________ 。
④欲用丙装置给铜镀银,G应该是_______ (填“铜”或“银”)。
⑤装置丁中的现象是________________ 。

①下列叙述正确的是
A.在使用过程中,电解质溶液的pH增大
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
②写出电池的总反应式:
(2)某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

①电源A极的名称是
②乙装置中电解反应的总离子方程式:
③C电极与E电极产生的气体(相同条件)的体积比是
④欲用丙装置给铜镀银,G应该是
⑤装置丁中的现象是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e=Cu2+,还原反应式:2Fe3++2e-=2Fe2+。并由此实现了化学能与电能的相互转化。据此,回答下列问题。
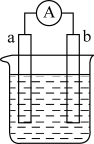
(1)将反应Zn+2H+=Zn2++H2↑拆写为两个“半反应式”,氧化反应式为:______ ,还原反应式为:______ 。
(2)由题(1)反应,设计成原电池如图所示:若电极a为Zn,电极b可选择材料:______ (只填一种);电解质溶液是______ 。
(3)由反应2H2+O2 2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极____ ,正极:_____ 。

(1)将反应Zn+2H+=Zn2++H2↑拆写为两个“半反应式”,氧化反应式为:
(2)由题(1)反应,设计成原电池如图所示:若电极a为Zn,电极b可选择材料:
(3)由反应2H2+O2
 2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
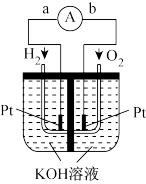
(1)氢氧燃料电池能量转化的主要形式是___________ ,在导线中电子流动方向为________ (用a、b表示)。
(2)负极反应式为___________ 。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2===2LiH Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是________ ,反应Ⅱ中的氧化剂是________ 。
②金属锂吸收的氢气与放出的氢气的物质的量之比为________ 。

(1)氢氧燃料电池能量转化的主要形式是
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2===2LiH Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是
②金属锂吸收的氢气与放出的氢气的物质的量之比为
您最近半年使用:0次

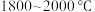 反应制备粗硅的化学方程式
反应制备粗硅的化学方程式 的化学方程式
的化学方程式 溶液)的负极反应方程式:
溶液)的负极反应方程式: 、
、 时,
时,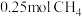 完全燃烧生成
完全燃烧生成 气体和液态
气体和液态 时,放出
时,放出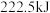 的热量。其热化学方程式为
的热量。其热化学方程式为

