美国阿波罗宇宙飞船上使用了一种新型发电装置——氢氧燃料电池,其构造如图所示,其中A、B两个电极均由多孔的碳块组成。
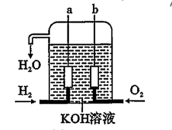
(1)①该电池的正极通入的气体是______ ,一段时间后正极区域溶液的pH值将________ ,负极的电极反应方程式为__________ 。
②若该电池工作时溶液中增加了1 mol H2O,则理论上电路中通过电子的物质的量为____ 。
(2)若将反应:Cu+2FeCl3=CuCl2+2FeCl2,设计成原电池。请写出负极材料_________ ,正极的电极反应方程式为__________ 。
(3)锌锰电池以锌皮、石墨棒为电极材料,电池工作时电流从____ 流向____ (填“锌皮”或“石墨棒”)

(1)①该电池的正极通入的气体是
②若该电池工作时溶液中增加了1 mol H2O,则理论上电路中通过电子的物质的量为
(2)若将反应:Cu+2FeCl3=CuCl2+2FeCl2,设计成原电池。请写出负极材料
(3)锌锰电池以锌皮、石墨棒为电极材料,电池工作时电流从
更新时间:2020-10-22 07:19:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)图1是高铁电池的模拟实验装置,放电时电池反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH
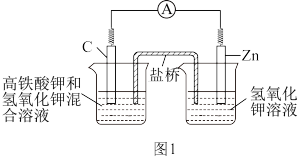

①该电池放电时正极的电极反应式为_________ 。
②盐桥中含有饱和KCl溶液,此盐桥中氯离子向______ 移动(填“左”或“右”)。
③如图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________________ 。
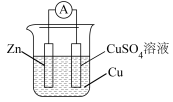
(2)某同学在研究如图所示的原电池装置时,测得Zn电极质量减轻6.5 g,Cu电极质量增加4.8 g。通过导线的电子数与反应转移电子总数的比值定义为电池的能量转换效率,则该实验中电池的能量转换效率为_______ 。
(3)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
负极反应式:2CO+2 −4e−═4CO2
−4e−═4CO2
正极反应式____________ ;总电池反应_______________ 。


①该电池放电时正极的电极反应式为
②盐桥中含有饱和KCl溶液,此盐桥中氯离子向
③如图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)某同学在研究如图所示的原电池装置时,测得Zn电极质量减轻6.5 g,Cu电极质量增加4.8 g。通过导线的电子数与反应转移电子总数的比值定义为电池的能量转换效率,则该实验中电池的能量转换效率为

(3)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
负极反应式:2CO+2
 −4e−═4CO2
−4e−═4CO2正极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
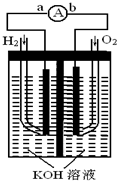
(1)氢氧燃料电池的能量转化主要形式是_______________________ ,在导线中电子流动方向为___ (用a、b 表示)。
(2)负极反应式为________ 。
(3)电极表面镀铂粉的原因为_____

(1)氢氧燃料电池的能量转化主要形式是
(2)负极反应式为
(3)电极表面镀铂粉的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学电池的发明,是贮能和供能技术的巨大进步。
(1)如图所示装置的总反应的离子方程式是________________________ 。其中铜片是________ (填“正极”或“负极”),该电极的反应式为__________________________ 。

(2)能证明该装置将反应释放的能量转化为电能的实验现象是:______________ 、_______________ 。
(3)外电路中,电子从______ 电极流出(填“Zn”或“Cu”)。
(4)汽车尾气中NO含量可通过NO传感器监测,工作原理如图:

Pt电极上氧气______________ 电子(得、失) 。
(1)如图所示装置的总反应的离子方程式是

(2)能证明该装置将反应释放的能量转化为电能的实验现象是:
(3)外电路中,电子从
(4)汽车尾气中NO含量可通过NO传感器监测,工作原理如图:

Pt电极上氧气
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】生活中平常使用的5号电池或7号电池都是锌锰干电池。锌锰干电池分为酸性锌锰干电池和碱性锌锰干电池两种。酸性锌锰干电池的组成如图所示。请根据原电池原理和构造思考以下问题。
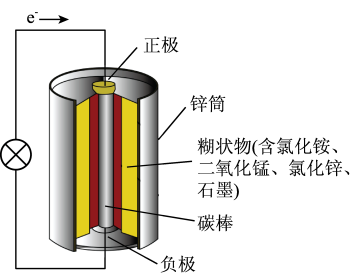
在酸性锌锰干电池中,负极反应物是_______ ,正极反应物分别是_______ 。负极材料是_______ ,正极材料是_______ 。离子导体是_______ 。

在酸性锌锰干电池中,负极反应物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。
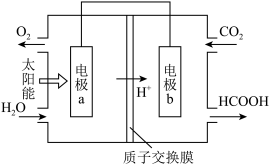
电极b为_______ 极。电极b上的电极反应为_______ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
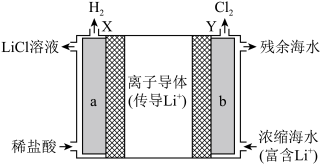
①X为_______ 极,Y极的电极反应式为_______ 。
②Y极生成1 mol Cl2时,_______ mol Li+移向_______ (填“X”或“Y”)极。
(3)某甲烷燃料电池采用铂作为电极材料,两个电极上分别通入CH4和O2,电解质溶液均为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解KOH溶液的实验如图所示,回答下列问题:
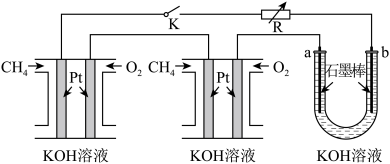
当闭合开关K,甲烷燃料电池工作时,电极a的电极反应式为_______ 。若每个 电池甲烷通入量为1.12 L (标准状况),且反应完全,则理论上最多能产生氢气的体积为_______ L(标况)。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。

电极b为
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1 mol Cl2时,
(3)某甲烷燃料电池采用铂作为电极材料,两个电极上分别通入CH4和O2,电解质溶液均为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解KOH溶液的实验如图所示,回答下列问题:

当闭合开关K,甲烷燃料电池工作时,电极a的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应中伴随着能量变化,请按要求回答下面的问题。
(1)下列反应中,生成物总能量大于反应物总能量的是___________ (填序号)。
①酸与碱的中和反应 ②碳酸氢钠和盐酸反应 ③镁和盐酸反应
④碳与二氧化碳反应 ⑤ 晶体与
晶体与 混合搅拌
混合搅拌
(2)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,如图是
等污染大气,如图是 和
和 反应生成
反应生成 的能量变化,则图中三种分子最稳定的是
的能量变化,则图中三种分子最稳定的是___________ (写分子式)。若反应生成 气体,则
气体,则___________ (填“吸收”或“放出”)___________  的热量。
的热量。 ,写出该铅酸蓄电池放电时正极的电极反应式
,写出该铅酸蓄电池放电时正极的电极反应式___________ 。
(4)根若依据反应 设计原电池,其工作原理示意图如图。
设计原电池,其工作原理示意图如图。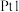 极为
极为___________ (填“正极”或“负极”)。
②溶液中 向
向___________ (填“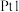 ”或“
”或“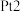 ”)极移动。
”)极移动。
③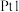 电极上的电极反应式为
电极上的电极反应式为___________ 。
④每转移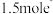 ,消耗标准状况下的
,消耗标准状况下的 。
。
(1)下列反应中,生成物总能量大于反应物总能量的是
①酸与碱的中和反应 ②碳酸氢钠和盐酸反应 ③镁和盐酸反应
④碳与二氧化碳反应 ⑤
 晶体与
晶体与 混合搅拌
混合搅拌(2)汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,如图是
等污染大气,如图是 和
和 反应生成
反应生成 的能量变化,则图中三种分子最稳定的是
的能量变化,则图中三种分子最稳定的是 气体,则
气体,则 的热量。
的热量。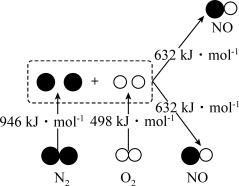
 ,写出该铅酸蓄电池放电时正极的电极反应式
,写出该铅酸蓄电池放电时正极的电极反应式(4)根若依据反应
 设计原电池,其工作原理示意图如图。
设计原电池,其工作原理示意图如图。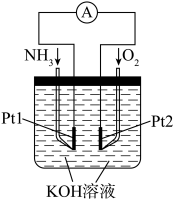
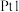 极为
极为②溶液中
 向
向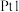 ”或“
”或“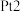 ”)极移动。
”)极移动。③
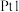 电极上的电极反应式为
电极上的电极反应式为④每转移
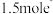 ,消耗标准状况下的
,消耗标准状况下的 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:
A. ; B.
; B. 。
。
判断能否设计成原电池A_______ ,B_______ (填“能”或“不能”)。
(2)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是_______ 。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的 均增大
均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:_______ 。构成原电池的电池工作时,溶液中 向
向_______ 极移动;电池工作完成后,溶液中 浓度
浓度_______ (填“增大”或“减小”或“不变”)。
④当乙中产生1.12L 标准状况
标准状况 气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中
气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中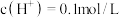
 设反应前后溶液体积不变
设反应前后溶液体积不变 。试确定原稀硫酸的物质的量浓度为
。试确定原稀硫酸的物质的量浓度为_______ 。
(3)当甲中产生1.12L 标准状况
标准状况 气体时,理论上通过导线的电子数目为
气体时,理论上通过导线的电子数目为___________ 。
(1)现有如下两个反应:
A.
 ; B.
; B. 。
。判断能否设计成原电池A
(2)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的
 均增大
均增大②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
 向
向 浓度
浓度④当乙中产生1.12L
 标准状况
标准状况 气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中
气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1L,测得溶液中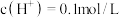
 设反应前后溶液体积不变
设反应前后溶液体积不变 。试确定原稀硫酸的物质的量浓度为
。试确定原稀硫酸的物质的量浓度为(3)当甲中产生1.12L
 标准状况
标准状况 气体时,理论上通过导线的电子数目为
气体时,理论上通过导线的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】SO2、H2S、Na2S等均是重要的含硫化合物。回答下列问题:
(1)向H2S溶液中加入NaOH固体时,不考虑温度变化,H2S的电离平衡_____ (填“正向”或“逆向”)移动;若要使H2S溶液中c(HS-)增大且使其电离平衡逆向移动,可以加入_____ (填化学式)固体。
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡_____ (填“正向”“逆向”或“不”)移动。试计算溶液中c( )∶c(
)∶c( )=
)=_____ (常温下H2SO3的电离平衡常数Ka1=1.0×10-2,Ka2=6.0×10-8)。
(3)将Na2S加入CuCl悬浊液中,发生的反应为2CuCl(s)+S2-(aq) Cu2S(s)+2Cl-(aq),该反应的平衡常数K=
Cu2S(s)+2Cl-(aq),该反应的平衡常数K=_____ [已知Ksp(CuCl)=1.2×10-6,Ksp(Cu2S)=2.5×10-43]。
(4)我国规定生活用水中镉排放的最大允许浓度为0.005mg·L-1.向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol·L-1时,废水中Cd2+的浓度为_____ mol·L-1[已知:Ksp(CdS)=7.9×10-27],此时是否符合生活饮用水卫生标准?_____ (填“是”或“否”)。
(5)一种新型燃料电池以SO2和空气为原料,工作原理如图所示:_____ 。
②相同条件下,放电过程中消耗的SO2和O2的体积之比为_____ 。
(1)向H2S溶液中加入NaOH固体时,不考虑温度变化,H2S的电离平衡
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡
 )∶c(
)∶c( )=
)=(3)将Na2S加入CuCl悬浊液中,发生的反应为2CuCl(s)+S2-(aq)
 Cu2S(s)+2Cl-(aq),该反应的平衡常数K=
Cu2S(s)+2Cl-(aq),该反应的平衡常数K=(4)我国规定生活用水中镉排放的最大允许浓度为0.005mg·L-1.向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol·L-1时,废水中Cd2+的浓度为
(5)一种新型燃料电池以SO2和空气为原料,工作原理如图所示:

②相同条件下,放电过程中消耗的SO2和O2的体积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图装置所示,是用氢氧燃料电池B进行的某电解实验:

(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH,则下列说法中正确的是________ 。
A. Li2NH中N的化合价是-1
B. 该反应中H2既是氧化剂又是还原剂
C. Li+和H-的离子半径相等
D. 此法储氢和钢瓶储氢的原理相同
(2)在电池B工作时:
①若用固体Ca(HSO4)2为电解质传递H+,则电子由________ 极流出,H+向______ 极移动(填“a”或“b ”)。
②b极上的电极反应式为_________ 。
③外电路中,每转移0.1 mol电子,在a极消耗________ L的H2(标准状况下)。
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCl溶液,则B工作时:
①电解池中X极上的电极反应式是______________ 。在X极这边观察到的现象是____________ 。
②检验Y电极上反应产物的方法是______________ 。

(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH,则下列说法中正确的是
A. Li2NH中N的化合价是-1
B. 该反应中H2既是氧化剂又是还原剂
C. Li+和H-的离子半径相等
D. 此法储氢和钢瓶储氢的原理相同
(2)在电池B工作时:
①若用固体Ca(HSO4)2为电解质传递H+,则电子由
②b极上的电极反应式为
③外电路中,每转移0.1 mol电子,在a极消耗
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCl溶液,则B工作时:
①电解池中X极上的电极反应式是
②检验Y电极上反应产物的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
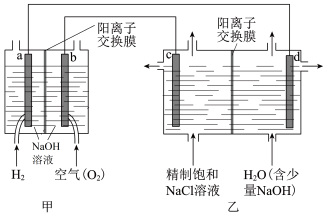
(1)a电极反应式是_______ 。
(2)乙装置中电解饱和NaCl溶液的化学方程式为_______ 。
(3)结合化学用语解释d极区产生NaOH的原因_______ 。
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用_______ 。
(5)下列说法正确的是_______ 。

(1)a电极反应式是
(2)乙装置中电解饱和NaCl溶液的化学方程式为
(3)结合化学用语解释d极区产生NaOH的原因
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用
(5)下列说法正确的是
| A.甲装置可以实现电能向化学能转化 |
| B.甲装置中Na+透过阳离子交换膜向a极移动 |
| C.乙装置中c极一侧流出的是淡盐水 |
| D.理论上,每消耗2.24LH2(标况下),可制得0.2molNaOH |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
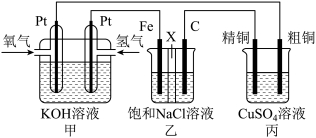
根据要求回答相关问题:
(1)通入氧气的电极为___________ (填“正极”或“负极”),负极的电极反应式为___________ 。
(2)铁电极为___________ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为___________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将___________ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为___________ ;丙装置中阴极析出铜的质量为___________ 。
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的___________ 极;该发生器中反应的总离子方程式为___________

(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
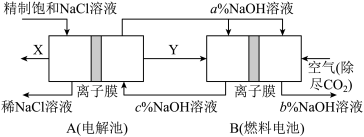
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为___________ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
(5)利用图制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的

(6)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电池是人类生产和生活中的重要能量来源。回答下列问题:
Ⅰ.硅是太阳能电池的重要材料,工业制备高纯硅的主要过程如下:

反应②、③的能量变化如右图所示。
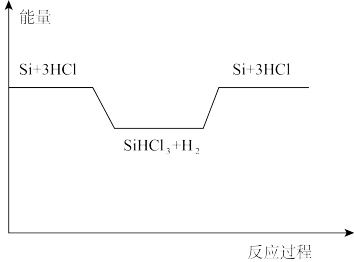
(1)硅在元素周期表中的位置是___________ 。
(2)反应①还生成了可燃性气体,其化学方程式为___________ 。
(3)反应②是___________ 反应(填“放热”或“吸热”)。已知 与
与 结构相似,反应③生成
结构相似,反应③生成 时有
时有___________  化学键断裂。
化学键断裂。
Ⅱ.某种燃料电池的工作原理如图所示,a、b均为铂电极。
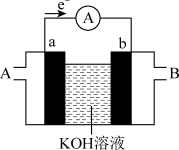
(4)电池工作时,电解质溶液中 向
向___________ 极迁移(填“a”或“b”),当有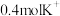 发生迁移,消耗
发生迁移,消耗 的体积为
的体积为___________ L(标准状况下)。
(5)若该电池是氢氧燃料电池,则通入氢气端是___________ (填“A”或“B”)。
Ⅰ.硅是太阳能电池的重要材料,工业制备高纯硅的主要过程如下:

反应②、③的能量变化如右图所示。

(1)硅在元素周期表中的位置是
(2)反应①还生成了可燃性气体,其化学方程式为
(3)反应②是
 与
与 结构相似,反应③生成
结构相似,反应③生成 时有
时有 化学键断裂。
化学键断裂。Ⅱ.某种燃料电池的工作原理如图所示,a、b均为铂电极。

(4)电池工作时,电解质溶液中
 向
向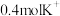 发生迁移,消耗
发生迁移,消耗 的体积为
的体积为(5)若该电池是氢氧燃料电池,则通入氢气端是
您最近一年使用:0次



