电池是人类生产和生活中的重要能量来源。回答下列问题:
Ⅰ.硅是太阳能电池的重要材料,工业制备高纯硅的主要过程如下:

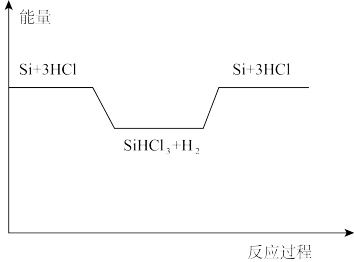
反应②、③的能量变化如右图所示。
(1)硅在元素周期表中的位置是___________ 。
(2)反应①还生成了可燃性气体,其化学方程式为___________ 。
(3)反应②是___________ 反应(填“放热”或“吸热”)。已知 与
与 结构相似,反应③生成
结构相似,反应③生成 时有
时有___________  化学键断裂。
化学键断裂。
Ⅱ.某种燃料电池的工作原理如图所示,a、b均为铂电极。
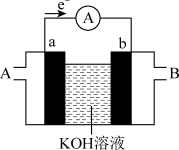
(4)电池工作时,电解质溶液中 向
向___________ 极迁移(填“a”或“b”),当有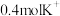 发生迁移,消耗
发生迁移,消耗 的体积为
的体积为___________ L(标准状况下)。
(5)若该电池是氢氧燃料电池,则通入氢气端是___________ (填“A”或“B”)。
Ⅰ.硅是太阳能电池的重要材料,工业制备高纯硅的主要过程如下:

反应②、③的能量变化如右图所示。

(1)硅在元素周期表中的位置是
(2)反应①还生成了可燃性气体,其化学方程式为
(3)反应②是
 与
与 结构相似,反应③生成
结构相似,反应③生成 时有
时有 化学键断裂。
化学键断裂。Ⅱ.某种燃料电池的工作原理如图所示,a、b均为铂电极。

(4)电池工作时,电解质溶液中
 向
向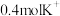 发生迁移,消耗
发生迁移,消耗 的体积为
的体积为(5)若该电池是氢氧燃料电池,则通入氢气端是
更新时间:2023-07-13 10:56:33
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请按要求回答下列问题:
(1)下列纯净物中:a.NaOH b.Ar c.MgCl2 d.HCl e.NH3 f.KNO3
①不含化学键的物质是_______ (填序号,下同)。
②既含有离子键又含有共价键的物质是______ 。
③只含有离子键的物质是________ 。
(2)下列变化中,不需要破坏化学键的是______ 。
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
(3)实验室盛放碱液的试剂瓶不能用玻璃塞,以氢氧化钠为例,用离子方程式表示其原因:_________ ,任写一个制造普通玻璃的主要反应的化学方程___________________ 。
(4)硅是良好的半导体材料,写出工业上生产粗硅的化学方程式:__________________________ 。
(1)下列纯净物中:a.NaOH b.Ar c.MgCl2 d.HCl e.NH3 f.KNO3
①不含化学键的物质是
②既含有离子键又含有共价键的物质是
③只含有离子键的物质是
(2)下列变化中,不需要破坏化学键的是
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
(3)实验室盛放碱液的试剂瓶不能用玻璃塞,以氢氧化钠为例,用离子方程式表示其原因:
(4)硅是良好的半导体材料,写出工业上生产粗硅的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下反应的化学方程式或离子方程式
(1)铝与氧化铁在高温下反应(铝热反应)_________________ ;
(2)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式___________
(3)工业上用焦炭和二氧化硅反应制得粗硅(Si)_____________________
(4)装氢氧化钠溶液的试剂瓶不用玻璃塞,原因用化学方程式表示为________
(1)铝与氧化铁在高温下反应(铝热反应)
(2)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式
(3)工业上用焦炭和二氧化硅反应制得粗硅(Si)
(4)装氢氧化钠溶液的试剂瓶不用玻璃塞,原因用化学方程式表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:_____________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3 遇水剧烈反应生成H2SiO3、HCl 和另一种气体,写出配平的化学反应方程式:_____________ ;H2 还原SiHCl3 过程中若混入O2,可能引起的后果是______________ 。
(2)下列有关硅材料的说法正确的是_____________ (填字母代号)。
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10 号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:
②整个制备过程必须严格控制无水无氧。SiHCl3 遇水剧烈反应生成H2SiO3、HCl 和另一种气体,写出配平的化学反应方程式:
(2)下列有关硅材料的说法正确的是
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10 号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)生石灰和氢氧化钠固体溶于水放热,而硝酸铵溶于水吸热。氢氧化钠固体溶于水放热的原因是_______ 。
(2)热胀冷缩是自然界的普遍现象,但当温度由0℃上升至4℃时,水的密度却增大,主要原因是_______ 。
(1)生石灰和氢氧化钠固体溶于水放热,而硝酸铵溶于水吸热。氢氧化钠固体溶于水放热的原因是
(2)热胀冷缩是自然界的普遍现象,但当温度由0℃上升至4℃时,水的密度却增大,主要原因是
您最近一年使用:0次
【推荐2】氢能的优点是燃烧热值高,无污染。目前工业制氢气的一个重要反应为 △H,反应的能量关系如图所示:
△H,反应的能量关系如图所示:

(1) △H
△H_______ 0(填“>”“<”或“=”)。
(2)过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热_______ (填“相等”或“不相等”),过程Ⅱ活化能_______ kJ/mol。
(3)已知:
 kJ·mol
kJ·mol

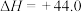 kJ·mol
kJ·mol
则H2(g)燃烧生成H2O(l)的热化学方程式为_______ 。
(4)向1 L 1 mol·L 的NaOH溶液中分别加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的由小到大的顺序为
的NaOH溶液中分别加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的由小到大的顺序为_______ 。
 △H,反应的能量关系如图所示:
△H,反应的能量关系如图所示:
(1)
 △H
△H(2)过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热
(3)已知:

 kJ·mol
kJ·mol

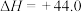 kJ·mol
kJ·mol
则H2(g)燃烧生成H2O(l)的热化学方程式为
(4)向1 L 1 mol·L
 的NaOH溶液中分别加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的由小到大的顺序为
的NaOH溶液中分别加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的由小到大的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学反应的过程,既有物质的转化过程,也有化学能与热能或其他能量的转化过程。
已知反应3A(g)+B(g) 2C(g)+D(g)的能量变化如图所示。
2C(g)+D(g)的能量变化如图所示。

(1)该反应_______ (填“吸收”或“释放”)_______ (用含 、
、 的式子表示)kJ能量。
的式子表示)kJ能量。
(2)断开3 mol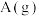 和1 mol
和1 mol  中的化学键吸收的能量
中的化学键吸收的能量_______ (填“>”、“<”或“=”)形成2 mol  和1 mol
和1 mol  中的化学键释放的能量。
中的化学键释放的能量。
(3)恒温下,在2 L恒容密闭容器中加入3 mol A、2 mol B,2 min末测得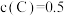 mol·L
mol·L 。
。
①2 min末,B的物质的量浓度为_______ 。
②下列说法正确的是_______ (填标号)。
A.向容器中通入少量的He(不参与反应),正反应速率减慢
B.总压强保持不变时,反应达到平衡状态
C.从容器中抽走部分D,正反应速率加快,逆反应速率减慢
(4)以反应 为原理设计成燃料电池,其利用率高,装置如图所示。
为原理设计成燃料电池,其利用率高,装置如图所示。
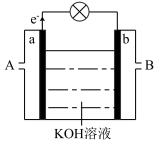
①A处加入的是_______ ,a处的电极反应式是_______ 。
②当消耗标准状况下3.36 L O2时,导线上转移的电子的物质的量是_______ mol。
已知反应3A(g)+B(g)
 2C(g)+D(g)的能量变化如图所示。
2C(g)+D(g)的能量变化如图所示。
(1)该反应
 、
、 的式子表示)kJ能量。
的式子表示)kJ能量。(2)断开3 mol
 和1 mol
和1 mol  中的化学键吸收的能量
中的化学键吸收的能量 和1 mol
和1 mol  中的化学键释放的能量。
中的化学键释放的能量。(3)恒温下,在2 L恒容密闭容器中加入3 mol A、2 mol B,2 min末测得
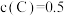 mol·L
mol·L 。
。①2 min末,B的物质的量浓度为
②下列说法正确的是
A.向容器中通入少量的He(不参与反应),正反应速率减慢
B.总压强保持不变时,反应达到平衡状态
C.从容器中抽走部分D,正反应速率加快,逆反应速率减慢
(4)以反应
 为原理设计成燃料电池,其利用率高,装置如图所示。
为原理设计成燃料电池,其利用率高,装置如图所示。
①A处加入的是
②当消耗标准状况下3.36 L O2时,导线上转移的电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)下列过程中属于吸热反应的是___________ 。
①灼热的木炭中通入CO2②碘升华③石灰石受热分解④水蒸气液化⑤Mg+2HCl=MgCl2+H2↑⑥CH4+2O2 CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋
CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋
(2)汽车发动机工作时会引发N2和O2反应,生成NOX等污染大气,其中生成NO的能量变化如图所示,则图中三种分子最稳定的是___________ 。若反应生成2molNO气体(“吸收”或“放出”)___________ 热量。

(3)如果将燃料燃烧设计成燃料电池就可避免NOX的生成,某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①使用时,空气从___________ 口通入(填“A"或“B");当外电路通过0.4mol的电子时,消耗O2的体积___________ L(标况下)。
②假设使用的“燃料”是甲烷(CH4),a极的电极反应式为___________ 。
(1)下列过程中属于吸热反应的是
①灼热的木炭中通入CO2②碘升华③石灰石受热分解④水蒸气液化⑤Mg+2HCl=MgCl2+H2↑⑥CH4+2O2
 CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋
CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋(2)汽车发动机工作时会引发N2和O2反应,生成NOX等污染大气,其中生成NO的能量变化如图所示,则图中三种分子最稳定的是

(3)如果将燃料燃烧设计成燃料电池就可避免NOX的生成,某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲烷(CH4),a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题。
(1)写出石膏的化学式_______ 。
(2)写出工业制粗硅的化学方程式_______ 。
(3)Na3N固体溶于水能产生NaOH和氨气,则Mg3N2固体与稀盐酸反应的化学方程式为_______ 。
(4)电解质为稀硫酸溶液的氢氧燃料电池原理示意图如图。写出该电池的正极电极反应式_______ 。
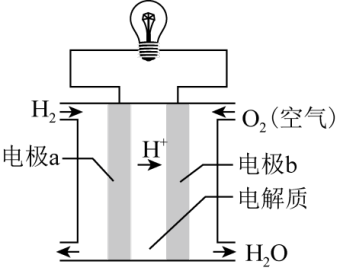
(1)写出石膏的化学式
(2)写出工业制粗硅的化学方程式
(3)Na3N固体溶于水能产生NaOH和氨气,则Mg3N2固体与稀盐酸反应的化学方程式为
(4)电解质为稀硫酸溶液的氢氧燃料电池原理示意图如图。写出该电池的正极电极反应式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知在250C、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
(1)若2 mol氢气完全燃烧生成水蒸气,则放出的热量___ (填“>”、“<”或“=”)570 kJ
(2)现有250C、1.013×105Pa下的H2和CH4的混合气体0.5mol,完全燃烧生成一定质量的CO2气体和10.8gH2O(l),放出203kJ的热量,则1molCH4 完全燃烧生成CO2气体和H2O(l)的热化学方程式为______________________ 。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成。

该电池的正极为:__________ (填A或B)。若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为 ____________ 。
(4)如果将上述装置中通往的H2改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为:_____________ 。
(1)若2 mol氢气完全燃烧生成水蒸气,则放出的热量
(2)现有250C、1.013×105Pa下的H2和CH4的混合气体0.5mol,完全燃烧生成一定质量的CO2气体和10.8gH2O(l),放出203kJ的热量,则1molCH4 完全燃烧生成CO2气体和H2O(l)的热化学方程式为
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成。

该电池的正极为:
(4)如果将上述装置中通往的H2改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:
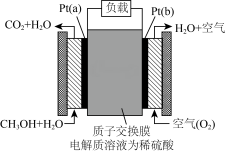
(1)该装置的能量转化形式为________ 。
(2)Pt(a)电极是电池________ (填“正”或“负”)极;
(3)电解液中的H+向_____ (填“a”或“b”)极移动;
(4)如果该电池工作时消耗1 mol CH3OH,则电路中通过___ mol电子。
(5)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化率高,其次是________ 。

(1)该装置的能量转化形式为
(2)Pt(a)电极是电池
(3)电解液中的H+向
(4)如果该电池工作时消耗1 mol CH3OH,则电路中通过
(5)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化率高,其次是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是某氢氧燃料电池的结构示意图,电解质为硫酸溶液。氢气在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2H2+O2=2H2O,完成下列问题:

(1)通H2的极为电池的________ 极(填“正”或“负”)。
(2)b极上的电极反应式为:________ 。
(3)每转移0.1mol电子,消耗H2的体积为________ L(标准状况下)。
(4)若将氢气换成二乙醚(C4H10O),将电解质溶液硫酸换成氢氧化钠溶液,去掉质子交换膜。
①则a极的电极反应式为________ 。
②电池工作一段时间后电解质溶液的pH______ (填“增大”“减小”或“不变”)。
(5)氢氧燃料电池为环境友好电池。而传统电池生产企业排放的工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。请用离子方程式说明上述除杂的原理___________ 。

(1)通H2的极为电池的
(2)b极上的电极反应式为:
(3)每转移0.1mol电子,消耗H2的体积为
(4)若将氢气换成二乙醚(C4H10O),将电解质溶液硫酸换成氢氧化钠溶液,去掉质子交换膜。
①则a极的电极反应式为
②电池工作一段时间后电解质溶液的pH
(5)氢氧燃料电池为环境友好电池。而传统电池生产企业排放的工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。请用离子方程式说明上述除杂的原理
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重要贡献。
(1)原电池的设计原理与某一类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是___________ (填字母)。
A.锌锰干电池工作一段时间后正极碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.太阳能电池的主要材料是高纯度的二氧化硅
D.铅蓄电池负极是 ,正极是
,正极是
E.原电池的负极金属的活动性一定比正极金属的活动性强
F.原电池工作时,阳离子向正极移动,阴离子向负极移动
(3)根据氧化还原反应: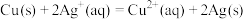 设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移
设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移 电子时两电极的质量差为
电子时两电极的质量差为___________ g。
(4)航天技术上使用的氢氧燃料电池具有高能,轻便和不污染环境等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为: 。
。
①酸式氢氧燃料电池的电解质是硫酸,其正极的电极反应式为___________ 。
②酸式氢氧燃料电池,工作一段时间后,电解质溶液的 将
将_______ (填“变大”、“变小”或“不变”)。
(5)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压,电池总反应式为: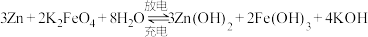 ,负极为
,负极为___________ ,放电时,溶液中 向
向___________ (填“正”或“负”)极移动。
(1)原电池的设计原理与某一类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
A. |
B. |
C.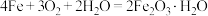 |
D. |
A.锌锰干电池工作一段时间后正极碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.太阳能电池的主要材料是高纯度的二氧化硅
D.铅蓄电池负极是
 ,正极是
,正极是
E.原电池的负极金属的活动性一定比正极金属的活动性强
F.原电池工作时,阳离子向正极移动,阴离子向负极移动
(3)根据氧化还原反应:
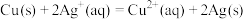 设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移
设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移 电子时两电极的质量差为
电子时两电极的质量差为(4)航天技术上使用的氢氧燃料电池具有高能,轻便和不污染环境等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为:
 。
。①酸式氢氧燃料电池的电解质是硫酸,其正极的电极反应式为
②酸式氢氧燃料电池,工作一段时间后,电解质溶液的
 将
将(5)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压,电池总反应式为:
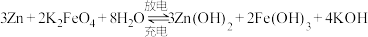 ,负极为
,负极为 向
向
您最近一年使用:0次



