金属的腐蚀
(1)概念:金属或合金与周围的_______ 发生_______ 反应而引起损耗的现象。其实质是金属原子_______ 电子变为阳离子,金属发生_______ 反应。
(2)根据与金属接触的_______ 不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如_______ 等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而_______ 。
②电化学腐蚀:当_______ 的金属与_______ 溶液接触时会发生_______ 反应,比较_______ 的金属发生氧化反应而被腐蚀。
(1)概念:金属或合金与周围的
(2)根据与金属接触的
①化学腐蚀:金属与其表面接触的一些物质(如
②电化学腐蚀:当
2023高二上·全国·专题练习 查看更多[1]
(已下线)【知识图鉴】单元讲练测选择性必修1第4单元01讲核心
更新时间:2023-07-20 14:43:13
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
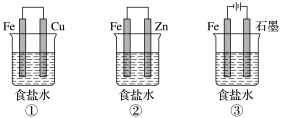
为防止金属Fe被腐蚀,可以采用上述________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________________ 。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_______________________ 。
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
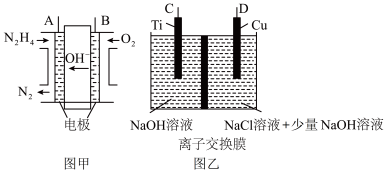
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为____________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
(3)当反应生成14.4 g Cu2O时,至少需要肼
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据信息填空
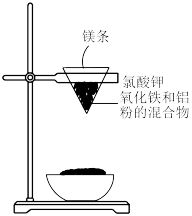
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:_______ 。
(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液______ 。该原电池中,三价铁离子向_______ (填“正极”或“负极”)移动。负极的电极反应式为_______

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式_______ 。
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法_______ (只填一种方法)。
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:

(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____。
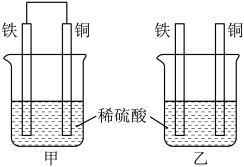
(2)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:_____ 。
A.甲中铜片质量减少、乙中铁片质量减少 B.甲、乙均为化学能转变为电能的装置
C.乙中铜片上没有明显变化 D.甲、乙两烧杯中 均减小
均减小
②在相同时间内,两烧杯中产生气泡的速度:甲_____ 乙(填“>”、“<”或“=”)。
③请写出甲、乙中构成原电池的正极电极反应式:_____ 。电池工作时,溶液中 向
向_____ 极(填“正”或“负”)移动。当甲中溶液质量增重27g时,电极上转移电子数目为_____ 。
④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为_____ 。
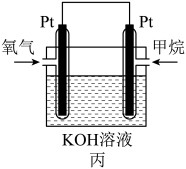
(3)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.通甲烷一极是电池的____ 极,电极反应为______ 。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____。
A. 与 与 反应 反应 | B. 与 与 燃烧反应 燃烧反应 |
C.灼热的炭与 反应 反应 | D.氢氧化钠与稀盐酸反应 |
(2)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
A.甲中铜片质量减少、乙中铁片质量减少 B.甲、乙均为化学能转变为电能的装置
C.乙中铜片上没有明显变化 D.甲、乙两烧杯中
 均减小
均减小②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出甲、乙中构成原电池的正极电极反应式:
 向
向④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为
(3)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.通甲烷一极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)如图所示是 Zn 和Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是______ (填序号)。

实验后的记录:
① Cu 为负极,Zn 为正极
② Cu 极上有气泡产生,发生还原反应
③ SO 向Cu 极移动
向Cu 极移动
④若有 0.5mol 电子流经导线,则可产生 0.25mol 气体
⑤电子的流向是:Cu→Zn
⑥ 正极反应式:Cu-2e- =Cu2+,发生氧化反应
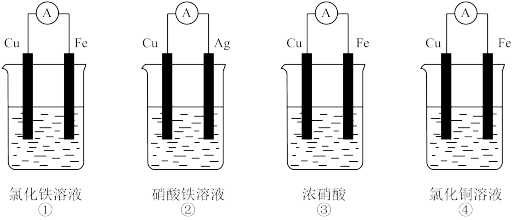
(2)为了验证 Fe3+与 Cu2+氧化性强弱,下列装置能达到实验目的是_____ (填序号)。
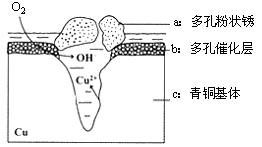
(3)图为青铜器在潮湿环境中因发生电化学反应而被腐蚀的原理示意图。

①腐蚀过程中,负极是____ (填图中字母“a”或“b”或“c”);
②环境中的 Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 Cu2(OH)3Cl,其离子方程式为____ ;

实验后的记录:
① Cu 为负极,Zn 为正极
② Cu 极上有气泡产生,发生还原反应
③ SO
 向Cu 极移动
向Cu 极移动④若有 0.5mol 电子流经导线,则可产生 0.25mol 气体
⑤电子的流向是:Cu→Zn
⑥ 正极反应式:Cu-2e- =Cu2+,发生氧化反应
(2)为了验证 Fe3+与 Cu2+氧化性强弱,下列装置能达到实验目的是

(3)图为青铜器在潮湿环境中因发生电化学反应而被腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的 Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 Cu2(OH)3Cl,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
(1)已知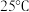 、
、 时,32g甲烷燃烧生成
时,32g甲烷燃烧生成 和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为
和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为___________ 。
Ⅱ.反应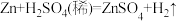 的能量变化如图所示。
的能量变化如图所示。___________ (填“吸热”或“放热”)反应。
(3)如图三个装置中,不能证明“锌与稀硫酸反应是吸热反应还是放热反应”的是___________ (填序号)
(5)请写出该电池的正极反应式___________
(6)若有1mol电子流过导线,则理论上在标准状况下,产生 的体积为
的体积为___________ L
(7)将稀 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是___________ (填“锌极”或“铜极”)。
(1)已知
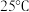 、
、 时,32g甲烷燃烧生成
时,32g甲烷燃烧生成 和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为
和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为Ⅱ.反应
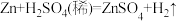 的能量变化如图所示。
的能量变化如图所示。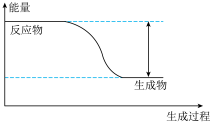
(3)如图三个装置中,不能证明“锌与稀硫酸反应是吸热反应还是放热反应”的是
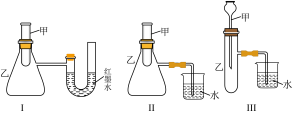
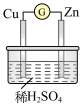
A.Cu极有 产生 产生 | B.锌作负极,发生还原反应 |
C. 向Zn极移动 向Zn极移动 | D.电子由Zn经导线流向Cu |
(6)若有1mol电子流过导线,则理论上在标准状况下,产生
 的体积为
的体积为(7)将稀
 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】研究和开发海水及其综合利用关系到人类的可持续发展。甲、乙两实验小组分别探索从海水中制取金属镁和单质溴的实验。
(1)甲实验小组的流程如图1。
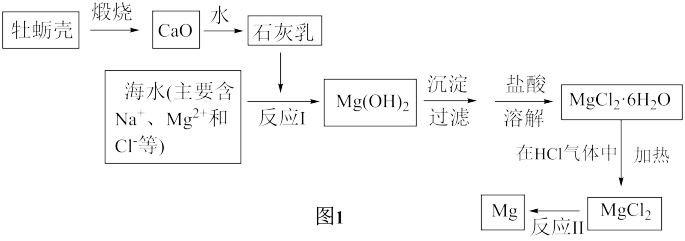
①制备石灰乳的化学反应方程式是___ 、___ 。
②写出反应Ⅰ的离子反应方程式___ 。
③反应Ⅱ是工业冶炼金属镁的反应原理,写出反应Ⅱ的化学反应方程式___ 。
(2)乙实验小组的流程如图2。

①分液漏斗使用前需检漏,检漏的方法为___ ,在步骤③中,萃取后分液漏斗内观察到的现象是___ 。
②写出步骤①发生反应的离子方程式___ ;写出步骤②发生反应的化学方程式___ 。
③在步骤③中,分离出溴单质的实验操作的名称是分液和___ ,后一实验操作用到的玻璃仪器有:___ 。
④在步骤①和步骤②之间设计了通入空气和水蒸气吹出的操作步骤的目的是___ 。
(3)图3各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为___ 。(填序号)

(1)甲实验小组的流程如图1。

①制备石灰乳的化学反应方程式是
②写出反应Ⅰ的离子反应方程式
③反应Ⅱ是工业冶炼金属镁的反应原理,写出反应Ⅱ的化学反应方程式
(2)乙实验小组的流程如图2。

①分液漏斗使用前需检漏,检漏的方法为
②写出步骤①发生反应的离子方程式
③在步骤③中,分离出溴单质的实验操作的名称是分液和
④在步骤①和步骤②之间设计了通入空气和水蒸气吹出的操作步骤的目的是
(3)图3各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属的腐蚀
(1)金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生_______________ 反应.
(2)金属腐蚀的类型
①化学腐蚀与电化学腐蚀
②析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例)
(1)金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生
(2)金属腐蚀的类型
①化学腐蚀与电化学腐蚀
| 类型 | 化学腐蚀 | 电化学腐蚀 |
| 条件 | 金属与其表面接触到的物质直接发生化学反应 | 不纯的金属接触到电解质溶液发生原电池反应 |
| 本质 |  |  |
| 现象 | 金属被腐蚀 | 较活泼金属被腐蚀 |
| 区别 | 无电流产生 | 有微弱电流产生 |
| 联系 | 电化学腐蚀比化学腐蚀普遍得多,腐蚀速率更快,危害也更严重 | |
②析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例)
| 类型 | 析氢腐蚀 | 吸氧腐蚀 | |
| 条件 | 水膜酸性较强 | 水膜酸性很弱或呈中性 | |
| 电 | 负极 |
| |
| 正极 | |||
| 总反应式 | |||
| 联系 | 吸氧腐蚀更普遍 | ||
您最近一年使用:0次
【推荐3】Ⅰ.当今社会的主题之一:发展经济,节能减排。而燃料电池因其无污染,且原料来源广可再生被人们青睐,广泛应用于生产、生活、科学研究中,现有如下图所示装置,所有电极均为Pt,请按要求回答下列问题:
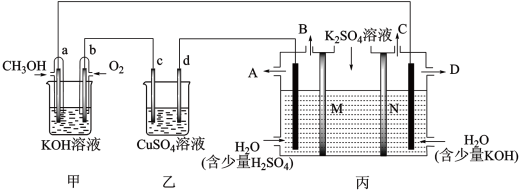
(1)写出a极的电极反应___________ 。
(2)若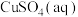 足够,电解一段时间后,要恢复到原来的状态,则可加入_____。(填序号)
足够,电解一段时间后,要恢复到原来的状态,则可加入_____。(填序号)
(3)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,M为_____ 离子交换膜(填“阴”或“阳”)。
Ⅱ.下图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

(4)①腐蚀过程中,负极是___________ (填“a”、“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为___________ 。

(1)写出a极的电极反应
(2)若
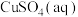 足够,电解一段时间后,要恢复到原来的状态,则可加入_____。(填序号)
足够,电解一段时间后,要恢复到原来的状态,则可加入_____。(填序号)A. | B. | C. | D. |
(3)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,M为
Ⅱ.下图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

(4)①腐蚀过程中,负极是
②环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】本题为《化学与生活(选修1)》选做题
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是_______ ;
②人体内最重要的供能物质是________ ;
③具有解热镇痛作用,用于治疗感冒的是_______ ;
④对支气管哮喘症有明显疗效的是_________ 。
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是________ ;
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的_______ 。
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是_________ ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是______ ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是_____________ 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是
②人体内最重要的供能物质是
③具有解热镇痛作用,用于治疗感冒的是
④对支气管哮喘症有明显疗效的是
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电化学保护法
金属在发生电化学腐蚀时,总是作为原电池_______ (阳极)的金属被腐蚀,作为_______ (阴极)的金属不被腐蚀,如果能使被保护的金属成为_______ ,就不易被腐蚀。
(1)牺牲阳极法
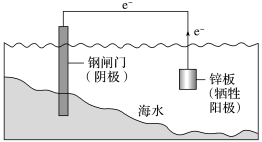
原理:原电池原理
要求:被保护的金属作_______ ,活泼性更强的金属作_______ 。
应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
实例 实验1:
如图装置反应一段时间后,往Fe电极区滴入2滴_______ 色K3[Fe(CN)6](铁氰化钾)溶液,观察实验现象。

已知Fe2+与[Fe(CN)6]3-反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
实例 实验2:
培养皿中放入含有NaCl的琼脂,并注入5~6滴酚酞和K3[Fe(CN)6]溶液,取两个2~3 cm的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。
(2)外加电流法
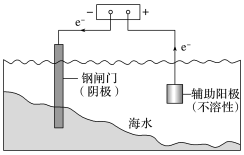
原理:电解池原理
要求:被保护的金属作为_______ ,与电源的_______ 相连。
应用:钢铁闸门,高压线铁架,地下管道连接直流电源的_______ 。
金属在发生电化学腐蚀时,总是作为原电池
(1)牺牲阳极法

原理:原电池原理
要求:被保护的金属作
应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
实例 实验1:
如图装置反应一段时间后,往Fe电极区滴入2滴

已知Fe2+与[Fe(CN)6]3-反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
| 实验装置 | 电流表 | 阳极(负极区) | 阴极(正极区) |
| 现象 | 指针 | Zn溶解 | 有 |
| 有关反应 | — | Zn-2e-=Zn2+ | 2H++2e-=H2↑ |
| 结论 | 溶液中不含 | ||
培养皿中放入含有NaCl的琼脂,并注入5~6滴酚酞和K3[Fe(CN)6]溶液,取两个2~3 cm的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。
| 实验装置 | 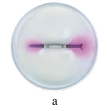 |  |
| 现象 | 铁钉周围 | 铁钉周围生成 |
| 结论 | 铁作为 | |

原理:电解池原理
要求:被保护的金属作为
应用:钢铁闸门,高压线铁架,地下管道连接直流电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
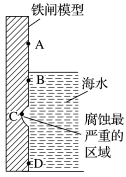
(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化学腐蚀称为______________ 。
②图中A、B、C、D四个区域,生成铁锈最多的是________ (填字母)。
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在________ 处(填字母)。
(2)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注:

________
(3)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是__________________ 。

(4)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是________ (填字母)。

A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001 mol气体

(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化学腐蚀称为
②图中A、B、C、D四个区域,生成铁锈最多的是
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在
(2)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注:

(3)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是

(4)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是

A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001 mol气体
您最近一年使用:0次