根据信息填空
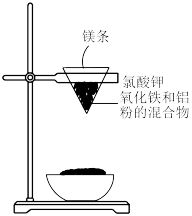
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:_______ 。
(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液______ 。该原电池中,三价铁离子向_______ (填“正极”或“负极”)移动。负极的电极反应式为_______

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式_______ 。
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法_______ (只填一种方法)。
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:

(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法
更新时间:2022-07-02 19:20:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铝是一种重要金属:
(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:___ 。
(2)铝还用于冶炼熔点较高的金属如钒、铬、锰等,请配平下列用铝冶炼金属钒的化学反应方程式:V2O5+Al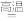 Al2O3+V。
Al2O3+V。___ 。该反应中氧化剂是___ ,要得到1mol金属钒,需要纯铝的质量___ g。
(3)铝与NaOH溶液反应的离子方程式为:___ 。在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为___ 。
(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:
(2)铝还用于冶炼熔点较高的金属如钒、铬、锰等,请配平下列用铝冶炼金属钒的化学反应方程式:V2O5+Al
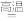 Al2O3+V。
Al2O3+V。(3)铝与NaOH溶液反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】除金、铂等极少数金属外,绝大多数金属元素以化合物形式存在于自然界中,将金属元素从其化合物中还原出来的工业工程称为金属的冶炼。下列材料描述了一些常见金属的冶炼方法。
①工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电解熔融的氯化镁;皮江法是硅在高温下还原氧化镁。
②霍尔-埃鲁铝电解法是以氧化铝为原料、冰晶石(Na3AlF6)为熔剂组成的电解质,在950-970℃的条件下通过电解的方法使电解质熔体中的氧化铝分解为铝和氧气。
③湿法炼铜是工业上常用的一种炼铜的方法。使用铁和硫酸铜溶液反应。
④工业上冶炼银的方法是加热条件下让氧化银分解。
⑤冶炼锰一般用铝热法,即在高温下用铝还原二氧化锰。
⑥相关各物质熔点见下表:
Ⅰ根据上述信息回答下列问题:
(1)影响金属冶炼方法的首要因素是________________________________ 。
(2)冶炼镁时电解熔融MgCl2而不电解熔融MgO,冶炼铝时电解熔融Al2O3而不电解熔融AlCl3的原因是______________________________________________________ 。
(3)写出铝热法冶炼锰的化学方程式_________________________________ ,一般使用铝热法冶炼的金属具有哪些性质_______________________________________ 。
Ⅱ下面是皮江法冶炼镁的工业流程示意图
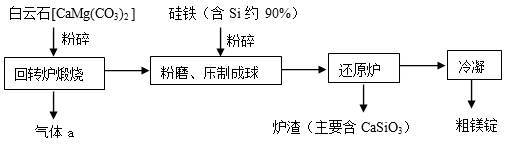
(1)气体a是________ 。
(2)白云石煅烧前粉碎的目的是______________________________________ 。
(3)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有________________________________ 、____________________________ 。
(4)还原炉中抽空气到近似真空的原因是_____________________________________ 。
①工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电解熔融的氯化镁;皮江法是硅在高温下还原氧化镁。
②霍尔-埃鲁铝电解法是以氧化铝为原料、冰晶石(Na3AlF6)为熔剂组成的电解质,在950-970℃的条件下通过电解的方法使电解质熔体中的氧化铝分解为铝和氧气。
③湿法炼铜是工业上常用的一种炼铜的方法。使用铁和硫酸铜溶液反应。
④工业上冶炼银的方法是加热条件下让氧化银分解。
⑤冶炼锰一般用铝热法,即在高温下用铝还原二氧化锰。
⑥相关各物质熔点见下表:
| 物质 | Al2O3 | AlCl3 | MgO | MgCl2 | Al | Mn | Mg |
| 熔点/℃ | 2303 | 190 | 2800 | 712 | 660 | 1244 | 649 |
(1)影响金属冶炼方法的首要因素是
(2)冶炼镁时电解熔融MgCl2而不电解熔融MgO,冶炼铝时电解熔融Al2O3而不电解熔融AlCl3的原因是
(3)写出铝热法冶炼锰的化学方程式
Ⅱ下面是皮江法冶炼镁的工业流程示意图

(1)气体a是
(2)白云石煅烧前粉碎的目的是
(3)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有
(4)还原炉中抽空气到近似真空的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应中伴随着能量变化。
(1)下列反应中,属于吸热反应的是______ (填序号)。
A.燃烧CO B.Ba(OH)2·8H2O晶体和NH4Cl晶体反应
C.铝和稀盐酸反应 D.NaOH溶液和稀盐酸反应
(2)按下图所示装置进行实验。

【实验现象】反应剧烈,火星四射,漏斗下方有红热熔融物流出。由此判断该反应是______ (填“吸热”或“放热”)反应,其反应的化学方程式是______ ,其能量变化可用下图中的______ (填“a”或“b”)表示。
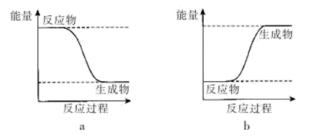
(3)依据事实,写出下列反应的热化学方程式。已知拆开1mol H﹣H键,1molN﹣H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为______ 。
(1)下列反应中,属于吸热反应的是
A.燃烧CO B.Ba(OH)2·8H2O晶体和NH4Cl晶体反应
C.铝和稀盐酸反应 D.NaOH溶液和稀盐酸反应
(2)按下图所示装置进行实验。

【实验现象】反应剧烈,火星四射,漏斗下方有红热熔融物流出。由此判断该反应是

(3)依据事实,写出下列反应的热化学方程式。已知拆开1mol H﹣H键,1molN﹣H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近一年使用:0次
【推荐1】铁和铁的化合物在工业生产和日常生活中都有广泛的用途。请回答下列问题:
(1)钢铁锈蚀是目前难以解决的现实问题,电化学腐蚀最为普遍。写出在潮湿空气中钢铁锈蚀时发生还原反应的电极反应式:___ 。
(2)爱迪生蓄电池的反应式为Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
①此装置中爱迪生蓄电池的负极是___ (填“a”或“b”),该电池工作一段时间后必须充电,充电时生成NiO2的反应类型是___ 。
②写出在用电解法制取高铁酸钠时,阳极的电极反应式___ 。
(1)钢铁锈蚀是目前难以解决的现实问题,电化学腐蚀最为普遍。写出在潮湿空气中钢铁锈蚀时发生还原反应的电极反应式:
(2)爱迪生蓄电池的反应式为Fe+NiO2+2H2O
 Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
①此装置中爱迪生蓄电池的负极是
②写出在用电解法制取高铁酸钠时,阳极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电化学原理在能量转换、物质制备、防止金属腐蚀等方面应用广泛。
(1)下图是常见电化学装置图
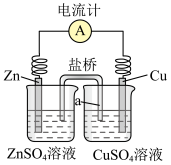
① 负极材料为Zn,其在此装置中的作用是___________ 。
② 若用一根铜丝代替盐桥插入两烧杯中,电流计指针也发生偏转,推测:其中一个为原电池,一个为电解池,写出a端发生的电极反应___________ 。
(2)下图探究金属Fe是否腐蚀的示意图
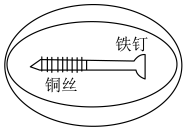
在培养皿中加入一定量的琼脂和饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ 端(填“左”或“右”),结合化学用语解释变红的原因___________ 。
(3)下图是氯碱工业电解饱和NaCl溶液的示意图

①电解饱和NaCl溶液的化学方程式是___________ 。
② NaOH溶液从___________ (填b或c)口导出。结合化学用语解释NaOH在此区域生成的原因___________ 。
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用___________ 。
(4)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①金属锂在电极___________ (填“A”或“B”)生成,发生的是___________ (填“氧化”或“还原”)反应。
②阳极产生两种气体单质,电极反应式分别是___________ ;___________ 。
(1)下图是常见电化学装置图

① 负极材料为Zn,其在此装置中的作用是
② 若用一根铜丝代替盐桥插入两烧杯中,电流计指针也发生偏转,推测:其中一个为原电池,一个为电解池,写出a端发生的电极反应
(2)下图探究金属Fe是否腐蚀的示意图

在培养皿中加入一定量的琼脂和饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
(3)下图是氯碱工业电解饱和NaCl溶液的示意图

①电解饱和NaCl溶液的化学方程式是
② NaOH溶液从
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用
(4)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①金属锂在电极
②阳极产生两种气体单质,电极反应式分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某课外活动小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的Fe发生___ 腐蚀(填“析氢”或“吸氧”),B极的电极反应式为___ 。
(2)若开始时开关K与b连接,下列说法正确的是___ (填序号);
a.溶液中Na+向A极移动
b.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
c.反应一段时间后加入适量稀盐酸可使电解质溶液恢复到电解前的浓度
d.若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子
此时装置内总反应的离子方程式为___ 。
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为___ ,此时通过阴离子交换膜的离子数___ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口___ (填“A”“B”“C”或“D”)导出。

(1)若开始时开关K与a连接,则B极的Fe发生
(2)若开始时开关K与b连接,下列说法正确的是
a.溶液中Na+向A极移动
b.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
c.反应一段时间后加入适量稀盐酸可使电解质溶液恢复到电解前的浓度
d.若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子
此时装置内总反应的离子方程式为
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。将变黑的银质器皿放入下图装置,一段时间后发现黑色会褪去。回答下列问题:
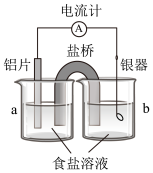
(1)铝为________ 极,KNO3盐桥中的________ 离子进入a烧杯中,银器的电极反应式为________ 。
(2)如不用盐桥,将铝片和银器插入一个盛食盐水的烧杯中处理,负极的电极反应式是_________ ,总反应方程式_______

(1)铝为
(2)如不用盐桥,将铝片和银器插入一个盛食盐水的烧杯中处理,负极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某学生进行下图所示的锌铜原电池的实验:
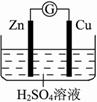
(1)从理论上讲,预期看到的现象是__________________________________ 。
(2)实验过程中,观察到锌极上有少量气泡逸出,铜极上有大量气泡逸出。试解释:
_________________________________________________________________

(1)从理论上讲,预期看到的现象是
(2)实验过程中,观察到锌极上有少量气泡逸出,铜极上有大量气泡逸出。试解释:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置。它可直接将化学能转化为电能,甲烷燃料电池以KOH溶液为电解质,其总反应的化学方程式为:CH4+2O2+2OH-= +3H2O。
+3H2O。
(1)负极上的电极反应为
(2)正极上的电极反应为
(3)消耗标准状况下的5.6 L O2时,有
(4)开始放电时,正极附近溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
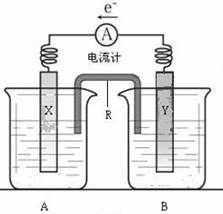
【推荐1】下图是铜锌原电池装置。其电池的总反应是:Zn(s)+CuSO4(aq)=ZnSO4(aq) + Cu(s)。R是盐桥,其作用是使两个烧杯中的溶液连成通路。
请回答以下问题:
(1)B中是ZnSO4溶液,电极Y的材料是________ 。
(2)R中的阳离子移向_______ (填A或B)中的溶液。
(3)X为原电池的______ 极,其电极反应式是_____________ 。

请回答以下问题:
(1)B中是ZnSO4溶液,电极Y的材料是
(2)R中的阳离子移向
(3)X为原电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将纯锌片和纯铜片按如图所示方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
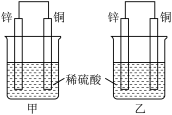
①下列说法正确的是_______ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置正极的电极反应式_______ 。

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的装置正极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】原电池反应一般是氧化还原反应,但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子,电子通过外电路输送到正极上,氧化剂在正极上得电子,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化。
(1)化学反应 ,
,_______ (填“能”或“不能”)通过原电池原理设计成化学电源,理由是_______ 。
(2)甲醇燃料电池结构简单、能量转化率高,工作原理如图所示。加入的a是_______ (填名称),该电极的名称是_______ (填“正”或“负”)极,其电极反应式为_______ 。
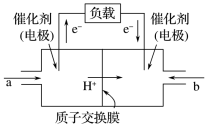
(3)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图所示。

①该电池的电流方向:由_______ (填“左”或“右”,下同)侧电极经过负载流向_______ 侧电极。
②当1mol 参与电极反应时,从
参与电极反应时,从_______ (填“左”或“右”,下同)侧穿过质子交换膜进入_______ 侧的 数目为
数目为_______  。
。
(1)化学反应
 ,
,(2)甲醇燃料电池结构简单、能量转化率高,工作原理如图所示。加入的a是

(3)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图所示。

①该电池的电流方向:由
②当1mol
 参与电极反应时,从
参与电极反应时,从 数目为
数目为 。
。
您最近一年使用:0次



