下图是铜锌原电池装置。其电池的总反应是:Zn(s)+CuSO4(aq)=ZnSO4(aq) + Cu(s)。R是盐桥,其作用是使两个烧杯中的溶液连成通路。
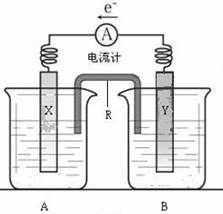
请回答以下问题:
(1)B中是ZnSO4溶液,电极Y的材料是________ 。
(2)R中的阳离子移向_______ (填A或B)中的溶液。
(3)X为原电池的______ 极,其电极反应式是_____________ 。

请回答以下问题:
(1)B中是ZnSO4溶液,电极Y的材料是
(2)R中的阳离子移向
(3)X为原电池的
10-11高二上·贵州黔西·期末 查看更多[1]
(已下线)2010年贵州册亨民族中学高二上学期期末考试化学卷(理)
更新时间:2011-01-17 19:02:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某科研小组用镍触媒废料(主要成分为Ni-Al合金,混有少量Fe、Cu、Zn、Pb及有机物) 制备NiO并回收金属资源的流程如下所示:
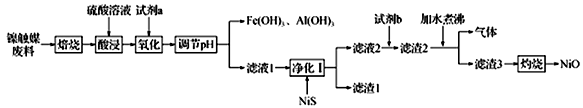
已知:相关数据如表1和表2所示
表1部分难溶电解质的溶度积常数(25℃)
表2 原料价格表
请回答下列问题:
(1)“焙烧”的目的是________________________________ 。
(2)“试剂a”的名称为__________________ ;选择该试剂的理由是________________________ 。
(3)“氧化”时反应的离子方程式为__________________________________________ 。
(4)欲使溶液中Fe3+和A13+的浓度均小于等于1.0×10-6 mol •L-1,需“调节pH”至少为_______________ 。
(5)“加水煮沸”时,反应的化学方程式为_______________________________ 。
(6)整个流程中,可回收的金属化合物为____________________________________ (填化学式)。
(7)氢镍电池是一种应用广泛的二次电池,放电时,该电池的总反应为NiOOH+MH==Ni(OH)2+M,当导线中流过2 mol电子时,理论上负极质量减少__________ g。充电时的阳极反应式为_______________________________________________ 。

已知:相关数据如表1和表2所示
表1部分难溶电解质的溶度积常数(25℃)
物质 | Ksp | 物质 | Ksp |
Fe(OH)3 | 4.0×10-38 | CuS | 6.3×10-34 |
Fe(OH)2 | 1.8×10-16 | ZnS | 1.6×10-24 |
Al(OH)3 | 1.0×10-33 | PbS | 8.0×10-28 |
Ni(OH)2 | 2.0×10-15 | NiS | 3.2×10-18 |
表2 原料价格表
物质 | 价格/(元•吨-1) |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
请回答下列问题:
(1)“焙烧”的目的是
(2)“试剂a”的名称为
(3)“氧化”时反应的离子方程式为
(4)欲使溶液中Fe3+和A13+的浓度均小于等于1.0×10-6 mol •L-1,需“调节pH”至少为
(5)“加水煮沸”时,反应的化学方程式为
(6)整个流程中,可回收的金属化合物为
(7)氢镍电池是一种应用广泛的二次电池,放电时,该电池的总反应为NiOOH+MH==Ni(OH)2+M,当导线中流过2 mol电子时,理论上负极质量减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学电池在通讯、交通及日常生活中有着广泛的应用。
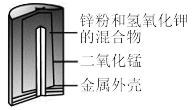
(1)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是______ (填名称),负极上发生的电极反应为______ 。若反应消耗13g负极材料,则电池中转移电子的物质的量______ mol。 。下列说法正确的是______(填标号)。
。下列说法正确的是______(填标号)。
(3)镁铝电池的构造如图所示,当电解质溶液为 溶液时,可知电池的负极材料为
溶液时,可知电池的负极材料为______ (填“Mg”或“Al”)反应式为______ 。
(1)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为
 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是
 。下列说法正确的是______(填标号)。
。下列说法正确的是______(填标号)。A.电解液中 的浓度始终保持不变 的浓度始终保持不变 |
B.放电时正极上的电极反应式为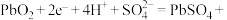 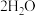 |
C.放电时,当外电路通过 电子时,理论上负极质量增加 电子时,理论上负极质量增加 |
D.放电时,溶液中的 向正极移动 向正极移动 |
(3)镁铝电池的构造如图所示,当电解质溶液为
 溶液时,可知电池的负极材料为
溶液时,可知电池的负极材料为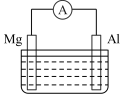
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学电池的发明,是贮能和供能技术的巨大进步。
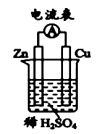
(1)如图所示装置中,Cu片是_______ (填“正极”或“负极”)。
(2)如图所示装置可将_______ (写化学方程式)反应释放的能量直接转变为电能;能证明产生电能的实验现象是_______ 、_______ 。
(3)锌在如图所示装置中的作用是传导电子、_______ 。
(4)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
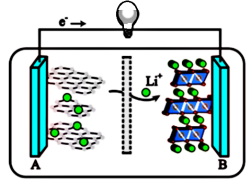
下列说法正确的是_______ (填序号)。
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动

(1)如图所示装置中,Cu片是
(2)如图所示装置可将
(3)锌在如图所示装置中的作用是传导电子、
(4)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。

下列说法正确的是
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a、b相连,a为正极;c、d相连,c为负极;a、c相连,c上产生气泡;b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:___________ 。
(2)碱性锌锰干电池比普通锌锰电池的使用寿命长且性能高,其构造如图所示,电池反应为: ,其中
,其中 作
作___________ 极,发生___________ 反应,电极反应式为___________ 。
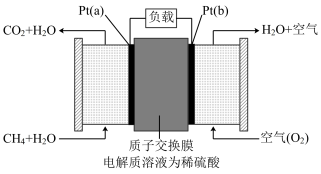
(3)甲烷燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:
①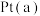 电极是电池的
电极是电池的___________ 极,电极反应式为___________ 。
②电解质溶液中的 向
向___________ (填“a”或“b”)极移动,电子流入的电极是___________ (填“a”或“b”)极。
③该电池工作时消耗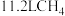 (标准状况下),则电路中通过
(标准状况下),则电路中通过___________ mol电子。
(2)碱性锌锰干电池比普通锌锰电池的使用寿命长且性能高,其构造如图所示,电池反应为:
 ,其中
,其中 作
作
(3)甲烷燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过。其工作原理的示意图如下,请回答下列问题:

①
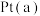 电极是电池的
电极是电池的②电解质溶液中的
 向
向③该电池工作时消耗
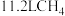 (标准状况下),则电路中通过
(标准状况下),则电路中通过
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学为了探究原电池产生电流的过程,设计了如图实验。
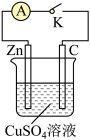
(1)打开K,观察到的现象为________________ 。
(2)关闭K,观察到的现象是_________ 。此电池的负极的电极反应式为_____ 。
(3)关闭K,溶液中阳离子向_______ (填“Zn”或“C”)极移动,外电路中,电子流动方向是________ 。

(1)打开K,观察到的现象为
(2)关闭K,观察到的现象是
(3)关闭K,溶液中阳离子向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为________________________ 。放电一段时间后,负极附近溶液的pH________ (填“升高”“降低”或“不变”)。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为________________________ 。请把该反应设计成一个原电池,在方框内面出原电池装置图(要求:标明电极材料和电解质溶液)。_______

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
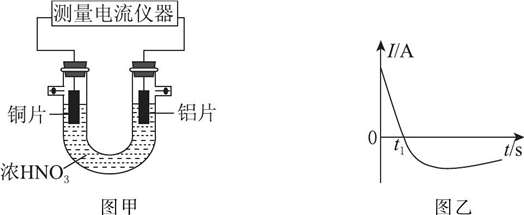
t1s前,原电池的负极是铝片,正极的电极反应式为____________ ,溶液中的H+向________ (填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是________________________ 。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

t1s前,原电池的负极是铝片,正极的电极反应式为
您最近一年使用:0次
【推荐1】氢能是一种极具发展潜力的清洁能源。
(1)已知 燃烧生成
燃烧生成 放出
放出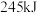 能量。该反应的热化学方程式为:
能量。该反应的热化学方程式为: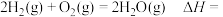
_______  。
。
(2)甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为: 。一定温度下,向体积为
。一定温度下,向体积为 的恒容密闭容器中充入
的恒容密闭容器中充入
 和
和 ,反应过程中测得
,反应过程中测得 的浓度与反应时间的关系如下表所示:
的浓度与反应时间的关系如下表所示:
① 时间段内用
时间段内用 表示该反应的速率
表示该反应的速率
_______  ,反应到
,反应到 时,
时, 的转化率为
的转化率为_______ 。
②下列措施可以使该反应速率加快的是_______ 。(填字母)
A.升高温度 B.减小甲烷的浓度 C.使用合适的催化剂
③下列能判断该反应已经达到化学平衡状态的是_______ 。(填字母)
A. 的浓度不再变化
的浓度不再变化
B.生成 的同时生成
的同时生成
C.容器内气体的密度不再发生变化
(3)某氢氧燃料电池已经成功应用在城市公交汽车上,其原理如下图所示。工作时的总反应为: ,负极的电极反应式为
,负极的电极反应式为_______ 。
(1)已知
 燃烧生成
燃烧生成 放出
放出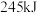 能量。该反应的热化学方程式为:
能量。该反应的热化学方程式为: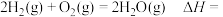
 。
。(2)甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为:
 。一定温度下,向体积为
。一定温度下,向体积为 的恒容密闭容器中充入
的恒容密闭容器中充入
 和
和 ,反应过程中测得
,反应过程中测得 的浓度与反应时间的关系如下表所示:
的浓度与反应时间的关系如下表所示:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.0 | 0.05 | 0.09 | 0.12 | 0.14 | 0.15 |
 时间段内用
时间段内用 表示该反应的速率
表示该反应的速率
 ,反应到
,反应到 时,
时, 的转化率为
的转化率为②下列措施可以使该反应速率加快的是
A.升高温度 B.减小甲烷的浓度 C.使用合适的催化剂
③下列能判断该反应已经达到化学平衡状态的是
A.
 的浓度不再变化
的浓度不再变化 B.生成
 的同时生成
的同时生成
C.容器内气体的密度不再发生变化
(3)某氢氧燃料电池已经成功应用在城市公交汽车上,其原理如下图所示。工作时的总反应为:
 ,负极的电极反应式为
,负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】将1 g琼脂加入250 mL烧杯中,再向其中加入50 mL饱和食盐水和150 mL水。搅拌、加热、煮沸,使琼脂溶解。稍冷后,趁热把琼脂溶液分别倒入两个培养皿中,各滴入5~6滴酚酞溶液和铁氰化钾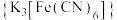 溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
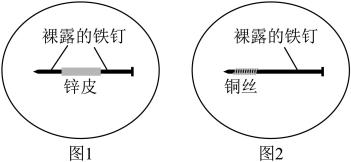
(1)图1中裸露的铁钉作___________ 极,该电极的电极反应式为___________ ,其附近可观察到的颜色变化为___________ 。
(2)图2中,在裸露的铁钉附近看到的颜色变化为___________ ,分析出现该颜色的原因:___________ ,靠近铜丝一端可观察到的颜色变化为___________ 。
(3)另一个同学也进行了上述实验操作,在图1装置中没有看到上述实验现象,其原因可能是___________ (填一条)。
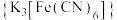 溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
(1)图1中裸露的铁钉作
(2)图2中,在裸露的铁钉附近看到的颜色变化为
(3)另一个同学也进行了上述实验操作,在图1装置中没有看到上述实验现象,其原因可能是
您最近一年使用:0次




