Ⅰ.铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
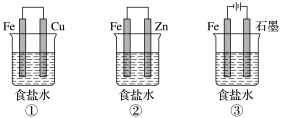
为防止金属Fe被腐蚀,可以采用上述________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________________ 。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_______________________ 。
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
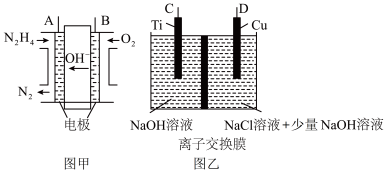
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为____________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
(3)当反应生成14.4 g Cu2O时,至少需要肼
更新时间:2019-11-23 12:44:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1)依据反应:2Ag+(aq)+Cu(s)⇌Cu2+(aq)+2Ag(s)设计的原电池如下图甲所示。
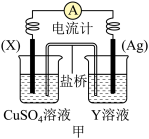
①电极X的材料是_______ ;Y溶液可以是_______ ;
②银电极上发生的电极反应式是_______ ,X电极上发生的电极反应为_______ 反应(填“氧化”或“还原”);外电路中的电子_______ (填“流出”或“流向”)Ag电极。
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是_______ (填离子符号)。
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀,可以采用电化学手段进行防腐。
①炒菜的铁锅未及时清洗容易生锈。写出铁锅生锈过程的正极反应式_______ 。
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用_______ (填写字母序号)。
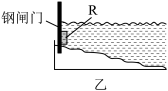
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的_______ 极。
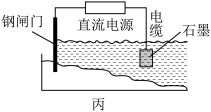
(1)依据反应:2Ag+(aq)+Cu(s)⇌Cu2+(aq)+2Ag(s)设计的原电池如下图甲所示。

①电极X的材料是
②银电极上发生的电极反应式是
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀,可以采用电化学手段进行防腐。
①炒菜的铁锅未及时清洗容易生锈。写出铁锅生锈过程的正极反应式
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用

A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的

您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】将干净的铁片浸在熔化的液体锌里可制得热镀锌铁板,这种铁板具有很强的耐腐蚀能力.镀锌铁板的镀锌层一旦被破坏后,锌将作为原电池的_________ 极,发生__________ 反应(填“氧化”或“还原”)而损耗,铁受到保护.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________ 。

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①A电极对应的金属是________ (写元素名称),
B电极的电极反应式是___________________________________ 。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________ mol。
③镀层破损后,不易被腐蚀的是___________ (填A或B)。
A.镀铜铁 B.镀锌铁 C. 镀锡铁
(1)下列哪个装置可防止铁棒被腐蚀

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①A电极对应的金属是
B电极的电极反应式是
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为
③镀层破损后,不易被腐蚀的是
A.镀铜铁 B.镀锌铁 C. 镀锡铁
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】甲烷燃料电池采用铂为电极,作为化学电源进行电解实验
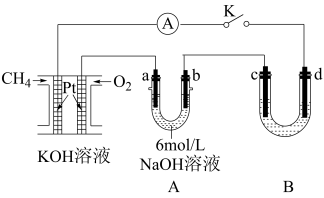
(1)写出燃料电池的正、负极反应式
负极:_______ ,
正极:_______ 。
(2)已知 A 中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾K2FeO4。资料显示: FeO 在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是_______ (填 a 或 b),该电极的电极反应式 为:_______ 。
(3)若 B 中的溶液为饱和 NaCl 溶液,用该装置模拟氯碱工业。
① 检验 c 电极产物的方法是:_______ 。
② 写出 d 电极的电极反应式:_______ 。
(4)若用 B 装置模拟工业粗铜精炼,则 c 极为_______ ,电解质溶液为_______ 。电解一段时间后, 电解液浓度_______ (填“变大” 、“不变”或“变小”);当燃料电池消耗标准状况下 O2的体积为 0.112L 时,理论上可以得到纯铜_______ g。

(1)写出燃料电池的正、负极反应式
负极:
正极:
(2)已知 A 中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾K2FeO4。资料显示: FeO
 在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是(3)若 B 中的溶液为饱和 NaCl 溶液,用该装置模拟氯碱工业。
① 检验 c 电极产物的方法是:
② 写出 d 电极的电极反应式:
(4)若用 B 装置模拟工业粗铜精炼,则 c 极为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列方程式正确且能设计成原电池的是________ 。
A.KOH+HCl=KCl+H2O
B.Cu+Fe3+=Fe2++Cu2+
C.Na2O+H2O=2NaOH
D.Fe+H2SO4=FeSO4+H2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(图Ⅰ、图Ⅱ中除连接的铜棒不同外,其他均相同)。有关实验现象,下列说法正确的是___________ 。
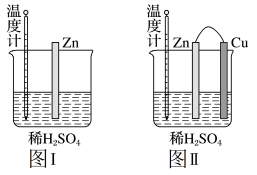
A.图Ⅰ中温度计的示数高于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速度比Ⅰ快
(3)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80,工作一段时间后,取出二者洗净,干燥后称重,总质量为54g,则产生氢气的体积_____ mL(标准状况)
(4)将铝片和镁片放入氢氧化钠溶液中,负极的电极反应式为:______________
(1)根据构成原电池的本质判断,下列方程式正确且能设计成原电池的是
A.KOH+HCl=KCl+H2O
B.Cu+Fe3+=Fe2++Cu2+
C.Na2O+H2O=2NaOH
D.Fe+H2SO4=FeSO4+H2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(图Ⅰ、图Ⅱ中除连接的铜棒不同外,其他均相同)。有关实验现象,下列说法正确的是

A.图Ⅰ中温度计的示数高于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速度比Ⅰ快
(3)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80,工作一段时间后,取出二者洗净,干燥后称重,总质量为54g,则产生氢气的体积
(4)将铝片和镁片放入氢氧化钠溶液中,负极的电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
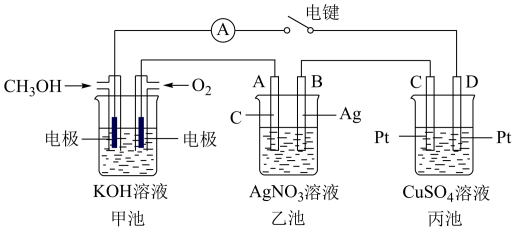
(1)甲池为__________ (填原电池、电解池或电镀池),通入甲醇电极的电极反应式 为______________________________________________ 。
(2)乙池中B电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为__________________________________________ 。
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为______ mL(标准状况)。
(4)丙池中,C上的电极反应式为____________________________________ 。

(1)甲池为
(2)乙池中B电极为
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为
(4)丙池中,C上的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】资料显示: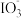 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为________ , 的还原性
的还原性________ I-(填“>”“=”或“<”)。
(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入________ ,蓝色迅速消失,随后再次变蓝。
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。
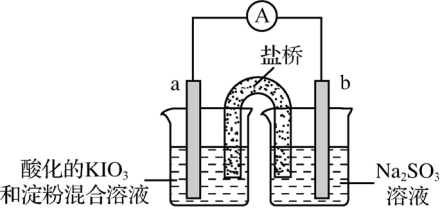
①甲同学在b电极附近的溶液中检测出了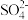
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。 在a极放电的产物是
在a极放电的产物是________ 。
③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是________ 。
④下列说法正确的是________ 。
a. a电极附近蓝色不再褪去时, 尚未完全氧化
尚未完全氧化
b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被 还原
还原
c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
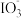 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为
 的还原性
的还原性(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。

①甲同学在b电极附近的溶液中检测出了
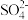
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。
 在a极放电的产物是
在a极放电的产物是③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是
④下列说法正确的是
a. a电极附近蓝色不再褪去时,
 尚未完全氧化
尚未完全氧化b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被
 还原
还原c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物是重要的化工原料,其转化一直是化学研究的热点。
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:
①氨催化氧化时会生成副产物N2O。生成含等物质的量氮元素的NO与N2O时,消耗的O2的物质的量之比为___________ 。
②一段时间后,观察到装置M中有白烟生成,该白烟成分是___________ (写化学式)。
(2)选择性催化还原法(SCR)工艺是以NH3 为还原剂,在催化剂作用下选择性地与NOx发生氧化还原反应生成无害化的N2和H2O。
已知:4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H1=-905.8 kJ/mol
N2(g)+ O2(g)=2NO(g) △H2 = +180 kJ/mol
则NH3与NO反应的热化学方程式为:___________ 。
(3)可用ClO2将氮氧化物转化成 。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为___________ 。
(4)纳米铁粉可去除水体中的 。
。
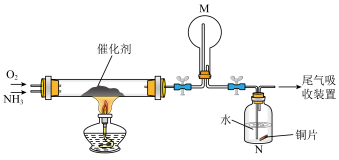
①将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中 ,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除
,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除 效率更高,其主要原因是
效率更高,其主要原因是___________ 。
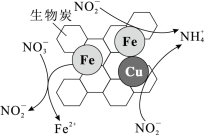
②控制其他条件不变,用纳米铁粉还原水体中的 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示。与初始溶液中
)浓度随时间变化如图所示。与初始溶液中 浓度相比,反应后溶液中所有含氮物质(
浓度相比,反应后溶液中所有含氮物质( 、
、 、
、 )总浓度减小,原因是
)总浓度减小,原因是___________ 。
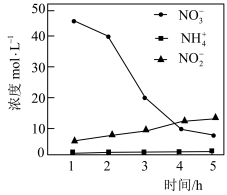
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:

①氨催化氧化时会生成副产物N2O。生成含等物质的量氮元素的NO与N2O时,消耗的O2的物质的量之比为
②一段时间后,观察到装置M中有白烟生成,该白烟成分是
(2)选择性催化还原法(SCR)工艺是以NH3 为还原剂,在催化剂作用下选择性地与NOx发生氧化还原反应生成无害化的N2和H2O。
已知:4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H1=-905.8 kJ/mol
N2(g)+ O2(g)=2NO(g) △H2 = +180 kJ/mol
则NH3与NO反应的热化学方程式为:
(3)可用ClO2将氮氧化物转化成
 。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为(4)纳米铁粉可去除水体中的
 。
。①将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中
 ,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除
,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除 效率更高,其主要原因是
效率更高,其主要原因是
②控制其他条件不变,用纳米铁粉还原水体中的
 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示。与初始溶液中
)浓度随时间变化如图所示。与初始溶液中 浓度相比,反应后溶液中所有含氮物质(
浓度相比,反应后溶液中所有含氮物质( 、
、 、
、 )总浓度减小,原因是
)总浓度减小,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】运用原电池原理可研究物质的性质或进行工业生产。
(1)某兴趣小组设计图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是____ (填“锌”或“铜”);当正极质量增加12.8g时,转移了____ mol电子。

(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。a是____ 极(填“正”或“负”),b电极反应式为____ ,生产过程中H+向____ (填“a”或“b”)电极区域运动。
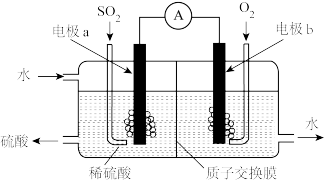
(1)某兴趣小组设计图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是

(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。a是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
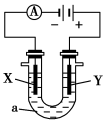
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为_______ ,在X极附近观察到的现象是_______ 。电解液中向X极方向移动的离子是_______ 。
②Y电极上的电极反应式为_______ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_______ ,电极反应式为_______ 。
②Y电极的材料是_______ ,电极反应式为_______ 。
(2)某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①放电时负极反应式为_______ ;
②充电时Fe(OH)3发生_______ 反应;(填“氧化”或“还原”)
③放电时1 mol K2FeO4发生反应,转移电子数是_______ 。

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
(2)某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①放电时负极反应式为
②充电时Fe(OH)3发生
③放电时1 mol K2FeO4发生反应,转移电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。现有下列两种制备ClO2的方法:
(1)方法一:可用亚氯酸钠和稀盐酸为原料制备,反应原理为5NaClO2+4HCl===5NaCl+4ClO2↑+2H2O。
①该反应中氧化剂和还原剂的物质的量之比是________ 。
②研究表明:若反应开始时盐酸浓度较大,则气体产物中有Cl2,用离子方程式解释产生Cl2的原因______ 。
(2)方法二:氯化钠电解法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO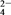 等杂质。某次除杂操作时,往粗盐水中先加入过量的
等杂质。某次除杂操作时,往粗盐水中先加入过量的_____ (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。
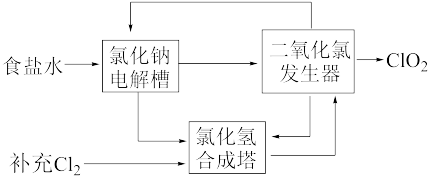
②该法工艺原理示意图如图所示。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2,氯化钠电解槽中阳极反应方程式为__________________ ,二氧化氯发生器中生成ClO2的化学方程式为_______________________ 。
(1)方法一:可用亚氯酸钠和稀盐酸为原料制备,反应原理为5NaClO2+4HCl===5NaCl+4ClO2↑+2H2O。
①该反应中氧化剂和还原剂的物质的量之比是
②研究表明:若反应开始时盐酸浓度较大,则气体产物中有Cl2,用离子方程式解释产生Cl2的原因
(2)方法二:氯化钠电解法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO
 等杂质。某次除杂操作时,往粗盐水中先加入过量的
等杂质。某次除杂操作时,往粗盐水中先加入过量的②该法工艺原理示意图如图所示。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2,氯化钠电解槽中阳极反应方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON内自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。

多孔电极b为_______ 极,a极的电极反应式为_______ ,工作时O2-的移动方向_______ (填“从a到b”或“从b到a”)。当消耗标况下一氧化碳33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量为_______ mol。
(2)现用蓄电池Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
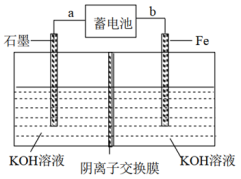
①电解时,石墨电极连接的a极上放电的物质为_______ (填“Fe”或“NiO2”)。
②写出电解池中铁电极发生的电极反应式_______ 。
③当消耗掉1molNiO2时,生成高铁酸钾_______ g。
(1)一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON内自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。

多孔电极b为
(2)现用蓄电池Fe+NiO2+2H2O
 Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
①电解时,石墨电极连接的a极上放电的物质为
②写出电解池中铁电极发生的电极反应式
③当消耗掉1molNiO2时,生成高铁酸钾
您最近一年使用:0次



