某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
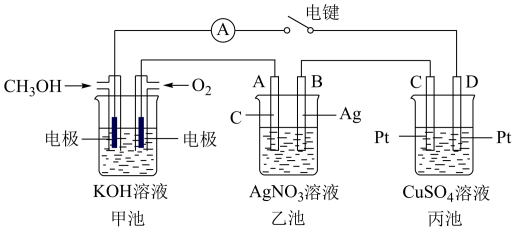
(1)甲池为__________ (填原电池、电解池或电镀池),通入甲醇电极的电极反应式 为______________________________________________ 。
(2)乙池中B电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为__________________________________________ 。
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为______ mL(标准状况)。
(4)丙池中,C上的电极反应式为____________________________________ 。

(1)甲池为
(2)乙池中B电极为
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为
(4)丙池中,C上的电极反应式为
更新时间:2020-01-27 11:21:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.某科研单位利用电化学原理,使用SO2来制备硫酸,装置如下图所示。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触,质子交换膜只允许 通过。
通过。

(1)通入 的电极为
的电极为______ (填“正极”或“负极”),其电极反应式为________ ,此电极区溶液的pH______ (填“增大”“减小”或“不变”)。
(2)电解质溶液中的 通过质子交换膜
通过质子交换膜________ (填“向左”或“向右”)移动,通入O2的电极反应式为_______ 。
Ⅱ.如上图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

(3)B极是电源的_____ (填“正极”或“负极”),一段时间后,丁中X极附近的颜色逐渐______ (填“变深”或“变浅”)。
(4)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为_____ 。
(5)现用丙装置给铜件镀银,则H应是________ 。若乙溶液体积为500mL,当乙中溶液的pH=13时,丙中镀件上析出银的质量为________ ,甲中溶液的pH_____ (填“变大”“变小”或“不变”)。
(6)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为______ 。
 通过。
通过。
(1)通入
 的电极为
的电极为(2)电解质溶液中的
 通过质子交换膜
通过质子交换膜Ⅱ.如上图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

(3)B极是电源的
(4)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(5)现用丙装置给铜件镀银,则H应是
(6)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】试运用电化学知识解决下列问题:
(1)利用自发进行的氧化还原反应: 设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:
设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:___________ ,正极反应式为___________ 。
(2)某原电池的工作原理为 ,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移
,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移 电子时,理论上两电极的质量差为
电子时,理论上两电极的质量差为___________ g。
(3)某研究团队合成的低配位 在碱性条件下催化
在碱性条件下催化 还原生成乙烯的电化学装置如图所示。
还原生成乙烯的电化学装置如图所示。
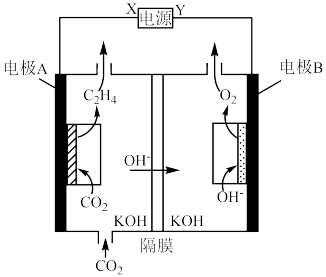
①Y为电源的___________ (填“正极”或“负极”)。
②电极A上的电极反应式为___________ 。
③理论上电极A上消耗的 与电极B上生成的
与电极B上生成的 的物质的量之比为
的物质的量之比为___________ 。
(4)下图为典型的电化学实验装置:

①甲池中C电极为___________ (填“阴极”或“阳极”),甲池的总反应式为___________ 。
②当甲池中 极质量增加
极质量增加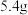 时,理论上乙池中
时,理论上乙池中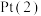 极的质量变化值为
极的质量变化值为___________ g。
(1)利用自发进行的氧化还原反应:
 设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:
设计一个原电池,可供选择的材料有:小灯泡、导线、铜棒、锌棒、石墨棒、硫酸铜溶液、硫酸锌溶液。请画出实验装置示意图:(2)某原电池的工作原理为
 ,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移
,该电池的两电极分别为铜棒、银棒,若开始时两电极质量相等,当电路中转移 电子时,理论上两电极的质量差为
电子时,理论上两电极的质量差为(3)某研究团队合成的低配位
 在碱性条件下催化
在碱性条件下催化 还原生成乙烯的电化学装置如图所示。
还原生成乙烯的电化学装置如图所示。
①Y为电源的
②电极A上的电极反应式为
③理论上电极A上消耗的
 与电极B上生成的
与电极B上生成的 的物质的量之比为
的物质的量之比为(4)下图为典型的电化学实验装置:

①甲池中C电极为
②当甲池中
 极质量增加
极质量增加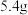 时,理论上乙池中
时,理论上乙池中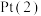 极的质量变化值为
极的质量变化值为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】1836年丹尼尔发明了世界上第一个实用电池,下图是实验室模拟原电池原理组装的丹尼尔电池,盐桥中装有饱和 溶液的琼胶,回答下列问题。
溶液的琼胶,回答下列问题。

(1)上图装置中能量的转化形式为___________ 能转化为___________ 能;
(2)在该原电池中,____ 是负极材料(填“锌片”或“铜片”),铜片一极发生___________ 反应(填“氧化”或“还原”);
(3)当该原电池开始工作时,盐桥中的 的移动方向是
的移动方向是____ (请在下列选项中选择) A. 流向硫酸锌溶液 B. 流向硫酸铜溶液
(4)该原电池的正极电极反应式为___________ ;当电路中转移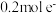 时,锌片溶解的质量为
时,锌片溶解的质量为___________  。
。
(5)图中甲池的总反应式为N2H4+O2=N2+2H2O。

①甲池中负极上发生的是___________ (填“氧化反应”或“还原反应”),乙池中SO 向
向___________ 移动(填“左”或“右”)。
②乙池中电解反应的离子方程为___________ 。
③要使乙池恢复到电解前的状态,应向溶液中加入___________ (填化学式)。
 溶液的琼胶,回答下列问题。
溶液的琼胶,回答下列问题。
(1)上图装置中能量的转化形式为
(2)在该原电池中,
(3)当该原电池开始工作时,盐桥中的
 的移动方向是
的移动方向是(4)该原电池的正极电极反应式为
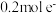 时,锌片溶解的质量为
时,锌片溶解的质量为 。
。(5)图中甲池的总反应式为N2H4+O2=N2+2H2O。

①甲池中负极上发生的是
 向
向②乙池中电解反应的离子方程为
③要使乙池恢复到电解前的状态,应向溶液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】纳米级Cu2O由于具有优良的催化性能而受到科学家的不断关注,下列为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是_________________________ 。
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为______________________________ ;电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解,通过离子交换膜的阴离子的物质的量为________ mol。(离子交换膜只允许OH-通过)
(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为________________ 。
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:___________________________ 。
| 方法Ⅰ | 用碳粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,原理为2Cu+H2O Cu2O+H2↑ Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为

(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b)。由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水通过)。
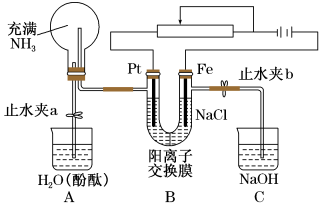
请分析并回答下列问题:
(1)写出B装置中的电极反应:阴极:_______ ;阳极:_______ 。
(2)①观察到A装置烧瓶中的现象:_______ 。
②烧杯中的现象_______ 并解释产生此现象的原因_______ 。
③B中U型管中现象_______
(3)当观察到A装置中的现象后,他们关闭止水夹a,打开止水夹b。再观察C装置中的现象,写出有关反应的化学方程式(是离子反应的写离子方程式):_______
(4)若想达到电解NaCl溶液的目的,应如何改进装置,请提出你的意见:_______

请分析并回答下列问题:
(1)写出B装置中的电极反应:阴极:
(2)①观察到A装置烧瓶中的现象:
②烧杯中的现象
③B中U型管中现象
(3)当观察到A装置中的现象后,他们关闭止水夹a,打开止水夹b。再观察C装置中的现象,写出有关反应的化学方程式(是离子反应的写离子方程式):
(4)若想达到电解NaCl溶液的目的,应如何改进装置,请提出你的意见:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图所示,若电解5 min时铜电极质量增加2.16 g,试讨论:

(1)电源电极X名称为______ 。
(2) pH变化:A______ ,B______ ,C______ 。
(3)通过5 min时,B中共收集224 mL气体(标况),溶液体积为200mL,则通电前硫酸铜溶液的物质的量浓度为______ 。
(4)若A中KCl溶液的体积也是200 mL,且电解过程中体积不变,电解后溶液中的氢氧根离子浓度是______ 。

(1)电源电极X名称为
(2) pH变化:A
(3)通过5 min时,B中共收集224 mL气体(标况),溶液体积为200mL,则通电前硫酸铜溶液的物质的量浓度为
(4)若A中KCl溶液的体积也是200 mL,且电解过程中体积不变,电解后溶液中的氢氧根离子浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是一个电化学过程的示意图,回答下列问题:

(1)甲池是_______ 装置,乙装置中电极A的名称是__________ 。
(2)甲装置中通入CH4的电极反应式为_______ ,乙装置中电极B(Ag)的电极反应式为______ ,丙装置中D极的产物是________ (写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25 ℃时的pH=________ (已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入________ (写化学式);其物质的量为____________ mol。

(1)甲池是
(2)甲装置中通入CH4的电极反应式为
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25 ℃时的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如下图所示,回答下列问题:

(1)该装置中B电极为电解池的___________ 极(填“阴”或“阳”);
(2)A电极上的电极反应式为______________________________________ ;
电解池总反应的离子方程式为___________________________________ ;
(3)电解过程中,电解质溶液的酸性______ (填“增强”、“减弱”或“不变”);
(4)下列实验操作中必要的是_________ (填写字母);
(5)铜的相对原子质量为________________ (用带有m、V的计算式表示)。

(1)该装置中B电极为电解池的
(2)A电极上的电极反应式为
电解池总反应的离子方程式为
(3)电解过程中,电解质溶液的酸性
(4)下列实验操作中必要的是
| A.称量电解前的电极的质量; |
| B.电解后,电极在烘干称量前,必须用蒸馏水冲洗; |
| C.刮下电解后电极上析出的铜,并清洗,称量; |
| D.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行; |
E.在有空气存在的情况下,烘干电极必须用低温烘干的方法。
(5)铜的相对原子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】认真观察下列装置,回答下列问题:

(1)装置B中PbO2上发生的电极反应方程式为__________________ 。
(2)装置A中总反应的离子方程式为____________________________ 。
(3)装置D中总反应的离子方程式为_____________________________ 。
(4)若装置E的目的是在Cu材料上镀银,则X为________ ,极板N的材料为__________ 。
(5)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为____ L(标准状况下)。

(1)装置B中PbO2上发生的电极反应方程式为
(2)装置A中总反应的离子方程式为
(3)装置D中总反应的离子方程式为
(4)若装置E的目的是在Cu材料上镀银,则X为
(5)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】依据氧化还原反应:2Ag+(aq)+Cu(s) Cu2+(aq)+2Ag(s)设计的原电池如图所示。
Cu2+(aq)+2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是_______ ;电解质溶液Y是____________ ;
(2)银电极为电池的___ 极,发生的电极反应为_____________ ;X电极上发生的电极反应为___________ ;
(3)外电路中的电子是从_______ 电极流向___________ 电极;
(4)如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,则

①a电极反应式为_________________________________ ;
②乙中的总反应为__________________________________ ;
③若整个电路中有2NA 个电子转移,则d电极产生__________ L气体 (标准状况)。
 Cu2+(aq)+2Ag(s)设计的原电池如图所示。
Cu2+(aq)+2Ag(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
(4)如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,则

①a电极反应式为
②乙中的总反应为
③若整个电路中有2NA 个电子转移,则d电极产生
您最近一年使用:0次
【推荐3】为实现“碳中和”目标,我国科学家做出了卓越贡献,最新科研成果之一为:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇 。
。
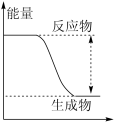
(1)转化过程的能量变化如图所示,可知 转化为
转化为 的反应为
的反应为___________ 反应(填“吸热”或“放热”)。
(2) 转化为
转化为 的总反应为
的总反应为 。下列描述能说明该反应已经达到限度的是___________。
。下列描述能说明该反应已经达到限度的是___________。
(3)科学家提出有关甲醇 的碳循环如图所示。
的碳循环如图所示。
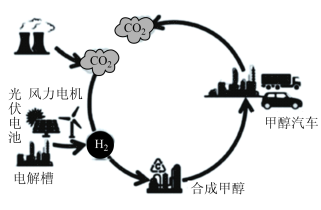
①碳循环过程中的能量转化方式有___________ (答出两种即可)。
②甲醇合成原理为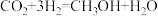 ,若合成甲醇
,若合成甲醇 ,则理论上可吸收工厂排放的
,则理论上可吸收工厂排放的
___________ L(标准状况);电解槽中发生电解反应 ,制备所需的
,制备所需的 转移的电子数为
转移的电子数为___________ (用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
 。
。(1)转化过程的能量变化如图所示,可知
 转化为
转化为 的反应为
的反应为
(2)
 转化为
转化为 的总反应为
的总反应为 。下列描述能说明该反应已经达到限度的是___________。
。下列描述能说明该反应已经达到限度的是___________。A. 的生成速率与 的生成速率与 的生成速率相等时 的生成速率相等时 |
| B.恒温恒容时,容器内气体的总压强不再随时间而改变时 |
| C.容器内气体的总质量不再改变时 |
D.恒容时, 、 、 、 、 、 、 的浓度相等时 的浓度相等时 |
 的碳循环如图所示。
的碳循环如图所示。
①碳循环过程中的能量转化方式有
②甲醇合成原理为
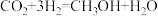 ,若合成甲醇
,若合成甲醇 ,则理论上可吸收工厂排放的
,则理论上可吸收工厂排放的
 ,制备所需的
,制备所需的 转移的电子数为
转移的电子数为 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次



